
3 курс / Патологическая физиология / pischevarenie
.pdf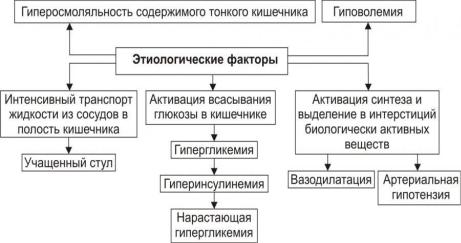
желудка в носовую часть глотки, а рефлекторное закрытие голосовой щели и угнетение дыхания препятствуют аспирации содержимого желудка в дыхательные пути.
Близкое расположение рвотного центра к другим центрам продолговатого мозга проявляется различными вегетативными эффектами при рвоте (гиперсаливация, тахикардия, снижение желудочной секреции).
Чаще рвота возникает при раздражении рецепторов желудка недоброкачественной пищей, токсическими веществами (в таких случаях рвоту называют желудочной).
Рефлексогенными зонами рвотного акта являются также задняя стенка глотки, илеоцекальная область кишки, рецепторы брюшины, жѐлчных протоков, жѐлчного пузыря, почек, мочевых путей, коронарных сосудов, перепончатого лабиринта внутреннего уха и др. Рвоту, вызываемую импульсами с периферических рефлексогенных зон, называют
периферической.
Рвота может иметь центральное происхождение и возникать при патологических процессах в области IV желудочка (опухоль, воспалительный процесс, интоксикация).
Рвота может возникнуть по механизму условного рефлекса – при неприятном запахе, виде несъедобной пищи (в лаборатории И.П. Павлова была воспроизведена условнорефлекторная рвота у собаки при сочетании индифферентного раздражителя (звук дудки) с инъекциями апоморфина).
Последствия рвоты. Защитное значение: при рвоте из желудка удаляются токсичные вещества, инородные тела. Патогенное значение: рвота (особенно многократная), приводит к целому ряду метаболических нарушений – метаболический алкалоз (потеря соляной кислоты), гипокалиемия и гипонатриемия (выведение ионов К+ и Na+ с рвотными массами).
Демпинг-синдром — патологическое состояние, развивающееся в результате быстрой эвакуации желудочного содержимого в тонкий кишечник. Развивается, как правило, после удаления части желудка (например, антерэктомия, гастрэктомия, пилоропластика).
Ранний демпинг-синдром развивается в течение первого часа после еды. Появляется чувство быстрого насыщения, диарея, вздутие и боли в животе. Отмечаются вегетативные реакции в виде покраснения лица, потливости, тахикардии. Эти симптомы связаны с поступлением большого количества гипертонического химуса из желудка или его культи в проксимальные отделы тонкой кишки. При этом происходит рефлекторная стимуляция моторики, обусловливающая диарею и внезапное увеличение содержания жидкости в тонкой кишке (гиперосмоляльность содержимого кишки), что ведет к ее растяжению. Вследствие этого возможна гиповолемия. Симптоматика усиливается в результате высвобождения кишечных гормонов и вазоактивных медиаторов (брадикинин, серотонин и др.), которые и вызывают вегетативные расстройства.
Рис. 5. Основные звенья патогенеза демпинг-синдрома.
11
Поздний демпинг-синдром развивается через 1,5-3 часа после еды. Появляется головокружение, головная боль, дрожание, сердцебиение, потливость, чувство голода, спутанность сознания. Симптомы могут появиться раньше, если пищевые продукты содержат большое количество простых углеводов (особенно сахарозу). Этот синдром обусловлен гипогликемией. Вначале происходит быстрое увеличение количества глюкозы в крови (гипергликемия) из-за резкого поступления сахаросодержащих компонентов пищи из желудка в проксимальные отделы тонкой кишки, которое сменяется гипогликемией. Это связано с тем, что быстрое всасывание углеводов стимулирует высвобождение инсулина, который циркулирует в крови дольше, чем глюкоза, и в конечном итоге развивается гипогликемия.
Язва желудка и 12-перстной кишки
Язва характеризуется появлением дефектов на слизистой оболочке желудка или двенадцатиперстной кишки и носит хронический характер.
Язвенная болезнь – хроническое, прогрессирующее заболевание, характеризующееся образованием участков деструкции слизистой оболочки желудка или двенадцатипѐрстной кишки.
Язвенная болезнь встречается у 6-10% взрослого населения, чаще у мужчин в возрасте до 50 лет. У 60-70% больных язвенная болезнь формируется в юношеском и молодом возрасте.
У подростков и молодых мужчин чаще развивается язвенная болезнь двенадцатиперстной кишки, у женщин и мужчин старших возрастных групп – язвенная болезнь желудка.
Причины язвенной болезни окончательно не установлены. Наибольшее значение в настоящее время придают хроническому стрессу (кортико-висцеральная теория) и инфицированию микроорганизмом Helicobacter pylory (инфекционная теория).
Факторы риска. Социальные факторы.
•Стрессы (переутомление, высокий темп жизни и т.д.). Данные факторы приводят к активации гипоталамо-гипофизарно-надпочечниковой системы, увеличивается образование АКТГ с последующим увеличением продукции кортикостероидов в корковом веществе надпочечников, которые уменьшают продукцию желудочной слизи и ухудшают ее качественный состав (снижают содержание сиаловых кислот). Кортикостероиды и катехоламины ухудшают процессы микроциркуляции, вызывают ишемию слизистой оболочки желудка. Формирование диффузного застойного возбуждения в ядрах гипоталамуса, повышают тонические влияния блуждающего нерва на желудочно-кишечный тракт.
•Курение. Никотин обусловливает подавление секреции защитных бикарбонатов, гиперсекрецию пепсиногена, снижение тонуса сфинктера привратника, что создаѐт условия для заброса кишечного содержимого, содержащего жѐлчь, в желудок.
•Алкоголь. Этанол непосредственно раздражает слизистую оболочку, стимулирует желудочную секрецию и разрушает слизисто–бикарбонатный барьер.
Алиментарные факторы. Частое употребление мясной пищи, которая стимулирует образование большого количества желудочного сока. Неупорядоченное, нерегулярное, однообразное питание. Частое употребление в пищу больших количеств специй, острых приправ, веществ, раздражающих слизистую оболочку желудка и кишечника (например, горчицы, уксуса, крепкого кофе).
Генетические факторы (наследственная предрасположенность, группа крови – 0 (I),
Rh+).
Инфекция. Доказана этиологическая роль Helicobacter pylory (НР) в развитии язв желудка
идвенадцатиперстной кишки. Этот микроорганизм выделяют у 90-95% больных язвенной болезнью.
Лекарственные средства. Ацетилсалициловая кислота и другие НПВС подавляют выработку защитных простагландинов (НПВС ингибируют активность циклооксигеназ → ↓
12
образование Pg). Глюкокортикоиды подавляют образование слизи и угнетают регенерацию слизистой оболочки желудка.
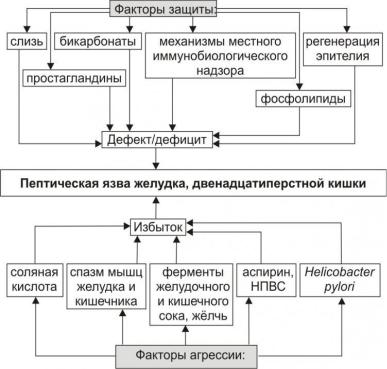
Патогенез. В основе патогенеза язвенной болезни лежит нарушение динамического равновесия между факторами агрессии (H. pylory, соляная кислота, спазм мышц желудка и кишечника, ферменты желудочного и кишечного сока, жѐлчь, НПВС и др.) и факторами защиты слизистой оболочки желудка (слизь, бикарбонаты, простагландины, механизмы местного иммунобиологического надзора, регенерация эпителия, микроциркуляция и др.).
Впатогенезе язвенной болезни желудка преимущественную роль играет снижение эффективности факторов защиты, а в развитии пептических язв двенадцатипѐрстной кишки – активация факторов агрессии.
Внастоящее время есть все основания рассматривать язвенную болезнь как инфекционное заболевание, так как доказана связь между развитием язвенной болезни и инфицированностью Helicobacter pylori. Австралийские ученые Р. Уоррен и Б. Маршалл в 2005 г. получили Нобелевскую премию за «неожиданное и потрясающее» открытие, которое они сделали в 1982 г.
–установили, что причиной гастритов и язвенной болезни желудка и двенадцатиперстной кишки является бактерия Helicobacter pylori.
Когда Б. Маршалл выделил чистую культуру бактерии, он провел на себе опыт самозаражения, и у него развился острый гастрит. В качестве средства лечения он использовал антибиотикотерапию.
Врезультате этого открытия появилась обоснованная возможность лечить язвенную болезнь антибиотиками, что увеличило частоту излечения язвенной болезни и уменьшило число рецидивов заболевания.
Helicobacter pylori – грамотрицательная анаэробная бактерия. Передаѐтся оральнооральным или фекально-оральным путем. Этот микроб синтезирует уреазу – фермент, который вызывает гидролиз мочевины, находящейся в желудочном секрете (выделяется слизистой желудка).
Рис. 6. Основные этиологические факторы язвы желудка и двенадцатиперстной кишки
13
В результате мочевина превращает в аммиак и углекислый газ, которые нейтрализуют соляную кислоту желудочного сока, что создает благоприятную среду для персистирования НР в желудке. Бактерии благодаря жгутикам и спиралевидной форме активно продвигаются и проникают из просвета желудка в эпителий его слизистой оболочки. Интенсивное размножение и колонизация HP ведут к повреждению эпителия слизистой желудка.
НР способен инициировать образование различных цитокинов. Одни цитокины (ИЛ-1, ФНО-α) активируют G-клетки антрального отдела желудка, вызывая гипергастринемию, и обкладочные клетки, образующие соляную кислоту. Другие цитокины (ИЛ-3, ИЛ-6, факторы роста) активируют пролиферацию эпителиоцитов в антральном отделе желудка, что может приводить к развитию гиперацидного гипертрофического гастрита, а затем – изъязвлению желудка.
Таким образом, инфицирование НР может быть первичным, а повышение секреции соляной кислоты – вторичным звеном в патогенезе язвенной болезни желудка. В подслизистом слое формируется воспалительный инфильтрат (состоящий из нейтрофилов, лимфоцитов, макрофагов, плазматических и тучных клеток), происходит некроз эпителия с образованием язвенного дефекта.
Патогенез язвы двенадцатипѐрстной кишки (ДПК). НР избирательно заселяют только метаплазированный эпителий и не поражают нормальную слизистую ДПК. Желудочная метаплазия (замещение цилиндрических клеток эпителия ДПК клетками желудочного эпителия) наблюдается у 90% больных дуоденальной язвой.
Метаплазия позволяет НР внедряться в клетки слизистой оболочки луковицы ДПК, делая их менее устойчивыми к повреждению соляной кислотой, пепсином, жѐлчью. Длительный заброс в луковицу ДПК кислого желудочного содержимого создает благоприятные условия для развития желудочной метаплазии ее эпителия.
Однако язвенная болезнь – это не классическая инфекция и одного инфицирования НР недостаточно для ее возникновения.
К главным этиологическим факторам язвенной болезни относят также нервнопсихический стресс. Под влиянием длительных или часто повторяющихся психоэмоциональных перенапряжений (нервные потрясения, профессиональные неудачи, семейные драмы) нарушается координирующая функция коры головного мозга в отношении подкорковых образований и особенно гипоталамуса.
Возникает стойкое возбуждение центров вегетативной нервной системы. Патологическая парасимпатическая импульсация из ЦНС приводит к гиперсекреции НС1 и гипермоторике желудка. Патологическая симпатическая импульсация из ЦНС приводит к выбросу катехоламинов в синапсах и мозговом веществе надпочечников, что вызывает трофические и гемодинамические нарушения в слизистой желудка.
Активация гипоталамо-гипофизарно-надпочечниковой системы вызывает усиленную выработку глюкокортикоидов, что влечет за собой гиперсекрецию желудочного сока, спазм сосудов, катаболический эффект (увеличенный распад и сниженный синтез белка). Все вышесказанное обусловливает формирование язвенных дефектов, уменьшение выработки слизи и снижение регенерации.
Проявления. Развивается болевой синдром, который характеризуется периодичностью (зависит от приема пищи, «голодные» боли), сезонностью (обострения весной и осенью), ритмичностью (ночные, дневные - от суточных ритмов выделения желудочно-кишечных соков). Болевой синдром является ведущим субъективным проявлением болезни в фазе обострения. Боль при язвах желудка локализуется в эпигастральной области и возникает через 15–60 мин после еды (ранние боли). При язве 12-перстной кишки боль локализуется в проекции пилодуоденальной зоны (возле пупка) и возникает через 1,5–3 ч после приѐма пищи (поздние), натощак (голодные) и ночью (ночные). На высоте боли может быть рвота, приносящая облегчение. Приѐм пищи улучшает состояние. Диспептические явления — отрыжка воздухом,
14
пищей, тошнота, изжога, запоры. Астеновегетативные проявления – снижение работоспособности, слабость, тахикардия, артериальная гипотензия.
Теории патогенеза язвообразования (исторический аспект). В каждой из этих теорий особая роль отведена определенному фактору, способному провоцировать «самопереваривание» желудка.
•Механический фактор (по Л. Ашоффу): повреждение слизистой желудка недостаточно обработанной пищей.
•Эндокринный фактор (по Г. Селье): ↑ АКТГ, ↑ глюкокортикоидов.
•Вегетативный фактор (по Дж. Бергману): генетически детерминированное или приобретенное повышение тонуса парасимпатического отдела вегетативной нервной системы.
•Нарушение кровообращения в желудке (по Р. Вирхову): ишемия слизистой желудка (тромбоз, стаз и т.д.) ведѐт к некрозу отдельных участков стенки желудка.
•Кислотно-пептический фактор (по К. Бернару): ↑ активность желудочного сока.
•Ацидозный фактор (по Р. Балинту): ↑ кислотность крови.
•Нарушение нейро-трофического контроля (по А.Д. Сперанскому).
•Расстройство высшей нервной деятельности – кортико-висцеральная (нейрогенная)
теория (по К.М. Быкову, И.Т. Курцину).
Симптоматические язвы желудка и двенадцатиперствной кишки.
• Стрессовые язвы. Основной причиной стрессового язвообразования является расстройство микроциркуляции слизистой оболочки желудка. Происходит спазм артериол мышечной оболочки желудка, стаз и далее – кровоизлияние в слизистый и подслизистый слой.
•Лекарственные язвы. НПВС (аспирин и др.), кортикостероиды – подавляют выработку слизи, угнетают регенерацию эпителия слизистой оболочки желудка.
•Язвы, обусловленные патологией эндокринной системы. Синдром Золлингера-
Эллисона (Zollinger, Ellison) – язвы желудка и 12-перстной кишки, возникающие в результате опухоли (гастринома) в поджелудочной железе или в других органах ЖКТ. Гастродуоденальные язвы при гиперпаратиреозе, сахарном диабете.
•Язвы при заболеваниях внутренних органов (дисциркуляторно-гипоксические).
Хронические неспецифические заболевания лѐгких, гипертоническая болезнь, атеросклероз, заболевания поджелудочной железы, хроническая почечная недостаточность и др.
Нарушения пищеварения в кишечнике
Кишечник выполняет секреторную, всасывательную и моторную функции, каждая из которых может нарушаться.
Нарушение секреторной функции тонкой кишки
Вся поверхность тонкого кишечника покрыта железами, продуцирующими «кишечный сок». Он содержит более 20 ферментов, необходимых для пищеварения.
Нарушение секреторной функции тонкого кишечника обусловлены врожденными и приобретенными энзимопатиями.
1. Врожденные энзимопатии. Чаще всего встречается дисахаридная недостаточность:
дефицит лактазы, сахаразы, изомальтазы, трегалазы (фермент, расщепляющий дисахарид трегалозу, содержащийся в грибах, водорослях). К редким формам врожденных энзимопатий относится дефицит энтерокиназы (фермент, активирующий панкреатический трипсиноген в трипсин). При недостатке энтерокиназы у детей наблюдаются тяжелые нарушения белкового обмена, гипопротеинемия, отеки, диарея.
К врожденным энтеропатиям относится глютеновая болезнь (целиакия), при развитии которой нарушается расщепление глютена (белковый компонент клейковины, склеивающий составные части некоторых злаков: пшеницы, ржи, ячменя, овса).
15
Основные теории патогенеза глютеновой болезни. Согласно первой – интестинальные эпителиальные клетки лишены соответствующей пептидазы. В связи с этим не происходит расщепления и последующего всасывания глютена. Непереваренный глютен и продукты его неполного расщепления оказывают токсическое действие на слизистую тонкой кишки.
Согласно второй теории первичную роль играют иммунологические реакции на глютен. Нерасщепленный глютен, взаимодействуя с иммуноцитами слизистой, приводит к их сенсибилизации, в частности к сенсибилизации лимфоцитов. В результате – образуются различные продукты иммуногенеза: антитела к глютену, иммунизированные лимфоциты, лимфокины, вызывающие повреждение кишечного эпителия с нарушением его переваривающей
ивсасывающей функций.
2.Приобретенные энзимопатии связаны с недостаточной продукцией как одного (моноэнзимопатии), так и нескольких (полиэнзимопатии) ферментов кишечного сока (например, при энтеритах).
Нарушение полостного и пристеночного пищеварения
Пищеварение в тонкой кишке обеспечивает деполимеризацию питательных веществ до стадии, в которой они всасываются в кровь и лимфу.
Пищеварение в тонкой кишке сначала происходит в ее полости (полостное пищеварение), а затем в зоне кишечного эпителия с помощью ферментов, фиксированных на его микроворсинках, и в гликокаликсе (пристеночное пищеварение).
Нарушение полостного пищеварения. Нарушение полостного пищеварения зависит, прежде всего, от расстройства выделения панкреатического сока и жѐлчи в 12-перстной кишке.
Отсутствие жѐлчи (ахолия) или недостаточное еѐ поступление (гипохолия) в 12-перстную кишку возникает вследствие нарушения проходимости жѐлчных путей, поражения паренхимы печени или расстройства регуляции образования и выведения жѐлчи.
При ахолии нарушается переваривание жиров из-за отсутствия жѐлчных кислот, участвующих в эмульгировании жиров, активирующих липазу и способствующих всасыванию жирных кислот. Снижается перистальтика кишок (активируется жѐлчью), бактерицидное действие жѐлчи. Нарушение всасывания жиров сопровождается дефицитом жирорастворимых витаминов (A, D, E, K).
Изменения панкреатической секреции вызывают серьѐзные нарушения пищеварения, так как поджелудочная железа вырабатывает все основные пищеварительные ферменты.
Нарушения секреции панкреатического сока наблюдаются при закупорке или сдавлении протока поджелудочной железы, воспалении поджелудочной железы (панкреатит), при нарушении нервно-гуморальных механизмов регуляции панкреатической секреции.
При отсутствии панкреатического сока нарушается переваривание жиров (стеаторея), белков (креаторея – непереваренные мышечные волокна), углеводов (амилорея), нарушается гидролиз нуклеиновых кислот. Нарушение переваривания белков возникает при недостаточной выработке пептидаз поджелудочной железы, а также при нарушении их активации. Так трипсиноген (фермент поджелудочной железы) активируется энтерокиназой кишечного сока, остальные протеолитические ферменты и фосфолипаза активируются трипсином.
Синдром мальдигестии (от лат. mal - болезнь, digestium - пищеварение) – нарушение преимущественно полостного пищеварения.
Причины мальдигестии: снижение секреторной функции желудка, тонкой кишки, поджелудочной железы, жѐлчеотделения; нарушения двигательной функции желудочнокишечного тракта (застой или ускорение пассажа пищевого химуса).
Проявления. Вздутие живота, избыточное газообразование, ощущение переливания и урчание в животе. В более выраженных случаях отмечается стеаторея, креаторея, амилорея, диарея и похудение. Трофические расстройства (сухость кожи, ломкость ногтей и т.д.) при синдроме нарушенного пищеварения практически не развиваются (в этом заключается принципиальное отличие синдрома мальдигестии от синдрома нарушенного всасывания).
16
Нарушение пристеночного (мембранного) пищеварения. Пристеночное пищеварение,
осуществляется в зоне кишечного эпителия с помощью ферментов, фиксированных на цитоплазматической мембране микроворсинок и в гликокаликсе.
В гликокаликсе ферменты расщепляют продукты полостного гидролиза – олигомеры, образующиеся из крупномолекулярных веществ, до димеров. На цитоплазматической мембране микроворсинок расщепление идет до конечного продукта – мономеров, которые поступают в энтероциты и далее в кровь и лимфу, т.е. всасываются.
Ферменты, осуществляющие пристеночное пищеварение, имеют двоякое происхождение: часть их адсорбируется из полости тонкой кишки (поступают в составе панкреатического и кишечного соков), и они связываются с гликокаликсом микроворсинок, а другая часть переносится из энтероцитов (клеток кишечного эпителия), фиксируясь на цитоплазматических мембранах микроворсинок. Пристеночное (мембранное) пищеварение осуществляется ферментами: олигосахаридазы, олигопептидазы, фосфатазы и др.
Причины нарушения пристеночного пищеварения.
•Нарушения структуры ворсинок и микроворсинок, уменьшение их числа на единицу поверхности (воспалительные, дистрофические, склеротические изменения слизистой оболочки кишки).
•Наследственная или приобретенная недостаточность ферментов, участвующих в пристеночном пищеварении (например, непереносимость молока при уменьшении или отсутствии галактокиназы). Наследственная недостаточность пристеночного пищеварения проявляется у детей в раннем возрасте при расширении пищевого рациона с включением в него новых продуктов, содержащих непереносимый дисахарид. Приобретенная недостаточность чаще является следствием заболеваний тонкой кишки (хронического энтерита, вирусного гепатита и других инфекций).
•Расстройства кишечной перистальтики, что приводит к нарушению переноса пищевых веществ из полости кишки на поверхность энтероцитов (например, хронические энтериты и др.).
•Недостаточность полостного пищеварения (малорасщепленные крупные молекулы не проходят в щеточную кайму эпителия ворсинок).
Проявления недостаточности пристеночного пищеварения аналогичны таковым при синдроме недостаточности всасывания (синдром мальабсорбции).
Нарушение всасывательной функции кишечника
В процессе мембранного пищеварения в тонкой кишке гидролиз пищевых веществ и перенос их через мембрану клеток тесно сопряжены. Поэтому к нарушению всасывания приводят все факторы, вызывающие расстройства мембранного пищеварения.
Нарушения всасывания проявляются в виде его замедления или патологического усиления.
Замедление всасывания лежит в основе синдрома мальабсорции (от лат. mal - болезнь, ab - от, sorbeo - поглощаю) – селективном нарушении всасывания одного или нескольких питательных веществ.
Синдром мальабсорции бывает врожденным (первичным) и приобретенным (вторичным).
Причины мальабсорбции.
•Недостаточность полостного и мембранного пищеварения.
•Уменьшение всасывающей поверхности тонкого кишечника.
•Гиперкинез тонкого кишечника (диарея).
•Расстройство крово- и лимфотока в стенках кишечника.
•Деструкция, дистрофия, атрофия энтероцитов (например, при воспалении тонкого кишечника).
Проявления. Синдром мальабсорбции характеризуется расстройством питания, хронической диареей, трофическими нарушениями. Важным клиническим симптомом является
17
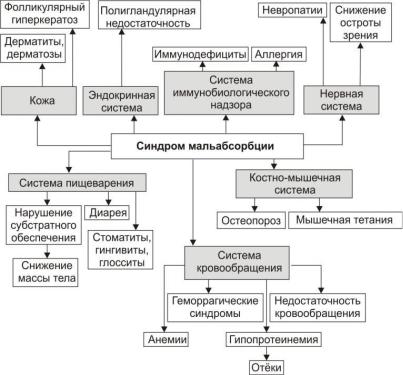
потеря массы тела (похудание). Нарушаются все виды обмена: белковый, жировой, углеводный, минеральный, витаминный.
Возникают трофические расстройства. Кожа становится сухой, с пониженным тургором, волосы – сухими, тусклыми, отмечается выпадение волос. Наблюдаются изменения ногтевых пластинок, их ломкость, а также болезни десен, гиперемия языка, сглаженность его сосочков (дефицит витаминов В2, В6, В12, никотиновой кислоты). Отмечается кровоточивость десен (дефицит витамина С). Вследствие дефицита Са2+ возникает остеопороз, вплоть до остеомаляции. Нарушение всасывания железа ведет к развитию железодефицитной анемии. Нарушение всасывания белков сопровождается гипопротеинемией с развитием отечного синдрома.
Диарея обусловлена накоплением в полости кишечника осмотически активных веществ. Наблюдается полифекалия с остатками непереваренной пищи, стеаторея (признак нарушения всасывания жира).
Могут наблюдаться нарушения деятельности эндокринных желез по типу плюригландулярной недостаточности – развитие эндокринопатии с поражением гипофиза, надпочечников, половых желез.
Рис. 7. Основные проявления синдрома мальабсорбции.
Патологическое усиление всасывания связано с повышенной проницаемости кишечной стенки при ее воспалении. Оно может сопровождаться всасыванием веществ антигенной природы и сенсибилизацией организма. Это чаще всего возникает у грудных детей. Например, в неизмененном виде всасывается белок коровьего молока или куриного яйца, что вызывает сенсибилизацию организма с развитием аллергических реакций.
Нарушение моторной функции кишечника
Нарушение моторной функции кишечника проявляется в ускорении (диарея) или замедлении перистальтики (запор) кишечника.
Диарея (от греч. diarrhоeа– истекаю) — учащенная дефекация (более 2–3 раз в сутки), при которой кал имеет жидкую консистенцию.
18
Диарея может быть острая (не превышает 2-3 недели) и хроническая (длится 4-6 недель и более), инфекционная и неинфекционная, воспалительная и невоспалительная.
Повышение двигательной функции кишок возникает при воспалительных процессах (энтерит, колит), под влиянием механических или химических раздражений плохо переваренной пищей, в результате действия бактериальных токсинов, при расстройстве нервной и гуморальной регуляции.
Примером нарушения нервной и гуморальной регуляции моторики кишок является «синдром раздраженного кишечника», при котором отрицательные эмоции изменяют двигательную и всасывательную функции кишок, становятся причиной вощникновения боли в животе и поноса, часто сменяющегося запором.
Основные типы диареи по механизму развития.
1.Гиперосмолярный тип диареи – имеет место снижение абсорбции воды и электролитов. Такой тип диареи отмечается при нарушениях всасывания, что наблюдается при глютеновой болезни, ишемической болезни тонкой кишки, врожденных дефектах всасывания, при хроническом панкреатите, раке поджелудочной железы, дефиците желчных кислот (например, при механической желтухе), недостаточном времени контакта химуса с кишечной стенкой (при резекции тонкой кишки, энтероанастомозах). Характер стула: полифекалия и стеаторея.
Так, при резекции подвздошной кишки («синдром короткой кишки») может возникнуть диарея вследствие нарушения всасывания жѐлчных кислот и свободных жирных кислот, стимулирующих секрецию жидкости в толстой кишке.
2.Гиперсекреторный тип диареи характеризуется повышенной секрецией воды и электролитов в просвет кишки. Это связано с воздействием на слизистую кишечника бактериальных эндотоксинов (при холере, кишечных инфекциях), жѐлчных и жирных кислот, глюкагона, простагландинов, слабительных лекарственных средств (касторовое масло, фенолфталеин и др.). Характер стула: обильный, водянистый
Гиперсекреторная диарея отмечается также при увеличении гидростатического давления в сосудах кишечника вследствие поражения лимфатической системы (например, при лимфоэктазах, амилоидозе кишечника, лимфоме) и правожелудочковой сердечной недостаточности.
Тяжелые поносы (так называемая водная диарея) могут быть обусловлены избыточной продукцией вазоактивного интестинального полипептида (ВИП), который в норме содержится в ЖКТ, в основном в стенке тонкой кишки. ВИП продуцируют некоторые опухоли – ганглионейробластомы (чаще у детей) и аденомы островковой ткани поджелудочной железы – ВИПомы (синдром Вернера-Моррисона – «панкреатическая холера»). Воздействуя на специфические рецепторы эпителия кишечника, ВИП активирует аденилатциклазу, повышает уровень цАМФ, что вызывает увеличение секреции воды и электролитов, вследствие чего развивается диарея. В сутки может теряяться более 3 л воды (иногда до 20 л).
Хроническая диарея может быть проявлением и других эндокринных опухолей. Например, при карциноме щитовидной железы диарея обусловлена повышенной секрецией кальцитонина.
Последствия. Гипогидратация организма, вплоть до эксикоза (крайняя степень гипогидратации организма). Гиповолемия, артериальная гипотензия, нарушения электролитного баланса (гипокалиемия, гипонатриемия) и КОС (метаболический ацидоз).
Запор (obstipatio) — длительная задержка стула или затруднение опорожнения кишечника (до 3 суток и более). В развитых странах запорами в той или иной степени страдают от 30-50% трудоспособного населения. У пожилых людей запор встречается в 5 раз чаще, чем у лиц молодого возраста.
Нормальным принято считать количество дефекаций от 3-х раз в сутки до 3-х раз в неделю. Для запора характерны малое количество кала, повышенная его твѐрдость и сухость, отсутствие чувства полного опорожнения кишечника после дефекации.
19
Основные виды и механизмы возникновения.
1.Алиментарный (малообъѐмный) – результат малого объѐма кишечного содержимого (например, при хроническом недоедании, малом потреблении жидкости, недостатке овощей и фруктов в пище – недостаток растительной клетчатки, употреблении легкоусвояемой пищи).
2.Нейрогенный (спастический и атонический запоры).
•Спастический запор – чрезмерное повышение вагусных нейрогенных влияний на стенку кишечника приводит к спазму еѐ мускулатуры. Это замедляет эвакуацию пищи и опорожнение кишечника.
•Атонический запор – снижение нейроэффекторных воздействий на мускулатуру кишечника вызывает его гипотонию и задержку стула.
3.Ректальный – следствие патологических процессов в прямой кишке, сопровождающихся болью (например, трещины, геморрой, парапроктит). Это подавляет рефлекс дефекации.
4.Механический – результат механической задержки эвакуации кишечного содержимого (например, опухолью, рубцом).
Кишечная аутоинтоксикация
Желудочно-кишечный тракт является естественной средой обитания микроорганизмов. Особенно богата микрофлорой толстая кишка. 90% микрофлоры толстой кишки – облигатные анаэробные бифидобактерии, в меньшем количестве содержаться молочнокислые бактерии, кишечные палочки, стрептококки.
Микрофлора кишечника вызывает в нѐм процессы брожения и гниения, но в норме они выражены нерезко. Образующиеся токсические вещества выводятся из организма или обезвреживаются, и интоксикации не наступает.
Этиология. Воспаление кишечника (энтериты, колиты), запоры, непроходимость кишок, дисбактериоз, голодание, гиповитаминозы, опухоли, применение лекарственных антибактериальных средств, аллергизация организма, лечение гормонами, ожоговая болезнь, лучевое воздействие, снижение иммунологической реактивности.
Патогенез синдрома кишечной аутоинтоксикации.
•Усиление гнилостных и бродильных процессов в кишечнике. Нарушается соотношение бактерий в различных отделах кишечника с усиленным размножением условно-патогенной и появлением патогенной флоры. Возникает вторичная энзимопатия, что приводит к усилению процессов брожения и гниения. Брожение сопровождается расщеплением углеводов с образованием кислот. Гнилостные процессы ведут к образованию из белков токсических веществ (скатола, индола, крезола, фенола).
•Недостаточность обезвреживающей функции печени при избытке поступления токсичных веществ по воротной вене.
•Недостаточное выведение токсичных веществ почками.
•Раздражение токсическими веществами хеморецепторов, механорецепторов кишечника, рецепторов сосудов головного мозга и внутренних органов.
Проявления. Токсические вещества, образующиеся в кишечнике (крезол, скатол, индол, фенол, гистамин, кадаверин, путресцин и др.) оказывают разнообразное влияние на органы и системы организма, начиная от желудочно-кишечного тракта до нервной и эндокринной систем регуляции.
Так, воздействуя на сосудистые рецепторы, кишечные токсины могут вызывать снижение АД, ослаблять работу сердца. Действуя на рецепторы ЦНС — понижать болевую чувствительность, угнетать дыхание, вызывать торможение нейронов коры головного мозга. Уменьшение запасов гликогена в печени и гипогликемия могут привести к коматозному состоянию. Проявляется кишечная аутоинтоксикация различными симптомами: головной болью, снижением аппетита, угнетением активности желез пищеварительного тракта, дистрофией миокарда, коматозным состоянием.
20
