
ДЗ 1 по физхимии вариант 258 / дз по физхимии №1 258вар
.docМосковский Государственный Университет Инженерной Экологии
Кафедра Общей и физической химии
Домашнее задание №1
Выполнил студент:
Максимчук Алексей
Группа М25
Преподаватель:
Мишустин А.И.
Москва 2007
1. Рассчитать константу скорости заданной реакции k1 при данной температуре Т1 по заданным энергии активации Е и предэкспоненциальному множителю k0.
2. Найти зависимость между временем t и текущей концентрацией C и построить кинетическую кривую (график зависимости С от t); задать 6 - 10 равноотстоящих значений С (во всём диапазоне изменения С) и с помощью кинетического уравнения заданного порядка рассчитать соответствующие значения t.
3. Найти время полупревращения τ1/2 аналитическим путем (по соответствующей формуле) и графическим путем (по графикам №1 и №2). Определить относительную ошибку определения.
4. Рассчитать, сколько % от исходной концентрации С0 первого вещества (то есть написанного первым в уравнении реакции) (m1), и сколько кг этого вещества вступит в реакцию к заданному моменту времени t1 от начала опыта при заданной первоначально температуре T1 и заданном объеме V. Сколько кг продуктов образуется к этому времени? (Учесть, что в кинетические уравнения входит текущая, то есть остающаяся концентрация вещества.)
5. Найти температуру Т2, при которой за то же самое время t1 прореагирует m2% от С0. Объяснить, почему изменилась температура по сравнению с Т1.
6. Для первоначальной температуры Т1 построить график №2 зависимости от времени такой функции концентрации первого вещества, которая линейна относительно t. График должен быть построен во всем интервале концентраций. Из графика №2 определить графически константу скорости реакции k и время полупревращения τ1/2.
7. Рассчитать, во сколько раз возрастет скорость реакции при температуре Т1 вследствие применения катализатора, снижающего энергию активации Е на n%.
|
Реакция |
Порядок |
Т1,К |
k0 |
Е, Дж/моль |
C0 моль/л |
t1, с |
V, л |
m2, % |
n% |
|
CH3Br+J- => CH3I+Br- |
2 |
353 |
2.3*1010 |
76285 |
1 |
1800 |
450 |
19 |
22 |
-
Расчёт константы скорости реакции k1
k1=k0e-E/RT R=8.31 Дж / (моль* К)
k1=0.117
2. Построение графика С от t.
t=1/k1*(1/C - 1/C0) – зависимость С от t
|
С, моль/л |
t, с |
|
1 |
0 |
|
0.9 |
0.951 |
|
0.8 |
2.139 |
|
0.7 |
3.667 |
|
0.6 |
5.704 |
|
0.5 |
8.556 |
|
0.4 |
12.834 |
|
0.3 |
19.964 |
|
0.2 |
34.224 |
|
0.1 |
77.004 |
построим график зависимости С от t
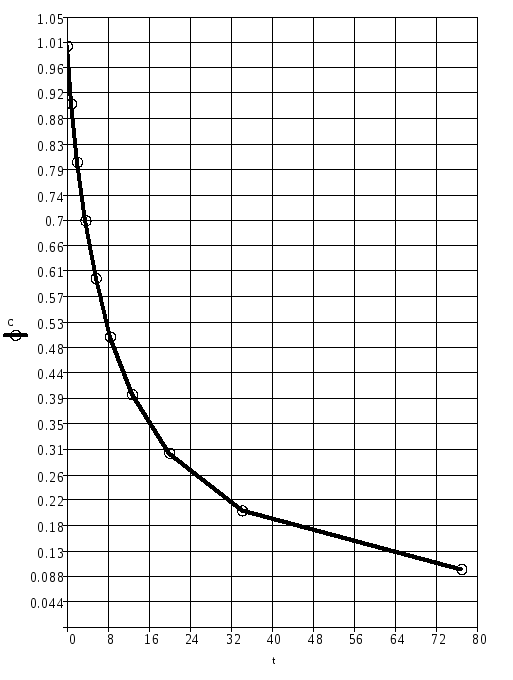 3.
Определим время полупревращения τ1/2
3.
Определим время полупревращения τ1/2
τ1/2ан =1/(k1*C0)
τ1/2ан= 8.556
τ1/2гр=8.547
ε(τ1/2)=((τ1/2ан - τ1/2гр)/ τ1/2ан ) *100%
ε(τ1/2)= 0,1 %
4. Расчёт массы прореагировавшего вещества.
1/Ст=1/C0+k1t
1/Cт= 4.731*10-3 моль/л – текущая концентрация вещества
Cпр=С0-1/Ст
Спр= 0,995 моль/л – концентрация прореагировавшего вещества
m1=Cпр/С0 *100%
m1= 99,527%
найдём массу продуктов реакции
M(CH3Br)=95 г/моль
mпр= Cпр*V* M
mпр= 4.255*104 г - масса продуктов реакции
5. Расчёт T2.
найдём концентрации Сх, которая составляет m2 от С0
Сх= C0* 19/100 %
Сх= 0.19 моль/л
найдём константу скорости k2 новой реакции
k2=1/t(1/Cx - 1/C0)
k2= 2,368*10-3
T2=- E/(ln(k2/ k0)*R)
T2= 306,976 К
Температура изменилась так, как изменилась константа скорости реакции, реакция идее медленнее.
6. Построение графика зависимости 1/С от t.
1/C = 1/C0 + k1 t 1/C=G ti=1/k1*(1/Ci - 1/C0)
|
1/С, моль/л |
t, с |
|
1 |
0 |
|
1.111 |
0.951 |
|
1.25 |
2.139 |
|
1.429 |
3.667 |
|
1.667 |
5.704 |
|
2 |
8.556 |
|
2.5 |
12.834 |
|
3.333 |
19.964 |
|
5 |
34.224 |
|
10 |
77.004 |
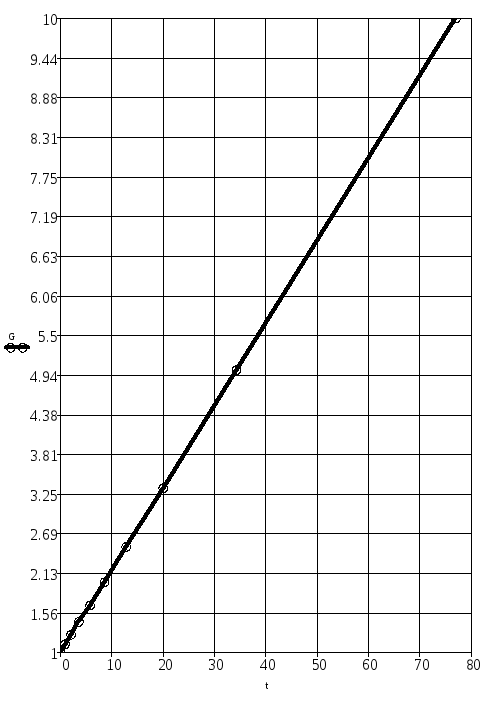
kгр=a/b
a=2.33
b=20
kгр=0.117
τ1/2гр=1/ kгр*C0
τ1/2гр= 8.584 c
8. Расчёт увеличения скорости реакции с применением катализатора.
Eкат=E*n/100 %
Eкат=1.678*104 Дж
ΔE=E-Eкат
ΔE=5.95*104
k3=k0*e-E/R*T1
k3=35.679
k3/k1=305.267
Скорость реакции возрастёт в 305.267раз.
|
Константа скорости |
Время полупревращения |
Расход первого вещества к моменту t1 |
к п.5 |
ускорение при катализе |
||
|
k1 |
графически |
аналитически |
m1, % |
кг |
T2 , K |
kкат/k1 |
|
0,117 |
8.547 |
8.556 |
99,527 |
42.55 |
306,976 |
305.267 |
