
ИЗУЧЕНИЕ ИМПЛАНТАЦИИ СЕТЧАТЫХ КОНСТРУКЦИЙ ИЗ НИКЕЛИДА ТИТАНА У КОШЕК И СОБАК
А.В.Чернов
ГУ «Клинический центр гастроэнтерологии». Проблемная лаборатория
ЮУНЦ РАМН, Центр ветеринарной медицины, г. Курган
Новые технологии хирургического лечения, связанные с применением имплантатов, продолжают интенсивно развиваться (1, 6, 12,). Этому способствует разработка новых имплантационных материалов, обладающих высокой биосовместимостью, и широкая, преимущественно гуманитарная, хирургическая практика их применения (3, 5, 10, 11). К таким материалам относится отечественные имплантаты последнего поколения из никелид титана (2, 4, 8, 9). Данный материал представляет собой интерметаллическое соединение никелида и титана (TiNi), обладает высокой коррозионной устойчивостью, биологической индифферентностью и по этим показателям превосходит медицинскую сталь (8, 9). Отдельные марки никелида титана при деформации обладают близким с живыми тканями свойством поведения (гистерезисом), что определяет биомеханическую совместимость материала (8). В зависимости от условий деформирования, в сплаве никелида титана наблюдается эффект обратимой памяти формы разного знака, весьма схожий по эластичности с живыми тканями (2, 9). По сравнению имплантатами из других материалов, тонкие и сверхтонкие сетчатые конструкции из никелида титана имеют сравнительно малую удельную площадь поверхности, что очень важно для имплантации любого инородного тела. Несомненным достоинством никелида титана перед другими распространенными полимерными имплантатами является простота хранения и стерилизации, которая может быть использована любым известным в настоящее время способом. Ценные свойства имплантационного материала находят применение в травматологии и ортопедии, сосудистой и абдоминальной хирургии и др. (8). Однако в ветеринарной медицине новые имплантационные материалы исследованы недостаточно.
Цель настоящей работы - изучить поведение сетчатых имплантационных конструкций из никелида титана в организме плотоядных животных и особенности формирования соединительной ткани в зоне имплантации.
Материалы и методы. Экспериментальную группу составили 26 беспородных собаки обоего пола в возрасте от 4 мес. до 9 лет. Моделировали крупные сквозные дефекты мышечно-апоневротического слоя в боковых отделах живота, в среднем 4 х 5 см, в которые имплантировали соответствующие по размеру сетки из никелида титана. Сетчатые конструкции изготавливали ручным способом из никелидтитановой проволоки марки ТН-10 калибром 60 и 90 мкм по типу рыболовной сети с ячеей 2-3 мм. Имплантацию выполняли с фиксацией сеток одноименным шовным материалом с расположением предбрюшинно sublay – кнутри от мышечно - апоневротического слоя. Брюшную стенку зашивали наглухо и зону имплантации не дренировали. В послеоперационном периоде проводили общеклиническое наблюдение и обследование, включая изучение морфологического и биохимического состава крови. Объективное исследование дополняли ультразвуковым сканированием (УЗИ) раны и зоны имплантации в сроки 7, 14, дней, 1, 3, 6 мес. Для этой цели использовали ультразвуковой сканер « Mysono -201» фирмы Medison (США) c широкополосным датчиком мощностью до 5,6 МГц. Кроме того, в сроки 14 дней, 1, 3, 6 мес. и 1 год проводили ножевую биопсию из зоны имплантации с последующим гистологическим и электронномикроскопическим исследованием биоптатов. Для изучения архитектоники формирующейся соединительной ткани использовалась сканирующая электронная микроскопия (СЭМ) электронным микроскопом GEOL – JSM 840 Scanning microscope фирмы Эйко (Япония). Параллельно с ножевой биопсией производили бактериологический контроль раневого содержимого и биоптатов. Наибольшая продолжительность наблюдения за экспериментальными животными составила 5 лет.
Клинические исследования представляли собой применение сетчатых имплантатов из никелида титана в реальной ветеринарной практике для ликвидации грыж и других дефектов мышечно-апоневротического слоя брюшной стенки у мелких домашних животных кошек (9) и собак (32). Общее число операций пластики дефектов брюшной стенки у животных – 34 с отдаленными результатами от 6 мес. до 5 лет.
Результаты исследований. Ближайший послеоперационный период по своему характеру соответствовал реакции на имплантацию биосовместимого инородного тела без признаков гнойного воспаления. Отмечены лишь отдельные случаи уплотнений в зоне дефекта и армированной имплантатом соединительной ткани. Ни в одном случае не отмечено образование грыж, сером, свищей и других характерных осложнений имплантации. Сравнение гематологических показателей на 14 день после имплантации с исходными подтверждает физико-химическую индифферентность имплантационного материала и отражает неспецифическую реакцию организма животного на операционную травму и имплантацию инородного тела. УЗИ – исследование ран и брюшной стенки в зоне имплантации свидетельствует о том, что в зоне имплантации в первые две недели наблюдается отек тканей, свойственный имплантации инородного тела. В последующий период времени, в среднем на 3-ей неделе экспериментальной имплантации отек тканей уменьшается, ткани уплотняются в зоне формирования соединительной ткани, и имплантат выделяется по своей оптической плотности на фоне окружающих тканей (рис.1). УЗИ – исследование подтверждает неосложненный характер поведения имплантата из никелида титана. Следует отметить, что рентгенологический контроль за тонкими сетчатыми конструкциями оказался недостаточно информативным из-за эффекта рассеивания при стандартных режимах работы обычных рентгеновских аппаратов.
Бактериологические исследования биоптатов на 14 сутки и через 1 мес. после имплантации свидетельствовали о практически полной стерильности в зоне имплантата и новообразованной соединительной ткани.
В ходе УЗИ - контроля и ножевой биопсии зоны имплантации никелида титана был обнаружен эффект контракции соединительной ткани, армированной сетчатым имплантатом. Данный эффект представляет собой сокращение вновь образованной соединительной ткани (контракция минус), который вызывает в ранние сроки (до 3 мес.) после имплантации сокращение площади ткани, армированной никелидом титана. В более поздние сроки (6 мес. и более) на отдельных участках имплантации может происходить расширение площади армированной сформированной соединительной ткани (контракция плюс). В целом эффект контракции и «эволюция» формы вновь образованной соединительной ткани связаны с действием сил натяжения – растяжения, действующих на участке имплантации (7). Биомеханическая совместимость и сверхэластичность материала из никелида титана позволяет следовать за изменениями архитектоники соединительной ткани на таких участках.
Макроскопически в ходе биопсии сетчатые имплантаты из никелида титана скрыты в толще вновь образованной соединительной ткани. Толщина комплекса имплантат - соединительная ткань достигает 3 – 5 мм и при биопсии режется с трудом.
Морфологические исследования с применением стандартной окраски гематоксилином и эозином, а также пирофуксином по Ван-Гизону срезов фиксированных биоптатов в указанные выше сроки подтверждают неосложненный характер «приживления» имплантатов из никелида титана. Умеренная воспалительно-клеточная инфильтрация, характерная для имплантации инородного тела, не носит характера деструктивного и тем более гнойного воспаления, отсутствует позднее 2-3 недель эксперимента как вокруг нитей, так и в отдалении. Коллагеновые волокна тонкие, тесно прилежат друг к другу, определяется их циркулярная ориентация по отношению к нитям имплантата Формирование зрелой волокнистой соединительной ткани завершается к 1 месяцу эксперимента, и в дальнейшем гистологическая картина сохраняет свою стабильность. Отмечается подчеркнутая ориентация коллагеновых волокон концентрически вокруг нитей имплантата. Перифокально гистологическая картина соответствует структуре зрелой соединительной ткани с трехмерно расположенными грубыми коллагеновыми волокнами, толстостенными сосудами с включениями жировой ткани. Воспалительно-клеточная инфильтрация отсутствует. В сроки 6 мес. и более соединительная ткань ровная, гладкая, блестящая. На отдельных участках сквозь соединительную ткань просвечивают элементы проволочной сетки. При разрезе имплантата рубцовая соединительная ткань прочно фиксирована к проволочным нитям. Форма имплантата не повторяет исходную, площадь поверхности армированной соединительной ткани изменена на отдельных участках имплантации как в сторону уменьшения, так и увеличения. Гистологическая картина демонстрирует завершенный гистогенез с ориентацией соединительнотканных волокон вокруг нитей имплантата (рис. 2). Сформированная соединительная ткань плотная, перифокального отека нет. Периферические участки соединительной ткани без признаков отека с включениями мышечной ткани.
Сканирующая электронная микроскопия имплантатов и новообразованной соединительной ткани дает объяснение прочной фиксации имплантата в соединительной ткани: шероховатый микрорельеф поверхности имплантата (рис. 3) благоприятствует четко ориентированному росту соединительной ткани непосредственно от поверхности имплантата без образования крупных грануляционных капсул, как при пленчатых имплантатах. Прочная фиксация ткани на имплантате исключает его свободную подвижность. Остов соединительной ткани, образованной вокруг имплантата, имеет волоконно-фибриллярный тип строения. Наблюдается прочная фиксация фибробластов и коллагеновых волокон к отдельным элементам имплантата. «Обрастание» элементов нитей имплантата достигает по толщине и превосходит калибр самой нити (рис. 4). Промежутки между коллагеновыми волокнами незначительны, что характерно для плотной соединительной ткани. Отмечается упорядоченное фибриллярное строение цилиндрических коллагеновых волокон. Коллагеновые волокна, образующие пучки, спиралевидно изогнуты, что придает соединительной ткани дополнительную прочность. Специфическая конформация спиральных коллагеновых волокон поддерживается системой тонких коллагеновых волоконец, оплетающих циркулярно нити имплантата и вплетенных в более толстые коллагеновые волокна, расположенные между ними.
В ветеринарной клинике выполнено 34 операции у кошек и собак с имплантацией сетки из никелида титана в область дефекта брюшной стенки сравнительно крупных размеров врожденного или приобретенного характера. Среди них: послеоперационные и рецидивные грыжи - 10, врожденные дефекты средней линии живота и пупка - 7, травматические дефекты брюшной стенки, в том числе проляпсусы - 5, грыжи промежности - 2, послеоперационные и посттравматические эвентрации, осложненные гнойной инфекцией - 8. Варианты расположения сетчатых имплантатов из никелида титана в брюшной стенке: onlay – кнаружи то мышечно-апоневротического слоя (13), inlay – в пределах границы грыжевого дефекта (2), sublay – предбрюшинно (11) и комбинированный способ, в котором сочетается традиционное ушивание дефекта лигатурами с укреплением апоневроза имплантатом (8).
Непосредственные результаты операций показали высокую надежность закрытия дефектов брюшной стенки, в том числе в условиях инфицированной раны, когда другие имплантаты и методы ушивания дефекта были неэффективны. Практически во всех случаях достигнут непосредственный положительный результат и ликвидация дефекта брюшной стенки. В отдаленном периоде до 5 лет признаков отторжения, инфицирования имплантатов из никелида титана не отмечено. Отсутствие рецидивов грыж и других дефектов брюшной стенки подтверждают полноценность и надежность армированной сетчатым имплантатом TiNi новообразованной соединительной ткани.
Заключение. Имплантация тонких сетчатых конструкций из никелида титана в организм плотоядных животных приводит к формированию полноценной соединительной ткани и ликвидации мышечно - апоневротического дефекта брюшной стенки. Характер формирования соединительной ткани в зоне имплантации отличается прочной фиксацией коллагеновых волокон на материале имплантата и биомеханической совместимостью с имплантатом, что повышает надежность армированной новообразованной ткани. Отсутствие пролонгированной воспалительной реакции в зоне имплантации и отсутствие других осложнений в отдаленном периоде свидетельствует о высокой биосовместимости никелида титана как имплантационного материала.
Чернов Александр Владимирович
ГУ «Клинический центр гастроэнтерологии», Проблемная лаборатория Южно-Уральского научного центра РАМН
Заведующий экспериментальной лаборатории
640000, Г. Курган, ул. Томина, 63.
тт. ( 352- 2) 46-38-88, (352-2) 53-23-28
Реферат
В работе представлены экспериментальные и клинические исследования по изучению использования отечественного имплантата из никелида титана для хирургического лечения грыж и других дефектов брюшной стенки у плотоядных животных. Методами клинического, лабораторного, ультразвукового, гистологического и ультраструктурного исследования показано, что при имплантации тонкой и сверхтонкой сетчатой конструкции
в зоне имплантации формируется полноценная соединительная ткань без признаков пролонгированного воспаления и отторжения имплантационного материала. Клиническая апробация имплантатов из TiNi, проведенная на плотоядных животных (кошки и собаки), ближайшие и отдаленные до 5 лет результаты подтверждает универсальность и высокую надежность разработанного метода хирургического лечения.
Литература
-
Белоконев В.И. и др. //Актуальные вопросы герниологии. – М., 2002.
-
Гюнтер В.Э. // II международный конгресс. Имплантаты с памятью формы. – Новокузнецк. – 1993. 5.
-
Зотов А.В. Хирургическое лечение грыж брюшной стенки: Автореферат дисс…докт. мед. наук.- Новосибирск. – 2000.
-
Зотов А.В. // Shape memory biomaterials and implants. Proceedings of international conference. – Tomsk. – 2001. 228.
-
Магда И.И., Воронин И.И., Бут И.Ф. // Ветеринария.- 1964.- №12. 43.
-
Малюга В.Г., Сильченко В.В. // Синтетические полимеры медицинского назначения. – Дзержинск, 1979.
-
Серов В.В., Шехтер А.В. // Соединительная ткань. – М.: Медицина, 1981.
-
Сплавы с памятью формы в медицине. / под ред. В.Э.Гюнтера и др. – Томск, 1986.
-
Шмерлинг М.А. и др. // Эффект памяти формы в сплавах. М.: Металлургия, 1974.
-
Batter et al. // Sinai J. Med. - 1999. – V.66. 20.
-
Klinge U. et al. // J. Biomed. Mater. Res. – 2002. – V. 63(6). 765.
-
Klosterhalphen B. et al. // Biomaterials. – 1998. – Dec. 19(24). 2235.
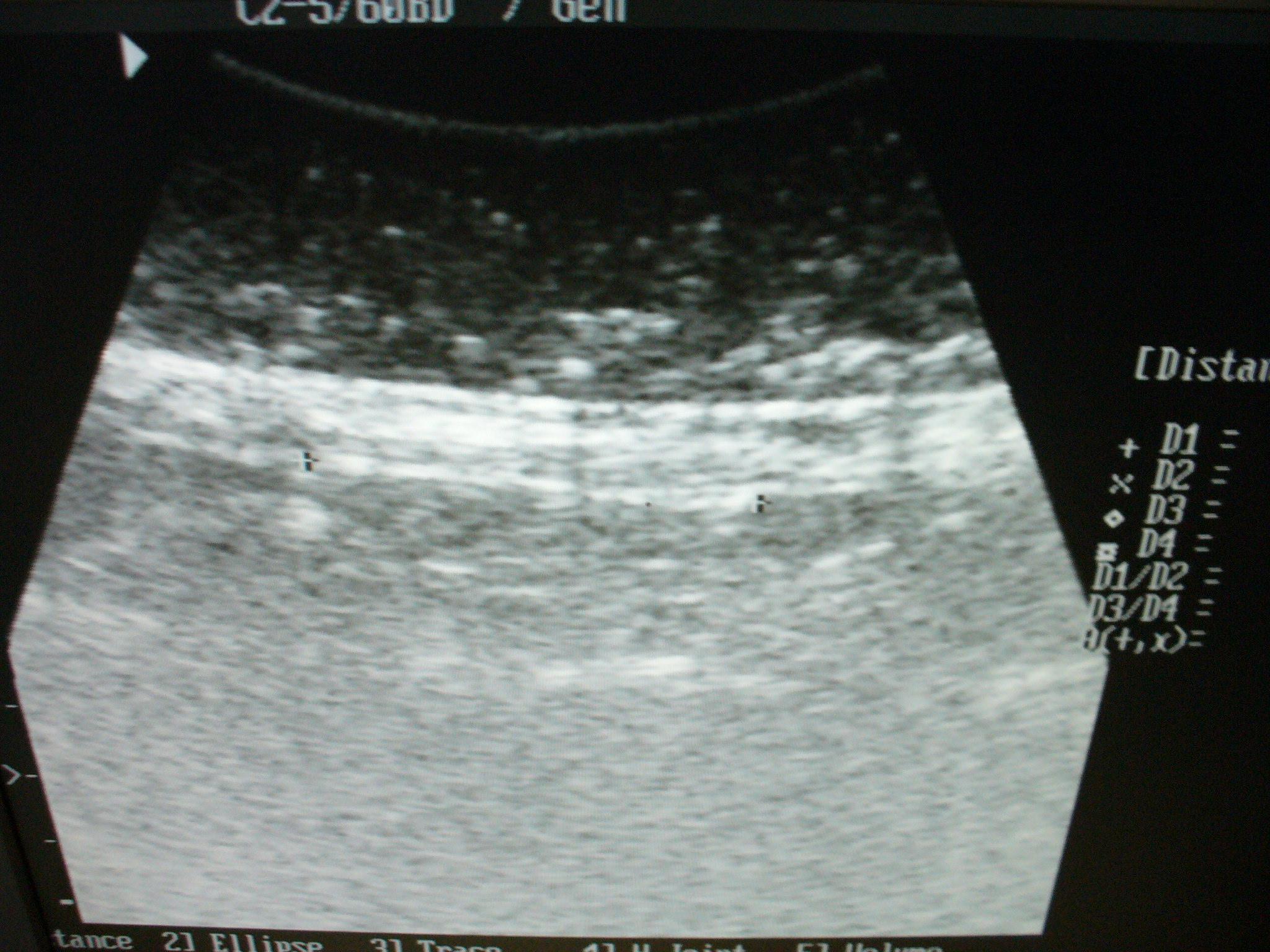
Рисунок 1 – Ультразвуковое сканирование имплантата из никелида титана (1 мес)
Диск Папка Эксперимент 027
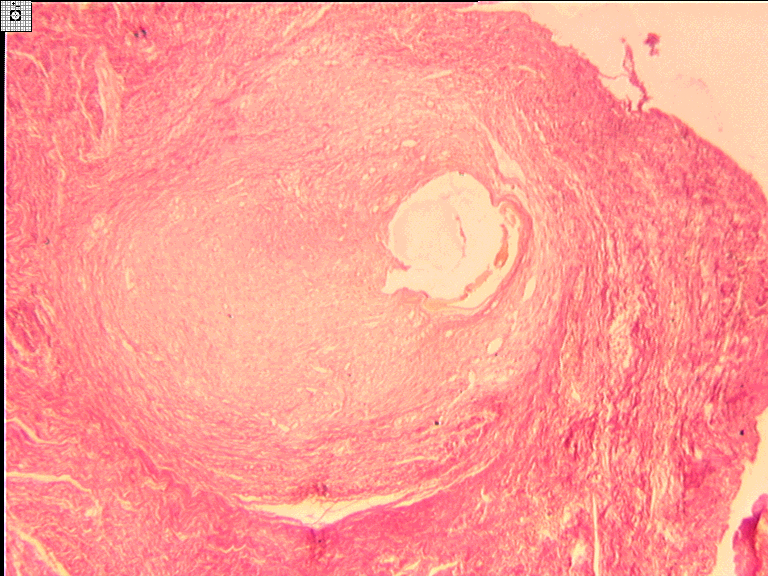
Рисунок 2 - Гистологическая картина сформированной соединительной ткани в зоне имплантации сетки из никелида титана (6 мес.)
Папка Желудок -01-гистол-30s- 6491-01

Рисунок 3 – Микрорельеф поверхности имплантата никелида титана марки ТН -10.

Рисунок 4 - Сканирующая электронная микроскопия новообразованной соединительной ткани, армированной имплантатом из никелида титана (3 мес.)
Папка Желудок 1. Серый 1

Рисунок 5 - Сканирующая электронная микроскопия новообразованной соединительной ткани, армированной имплантатом из никелида титана (3мес.)
Папка Желудок 1. 1-9
ПОДРИСУНОЧНЫЕ ПОДПИСИ
Рисунок 1 – Ультразвуковое сканирование имплантата из никелида титана (1мес.)
Стрелками отмечено предбрюшинное расположение имплантата. Отека тканей брюшной стенки и скоплений тканевой жидкости нет.
Рисунок 2 – Гистологическая картина сформированной соединительной ткани в зоне имплантации сетки из никелида титана (3 мес.). Окраска пирофуксином по Ван – Гизону. Объектив 2,5, окуляр 10.
Округлый дефект в препарате – место нахождения элемента имплантационной конструкции, вокруг которого слой циркулярно ориентированной зрелой соединительной ткани.
Рисунок 3 – Микрорельеф поверхности имплантационного материала – проволочной нити из никелида титана марки ТН-10. СЭГ. Увеличение 2000.
Шероховатая неровность имплантационного материала обеспечивает прочную фиксацию новообразованной соединительной ткани непосредственно к поверхности имплантационной конструкции.
Рисунок 4 - Пласт новообразованной соединительной ткани, армированной сетчатым имплантатом из никелида титана. (6 мес.). СЭГ. Увеличение 110.
Плотная фиксация соединительной ткани к материалу имплантата с циркулярной ориентацией элементов ткани к нитям имплантационной конструкции.
