
Формальдегид
.docx
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования
«МИРЭА – Российский технологический университет»
РТУ МИРЭА
|
|
Институт тонких химических технологий им. М.В. Ломоносова |
|
(наименование Института)
|
|
Кафедра общей химической технологии |
|
(наименование кафедры)
Получение формальдегида окислительным дегидрированием метанола
Вариант 4.
Работу выполнила
Студентка группы ХББО-02-16
Языкова Екатерина Игоревна
Руководитель работы
Кацман Евгений Александрович
Москва 2020
Экспериментальные данные:
Концентрация водного раствора метанола – 80 % масс.
Плотность водного раствора метанола при 20°C – 0,85 г/мл
Поданное в испаритель количество водного раствора метанола – 49 мл
Поданный за время опыта объём воздуха при условиях лаборатории – 43,2 л
Объём контактного газа, полученный за время опыта при условиях в лаборатории – 45,6 л
Температура в лаборатории – 20 °C
Барометрическое давление – 735 мм.рт.ст.
Объём катализатора – 3 мл
Доля свободного объёма – 0,6
Средняя температура в реакторе – 700 °C
Время опыта – 1 час
Количество формальдегида, полученного за время опыта – 25 г
Состав контактного газа
|
Наименование |
С, % объем. |
|
H2 |
18,9 |
|
O2+N2 |
75,4 |
|
CO |
2,2 |
|
CO2 |
3,5 |
Материальный баланс контактного аппарата для получения формальдегида
|
Приход |
Расход |
|||||||
|
Наименование |
л при н.у. |
г |
% масс. |
Наименование |
л при н.у. |
г |
% масс. |
|
|
MeOH |
- |
33,32 |
36,50 |
CH2O: |
- |
25,0 |
27,39 |
|
|
H2O |
- |
8,33 |
9,13 |
Окисл. |
- |
15,85 |
17,36 |
|
|
Воздух: |
38,93 |
49,62 |
54,37 |
Дегидрир. |
- |
9,15 |
10,03 |
|
|
O2 |
8,18 |
11,69 |
12,81 |
H2O: |
- |
20,15 |
22,08 |
|
|
N2 |
30,75 |
37,93 |
41,56 |
Реакц. |
- |
11,82 |
12,95 |
|
|
|
|
|
|
Введенная с MeOH |
- |
8,33 |
9,13 |
|
|
|
|
|
|
MeOH |
|
4,60 |
5,04 |
|
|
|
|
|
|
Газ: |
41,09 |
42,9 |
47,00 |
|
|
|
|
|
|
N2 |
30,75 |
37,93 |
41,56 |
|
|
|
|
|
|
CO |
0,90 |
1,13 |
1,24 |
|
|
|
|
|
|
CO2 |
1,44 |
2,82 |
3,09 |
|
|
|
|
|
|
O2 |
0,23 |
0,33 |
0,36 |
|
|
|
|
|
|
H2 |
7,77 |
0,69 |
0,75 |
|
|
|
|
|
|
Невязка |
- |
-1,38 |
-1,51 |
|
|
Всего |
- |
91,27 |
100 |
Всего |
- |
91,27 |
100 |
|
-
Пересчет поданного объёма воздуха и полученного объема контактного газа при л.у. на н.у.


-
Расчет прихода:
2.1. Метанол:
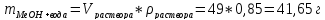

2.2. Вода:

2.3. Воздух:




-
Расчет расхода:
Реакции для расчетов:
CH3OH + 0,5O2 = CH2O + H2O (1)
CH3OH = CH2O + H2 (2)
CH3OH + 1,5O2 = CO2 + 2H2O (3)
CH2O = CO + H2 (4)
А) Расход газообразных продуктов:
3.1. Азот+кислород:
Поскольку азот является инертом в данном синтезе, то объем и масса азота на входе равна объему и массе на выходе.




3.2. Водород:


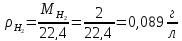
3.3. Углекислый газ:



3.4. Угарный газ:

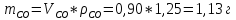

Б) Расход жидких продуктов:
3.5. Формальдегид, полученный дегидрированием:
Верхний индекс обозначает реакцию, по которой идет расчет.



3.6. Формальдегид, полученный окислением:

3.7. Реакционная вода:

3.8. Непрореагировавший метанол:

-
Коэффициент пересчета:

Для пересчета табл. мат. баланса на заданный базис, умножаем все значения масс и объемов на коэффициент пересчета.
Материальный баланс контактного аппарата для получения формальдегида, пересчитанный на базис 1 г формальдегида
|
Приход |
Расход |
|||||||
|
Наименование |
л при н.у. |
г |
% масс. |
Наименование |
л при н.у. |
г |
% масс. |
|
|
MeOH |
- |
1,33 |
36,50 |
CH2O: |
- |
1,00 |
27,39 |
|
|
H2O |
- |
0,33 |
9,13 |
Окисл. |
- |
0,63 |
17,36 |
|
|
Воздух: |
1,56 |
1,99 |
54,37 |
Дегидрир. |
- |
0,37 |
10,03 |
|
|
O2 |
0,33 |
0,47 |
12,81 |
H2O: |
- |
0,81 |
22,08 |
|
|
N2 |
1,23 |
1,52 |
41,56 |
Реакц. |
- |
0,48 |
12,95 |
|
|
|
|
|
|
Введенная с MeOH |
- |
0,33 |
9,13 |
|
|
|
|
|
|
MeOH |
- |
0,18 |
5,04 |
|
|
|
|
|
|
Газ: |
1,65 |
1,72 |
47,00 |
|
|
|
|
|
|
N2 |
1,23 |
1,52 |
41,56 |
|
|
|
|
|
|
CO |
0,04 |
0,05 |
1,24 |
|
|
|
|
|
|
CO2 |
0,06 |
0,11 |
3,09 |
|
|
|
|
|
|
O2 |
0,01 |
0,01 |
0,36 |
|
|
|
|
|
|
H2 |
0,31 |
0,03 |
0,75 |
|
|
|
|
|
|
Невязка |
|
-0,06 |
-1,51 |
|
|
Всего |
- |
3,65 |
100 |
Всего |
|
3,65 |
100 |
|
Расчет основных показателей процесса
-
Полученное при проведении опыта соотношение O2 : MeOH


Соотношение O2 : MeOH = 0,35:1
-
Время контактирования


Vк – объем катализатора
Ε – доля свободного объема катализатора
Vt,p – расход исходных веществ, проходящих через катализатор при условиях процесса


P=735 мм рт. ст.=0,967 атм
T=273,16+700=973,16 К







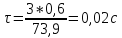
-
Степень превращения метанола
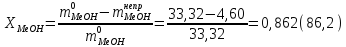
-
Выход формальдегида

-
Селективность образования формальдегида

-
Расходные коэффициенты по метанолу
-
Практический
-

-
Стехиометрчиеский

-
Интенсивность работы катализатора

где I – интенсивность работы катализатора
П – масса, полученного за единицу времени, целевого продукта
Vк – объем катализатора



