
- •1. Вступительная лекция к курсу факультетской педиатрии........ 5
- •28 Марта 1963 г.
- •I. Вступительная лекция к курсу факультетской педиатрии
- •2. Лекция о простой диспепсии
- •2 М. С. Маслов 33.
- •I стадия
- •II стадия
- •1. Сцеженное грудное молоко по 10 мл 10 раз и морковная смесь но 20 мл 5—б раз в сутки
- •4. Лекция о колите
- •I степени
- •II степени
- •III степени
- •6. Вторая лекция о дистрофиях
- •6 Атаманы Альоомицин * //
- •7. Лекция об анемиях
- •8. Лекция о лейкозах
- •9. Первая лекция о врожденных пороках сердца
- •1 В настоящее время принято считать, что сброс крови слева направо происходит не только при систоле, но и во время диастолы.
- •2 В последнее время проведение обычной ангиокардиографии при незаращенин боталлова протока считается нецелесообразным; лучше — зондирование и селективная ангиокардиография.
- •1 Без особой надобности к аортографии, являющейся опасным методом исследования, прибегать не следует,
- •10. Вторая лекция о врожденных пороках сердца
- •11. Лекция о ревматическом пороке сердца
- •12. Лекция о декомпенсации сердечной деятельности
- •13. Лекция о катаральной пневмонии
- •6 М. С. Маслов 161
- •1 В настоящее
- •14. Лекция о лобарной пневмонии
- •15. Лекция о хронической пневмонии
- •7 М, с. Маслов
- •16. Лекция о плевритах
- •17. Лекция об эпидемическом гепатите
- •18. Лекция о холецистите
7. Лекция об анемиях
Саша 3., 10 месяцев, поступил в клинику 12/XI 1955 г. с жалобами матери на бледность кожных покровов у ребенка. При оформлении ребенка в ясли врач обратил на это внимание и попросил сделать анализ крови. У ребенка было обнаружено 35% гемоглобина. Врач направил ребенка в клинику. Мать этому не придавала большого значения, так как, по ее словам, ребенок был всегда бледным.
Ребенок происходит от молодых родителей. Матери всего 22 года, она работает технологом. Страдает туберкулезом шейных желез. Отец с семьей не живет. Ребенок живет в комнате площадью 18 м2, теплой, но сырой и темной, имеет отдельную кроватку, обеспечен бельем, игрушками, летом гулял много, с осени — редко и не каждый день. Находится на попечении бабушки.
Ребенок от первой беременности, родился недоношенным, на 7-м месяце беременности, с весом 1770 г, закричал сразу. Грудь взял только с 15-го дня и сосал вяло. Он долго находился в отделении недоносков, где перенес пневмонию. На грудном вскармливании находился до 4 месяцев, а затем из-за малого количества молока у матери был переведен на искусственное питание, стал получать смесь № 3 по 200 мл 5 раз. С б месяцев стал получать манную кашу. Количество пищи мать строго не учитывала, давая ребенку пить молока, сколько он хочет. Иногда ребенок выпивал до 250 мл молока за раз. С 7—8 месяцев ребенку стали давать кисели, яблочное пюре, яичный желток.
Ребенок поступил в клинику в удовлетворительном состоянии, с весом 8800 г, ростом 73 см, т. е. нормальным для его возраста. Индекс Чулицкой у него был 14. При осмотре бросалось в глаза наличие очень бледных кожных покровов и слизистых оболочек, небольших трещин у углов рта. Подкожный жировой слой выражен хорошо. На шее прощупываются лимфатические узлы величиной до горошины. Головка несколько увеличена с выпячиванием лобных бугров, большой родничок еще открыт на 2X2 см. На грудной клетке определяются рахитические четки.
Границы сердца определяются: верхняя — на II ребре, левая — по наружному краю ареолы, правая — несколько кнаружи от правой гру-динной линии. Тоны сердца отчетливые, но I тон у верхушки нечистый. Акцента на легочной артерии не определяется. Перкуторный звук над легкими ясный, дыхание пуэрильное, без хрипов. Живот мягкий, прощупывается край печени и селезенки. Ребенок сидит, хорошо опирается на ножки. Произносит хорошо слоги. Дермографизм красный, скрытый период— 10 сек, длительность явного — 7 мин. Проба на адреналин более быстрая и более яркая, чем на гистамин. Моча в пределах нормы. Стул нормальный при осмотре глазом и при капрологическом исследовании.
Анализ крови: эр. 3 860 000, НЬ 35%, цветовой показатель — 0,44, л. 13 500; н. 25%, лимф. 69%, мон. 3%, э. 1%, плазматических клеток — 2%; РОЭ — 46 мм в час. Обнаружен выраженный анизоцитоз, пойкило-цитоз, умеренный ретикулез (2%о). Са в крови— 13,8 мг%, Р — 2,8 мг%.
При рентгенографии органы грудной клетки в пределах нормы. Реакция Пирке отрицательная.
В данном случае диагноз поставить легко. Ведущим симптомом является выраженная бледность кожных покровов и слизистых оболочек. Объективное исследование обнаружило наличие рахита и отсутствие изменений во внутренних органах и подтвердило анемию гипохромного типа у ребенка нормально развитого, с нормальным весом и ростом. Причины развития анемии также ясны. Ребенок родился недоношенным, а, как известно, почти у всех недоношенных детей анемия выявляется уже в первые недели и месяцы. Дальше, ребенок рано был переведен на искусственное вскармливание и уже на 4-м месяце получал около 1 л молока и больше. Прикорм был введен с 6 месяцев, но в диете ребенка почти отсутствовали овощи. Известно, что длительное злоупотребление молоком также способствует развитию анемии. Таким образом, мы можем считать анемию у нашего ребенка конституционально-алиментарной этиологии.
Переходим к разбору заболевания второго ребенка.
Галина К-, 2 лет 7 месяцев, поступила в клинику 17/Х 1955 г. с жалобами матери на общее исхудание, резкую бледность и большой живот у ребенка.
Мать стала замечать увеличение живота еще в конце первого года, одновременно у девочки стала нарастать бледность лица и слизистых оболочек, ухудшался аппетит. Врачи находили у девочки наличие рахита, и большой живот расценивался как одно из проявлений последнего.
Живот прогрессивно увеличивался на 2 и 3-м году жизни. Анализ крови доказывал наличие анемии.
Ребенок наш от первой беременности, родился весом 3100 г, получал грудь матери до 1 года 2 месяцев. Прикррм был введен в 6 месяцев. Соки стал получать только после года. После 6 месяцев получал ежедневно около 1 л молока. Семья живет в плохих бытовых условиях, малокультурная, девочка мало бывала на свежем воздухе.
Девочка с первого года жизни отставала в физическом развитии, плохо прибавляла в весе, и в 2 года весила 10 кг. Зубы прорезались с 9 месяцев. Ходить начала только в l'/г года. Психически развивается нормально.
Из ее заболеваний можно отметить наличие рахита, частых простудных заболеваний и коклюша в 12 месяцев, протекавшего тяжело и осложнившегося пневмонией.
Девочка поступила в удовлетворительном состоянии, но с резко пониженным питанием и весом 11 кг. Рост ее был — 83,5 см, окружность головы — 46 см, груди — 52 см, голени— 18 см, плеча — 13 см, бедра — 26 см. Индекс Чулицкой — 0,5, Эрисмана—10,5, Бедузи — 67.
Кожа резко бледная, сухая, подкожный жир слабо выражен, тургор кожи и мышц дряблый. Слизистые оболочки бледные. Увеличены миндалины. Прощупываются мелкие, плотные, безболезненные шейные, подмышечные, паховые лимфатические узлы. Суставы разболтанные. Грудная клетка слегка деформирована, прощупываются четки на ребрах и утолщения в запястьях.
Перкуссия легких дает нормальный, ясный звук; аускультация — наличие пуэрильного дыхания. Границы сердца в пределах возрастной 76
нормы. У верхушки прослушивается систолический шум; акцентов на основании сердца нет.
Живот резко увеличен, его окружность равняется 58,5 см, напряжен. Прощупывается край печени на 6 см ниже реберной дуги. В левой половине живота определяется громадная плотная селезенка, спускающаяся в малый таз. Жидкости в животе нет.
Дермографизм розовый, длящийся Р/2 мин. Патологических рефлексов нет.
Моча в пределах нормы. Копрограмма также без уклонений от нормы..Реакции Пирке и Манту отрицательные. Реакции Вассермана и Кона также отрицательные. Анализ крови: эр. 2 590 000, НЬ 44%, цветовой показатель 0,88, л. 25 200, н. 69%, с. 26%, п. 15%, юных — 10%, миелоцитов—10%, промиелоцитов — 8%., лимф. 26%, мон. 4%, э. 1%. тромбоцитов 95 300, анизоцитоз 4-4-4-, пойкилоцитоз 4-4-+, полихро-мазия 4-4-, наличие макроцитов и 30°/оо ретикулоцитов, единичные нор-мобласты. Длительность кровотечения 2 мин 30 сек, свертываемость по Бюркнеру 4 мин 35 сек — 5 мин 27 сек, осмотическая стойкость 0,50— 0,42% NaCl. Биохимическое исследование крови показало наличие 10,2 мг% Са, 1,7 мг% Р, протеинов крови 8,2%, из них альбуминов 4%, глобулинов 4,2% (альфа-глобулинов 1,13%, бета-глобулинов 1,52% и гамма-глобулинов 1,55%).
Анализ данных анамнеза, объективного исследования и данных лабораторного анализа позволяет поставить диагноз анемии, но уже в тяжелой форме. У этого ребенка по сравнению с вышеразобранной формой отмечается не только большая выраженность изменений в периферической крови, но и наличие резко увеличенной селезенки, высокого лейкоцитоза и измененной лейкоцитарной формулы со сдвигом в сторону нейтрофилеза и молодых форм (миелоцитов и промиелоцитов). Эта анемия выявлена на фоне резкого истощения ребенка и симптомов рахита, которые были подтверждены объективными лабораторными данными (снижение содержания Р в крови). Эта форма анемии называется селезеночной, или псевдолейкемической, или по фамилиям авторов, впервые ее описавших, — анемией Якш — Гайема. От истинной лейкемии она отличается более доброкачественным течением, отсутствием в периферической крови миелобластов, увеличенных лимфатических узлов и болезненности в костях, наличием регенеративных элементов со стороны эритропоэза (макроцитоз, ретикулоцитоз). Картина крови нашей девочки несколько отличается от типичной, при которой чаще бывает повышенное содержание лимфоцитов и моноцитов, небольшое содержание нейтрофилов с наличием молодых и незрелых форм (миелоцитов). Сочетание же с рахитом и дистрофией является характерным для всех форм анемии Якш — Гайема. Что касается этиологии данного заболевания у нашей больной, то она выявляется из анамнеза. Главными причинами являются, по-видимому, злоупотребление в питании цельным молоком во втором полугодии жизни, плохие бытовые условия, отсутствие прогулок на воздухе. Но анемии со спленомегалией и лейкоцитозом можно объяснить только наличием и своеобразной реактивности, поскольку у других детей эти же факторы обусловливают развитие простой анемии. Некоторую роль играет и рахит, и связанное с ним нарушение кровоснабжения в костном мозгу. Но еще более вероятно нарушение нервно-регуляторных механизмов.
Работами В. Н. Черниговского, А. Я. Ярошевского и другими доказано, что костный мозг снабжен рецепторами, реагирующими на химические раздражители. Равным образом насыщены рецепторами и все другие органы, принимающие участие в регуляции и распределении
форменных элементов. Ядра промежуточного мозга и подкорковых узлов являются центрами безусловных кровераспределительных рефлексов. Разрушение нервных связей этих органов с центральной нервной системой ведет к нарушению деятельности всей системы крови. В деле регуляции кровотворения большое значение имеет функциональное состояние коры головного мозга. В опытах со столкновением пищевого и оборонительного рефлексов, приводящих к срыву высшей нервной деятельности, можно наблюдать значительные изменения в составе крови и костного мозга. Кортикальная регуляция может менять состав крови и путем перераспределения крови из депо в общую систему.
Вполне понятно, что у детей раннего возраста, у которых кора головного мозга еще функционально не вполне совершенна, нервно-регуляторные механизмы действуют менее точно, легче наступают и расстройства кровотворения и притом в более своеобразных формах, чем у детей старшего Еозраста.
В частности, анемию Якш — Гайема надо рассматривать не как отдельную нозологическую форму, а лишь как крайний вариант гипо-хромной анемии. Встречаются ее легкие, средние и тяжелые формы. Легкая форма анемии Якш — Гайема вызывается алиментарным фактором при наличии желудочно-кишечных расстройств, и при ней еще нет выраженного лейкоцитоза, нет и значительного нормобластоза, но имеются увеличение селезенки и упадок питания. Средней тяжести формы чаще развиваются в результате воздействия повторных инфекций и уже сопровождаются лейкоцитозом, лимфоцитозом, нормобластозом, ретикулоцитозом и появлением миелоцитов. Роль желудочных желез, по новейшим данным, заключается лишь в том, что необходимые пищевые вещества (в частности, железо, витамин Bi2), будучи подвергнуты обработке секретами желудка (свободной соляной кислотой и гастро-мукопротеином), легко всасываются в тонких кишках. Таким образом, внутренний антианемический фактор Касля является в сущности гастро-мукопротеином. Внешний фактор отождествляется с белковым компонентом, содержащимся в печени, мясе и других продуктах. Возможно, что это одна из фракций комплекса витамина В12. Если желудочный сок лишен гастромукопротеина, то утрачивается способность связывать витамин В12 и последний не всасывается в кишечнике. Тяжелая форма дает уже геморрагии на коже, резкий лейкоцитоз, нейтрофилез со сдвигом влево, миелобластоз, резкий нормо- и мегалобластоз и увеличение селезенки и печени, что сближает ее с картиной лейкоза (Н. А. Кура-чова). Такие формы возникают при длительном воздействии отрицательных факторов при наличии измененной реактивности.
В происхождении той или иной формы анемии играет роль ряд факторов. Прежде всего индивидуальная реактивность детского организма и его органов, затем дефицит веществ, необходимых для процессов кровотворения, и, наконец, нарушения процесса кровообразования и кро-веразрушения и взаимодействия внешних и внутренних факторов, приводящих к образованию гемопоэтина.
Как надо себе представлять вредное влияние алиментарного фактора при так называемой алиментарной анемии? Прежние взгляды о дефиците железа, лежащего в основе патогенеза, не подтверждаются современными клиническими и экспериментальными исследованиями. Спорным и недоказанным является и роль трофотоксического фактора, т. е. вредного влияния токсических продуктов пищи. Больше основания предполагать наличие трофопенического фактора, т. е. недостатка в пище некоторых веществ, в частности полноценных аминокислот, необходимых для построения гемоглобиновой молекулы.
В свете новых данных можно предполагать, что известную роль в патогенезе алиментарной анемии играет отсутствие или явный недостаток в пище витаминов, в частности витаминов комплекса В, фолиевой кислоты и фактора Касля (внутреннего или внешнего). Недостаток железа в пище играет, по-видимому, вспомогательную роль. Исследования с радиоактивными изотопами железа показали, что в возрасте до 6 месяцев железо только в незначительной части идет на построение гемоглобина. Основная часть его содержится в гемоглобине крови, но значительная часть — в миоглобине, клеточных дыхательных ферментах и в печени в виде запасов (депо). При гипохромных анемиях обычно запасы железа в организме (в депо) имеются, но они не используются организмом для кровотворения. По-видимому, имеет место расстройство обмен-а железа наряду с другими нарушениями обменных процессов. Детали этого нарушения еще не выяснены, но можно предполагать, что оно зависит от нарушения деятельности регулирующего обмен железа нервнорефлекторного аппарата. За последнее время большое значение в патогенезе анемии начинают придавать отсутствию микроэлементов, т. е. минимального содержания меди, кобальта, магния.
Доказано, что у маленьких детей в норме содержится 92—202у% меди, при анемии содержание ее в крови повышено. Это повышение стоит, по-видимому, не в связи с насыщением организма медью, а в связи с нарушением обменных процессов, поскольку дача детям с анемией меди каким-то путем восстанавливает обмен и обусловливает нарастание числа эритроцитов. При этом, однако, не происходит одновременного увеличения гемоглобина. Последнее наступает только при одновременной даче и меди, и железа. В настоящее время установлено, что микродозы кобальта также приводят к усилению эритропоэза и даже к возрождению очагов экстрамедуллярного кровотворения. Известно, что кобальт является составной частью противоанемического витамина В12. У здоровых детей в крови содержится от 8 до 12у% кобальта, при анемии количество его снижается (Павлова). Интересно, что снижение кобальта и повышение меди часто бывает пропорциональным тяжести патологического процесса. Наименьшее содержание кобальта наблюдается у новорожденных (5у%). наибольшее — у детей первых 3 лет жизни (12у%) и снижение в старшем возрасте до 8—9у%. При алиментарных анемиях количество кобальта снижается до 3—5у% (Усов).
Микроэлементы входят в состав живых организмов как жизненно необходимая их часть. Они связаны с основными функциями: ростом, размножением, кровотворением. Принимая участие в ряде ферментативных процессов, действуя на активность гормонов, вступая в связь с витаминами, микроэлементы вовлекаются в обменные процессы. Известно, что цинк входит в состав угольной ангидразы, медь — в состав гемоцианазы, гемокупреина, гепатокупреина, ряда оксидаз, кобальт — в состав витамина BJ2, йод — в состав тироксина. Отдельные атомы микроэлементов, входящие в состав белковой молекулы, еще больше разнообразят свойства белковых соединений, создают физико-химическую основу способности органических молекул изменяться под влиянием внешних факторов. Кобальт способен увеличивать живой вес животных, синтез мышечных белков, ассимиляцию азота, утилизацию аминокислот. Это влияние кобальта на обмен веществ определяется связью его с деятельностью некоторых ферментов, особенно с тканевым дыханием и с дыхательной функцией крови. Медь — также биологически необходимый элемент, захват ее зародышем, значительное накопление в организме плода, увеличение количества в крови беременных указывает на важную ее роль для роста, развития и размножения. Участие
меди в процессах кровотворения и тканевого дыхания — одна из главных особенностей ее биологической активности.
Теперь попытаемся разобраться в патогенетической роли инфекционного фактора. Отличие гипохромной анемии инфекционного происхождения заключается в наличии более резких изменений в периферической крови, появлении незрелых форм эритроцитов, более выраженном лейкоцитозе и умеренном сдвиге нейтрофилов влево. В этих случаях речь идет о вредном воздействии на кровотворный аппарат эндо- и экзотоксинов, выделяемых микробами. Но не меньшую роль играет и своеобразие реактивности организма ребенка и присоединяющиеся вредные воздействия алиментарного фактора. Не всегда можно точно сказать, что является решающим, где кончается влияние одного фактора и начинается влияние другого. Всякая инфекция влияет на состояние вегетативной иннервации, изменяет состояние центральной нервной системы и реактивность организма (в том числе и кровотворного аппарата).
С другой стороны, при инфекциях всегда имеет место наличие однообразной и ограниченной диеты, понижение аппетита и секреторной функции желудка и кишок, а следовательно, возможно, и недостаточное всасывание и накопление токсических продуктов кишечного пищеварения. За большую роль реактивности организма говорит то, что анемии наиболее легко возникают и тяжело протекают у детей недоношенных и с резко выраженным упадком питания. При определенных условиях любая инфекция может быть причиной анемии, но чаще всего приходится иметь дело с анемией при пиуриях (пиелите, пиелоцистите), при сепсисах, ииодермиях, при врожденном сифилисе, малярии, лейшма-ниозе, менее отчетливо — при туберкулезе.
Токсические анемии встречаются главным образом при заражении Diphyllobotrium latum, Ankylostoma duodenale, реже — при Taenia, аскаридозе и острицах. В основе их лежит угнетающее действие на кроветворные органы токсических продуктов, выделяемых паразитами, и нарушение процессов всасывания, и в меньшей степени хронические потери крови, высасываемой паразитами из капилляров кишечника.
Апластическая анемия — далеко не редкая форма злокачественного малокровия у детей. Патогенез ее еще не вполне выяснен. Предполагают появление в крови какого-то вредного начала, которое повреждает регенерацию всех форменных элементов крови (т. е. панмиелофтиз). Другие считают, что в патогенезе ее играет решающую роль конституциональная неполноценность костного мозга, но с этим нельзя полностью согласиться. Скорее всего в основе ее лежит вредное воздействие ряда факторов среды, опосредованных через нервные регуляториые системы организма, приводящие к полному истощению функциональной способности костного мозга. Неполноценность же кровотворного аппарата является лишь предрасполагающим фактором.
Во многих случаях анемий играет вспомогательную, а иногда и решающую роль фактор врожденного предрасположения. Это особенно рельефно выявляется при так называемой анемии недоношенных детей. В основе патогенеза этих форм анемии лежит нарушение равновесия между процессами кровотворения и кроверазрушения. Неполноценность кровотворного аппарата у недоношенных детей проявляется уже в первые месяцы внеутробной жизни пониженной деятельностью гемопоэти-ческого аппарата при наличии нормального или даже слегка повышенного гемолиза. Она стоит в прямой зависимости от состояния нервно-рефлекторной регуляции кровотворения на соответствущем уровне развития коры головного мозга. За последние годы установлено наличие
F0
Плод Rh +
3
в крови двух видов гемоглобина, так называемого фетального и зрелого. У доношенных детей в крови наблюдается значительный процент фетального гемоглобина, который сохраняется почти до 3—4 лет, из чего можно заключить, что здоровые дети обладают способностью к его синтезу. У недоношенных детей уже в первые недели жизни наблюдается снижение содержания фетального гемоглобина, что указывает, по-видимому, на неспособность их к его синтезу. Только после 5—7 недель жизни у них начинает выравниваться состав красной крови. Исходя из этих данных, можно допустить, что анемия у недоношенных детей является даже не болезнью, а свойственной им физиологиче- » ской особенностью.
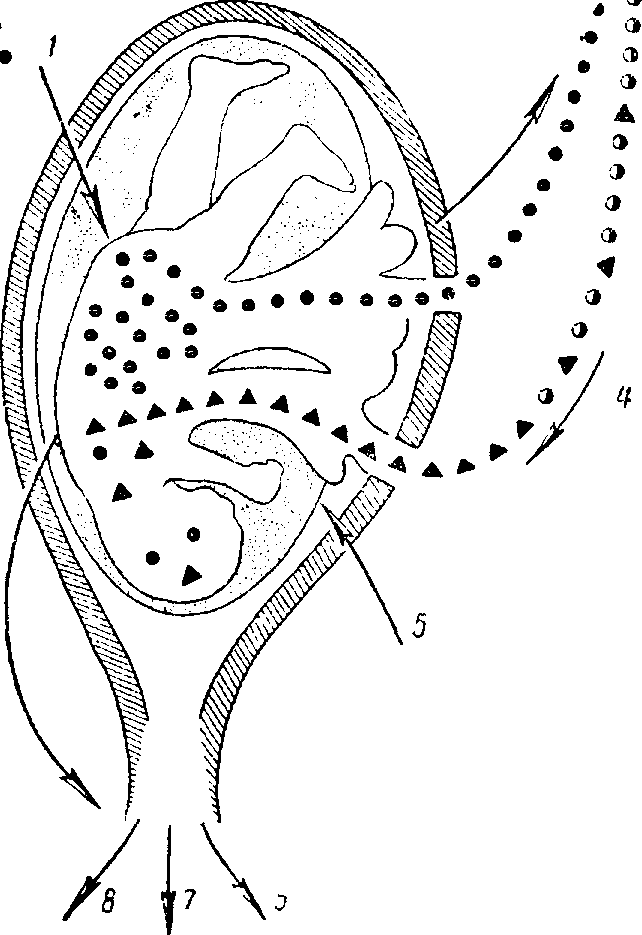
Одной из разновидностей врожденных анемий является врожденная гемолитическая анемия новорожденных, проявляющаяся у детей сразу с первых дней жизни то в виде тяжелой формы анемии с водянкой и желтухой, то в виде более легкой формы анемии без желтухи и отеков. Характерной особенностью этой анемии является часто отчетливо выраженный эритробластоз. В основе патогенеза этих форм лежит своеобразный гемолитический процесс, возникающий еще в период внутриутробной жизни вследствие несоответствия крови ребенка и матери. Если ребенок, как и его отец, имеет в крови особый антиген Rh (Rhesus-factor), а мать его не имеет, то этот антиген может переходить в кровь матери и вызывать в ней образование антител. Эти антитела, попадая через плаценту в кровь плода, вызывают у последнего реакцию агглютинации эритроцитов, что и ведет к гемолизу и развитию тяжелого малокровия. Очень важно отметить, что в таких случаях при первой беременности может родиться нормальный ребенок с легкой анемией, поскольку у матери еще не образовалось большого числа антител. При последующих же беременностях будут рождаться дети с тяжелой формой анемии с желтухой, водянкой и даже мертворожденные. Проведение такой матери внутривенных и внутримышечных введений крови с положительным резус-фактором также может повысить образование антител, тогда и первая беременность даст ребенка с тяжелой анемией. Отсюда является необходимым тщательное обследование беременных женщин на наличие или отсутствие у них резус-фактора. Прилагаемая схема (рис. 19) наглядно изображает развитие таких анемий.
Помимо резус-фактора, существуют и другие антигенные свойства фетальных эритроцитов, могущие привести к гемолитической болезни.
•Rh*
Э Rh-
Д, Rh-антатела
Рис. 19. Схема развития анемий при несовместимости крови в отношении резус-фактора.
/ — отец Rh-f-; 2 — мать Rh—; 3 — стимулируют образование антител; 4 — антитела через фетальное кровообращение попадают в кровь плода; 5 — гемо-лизируют эритроциты; 6 — hydrops foetalis; 7 — icterus gravis; 5 — анемия.
В первую очередь надо назвать АВО-систему. А- и В-антигены эритроцитов ребенка при наличии у матери группы O(I) могут возбудить наряду с повышением нормальных альфа- и бета-изоагглютининов также иммунные антитела неполного типа. Эта форма гемолитической болезни более благоприятна.
Другой формой врожденной анемии является гемолитическая анемия, характеризующаяся наличием желтухи без билирубинурии с резким понижением осмотической стойкости эритроцитов (до 0,7—0,3%), микроцигозом и увеличением селезенки.
В основе патогенеза этой формы лежит врожденное понижение осмотической стойкости эритроцитов и гиперфункция селезенки.
В нашем распоряжении еще пока не имеется клинических и экспериментальных данных о функциональном состоянии центральной нервной системы при различных формах анемии у детей и мы можем делать предположения на основании косвенных данных. Так, установлено, что при тяжелых формах анемии у детей всегда отчетливо выступают слегка выраженные вегетативные расстройства в виде склонности к появлению белого дермографизма, наклонности сосудов к спазмам, отрицательного глазо-сердечного и положительного ортостатического рефлексов, что позволяет предполагать наличие повышенной возбудимости симпатического отдела и пониженной — парасимпатического. Отмечается также некоторое угнетение безусловного и пилокарпинового слюноотделения, удлинение времени адаптации на боль и иногда пирамидные микросимптомы (И. И. Астахов). При легких анемиях наблюдаются только слабые проявления вегетативных расстройств.
Для того, чтобы вы смогли лучше ориентироваться в диагностике различных форм анемий и спленомегалий, предлагаю вашему вниманию табл. 13 и 14.
Из всего вышесказанного вытекает, что анемии у детей являются очень частым заболеванием и протекают разнообразно, в зависимости как от воздействия разных вредных факторов, так и от своеобразия реактивности детей (возрастной и индивидуальной). Прогноз при них также различен. При простых алиментарных и инфекционных формах анемии наблюдается быстрое улучшение, хороший прогноз. Там же, где имеется наличие конституционального фактора и измененной реактивности, заболевание труднее поддается лечению. Анемии Якш — Гайема обычно длятся многие месяцы и даже годы и только у части больных поддаются лечению обычными методами. Самый плохой прогноз — при апластических анемиях, выздоровление возможно только при наличии неполной аплазии костномозгового кровотворения. Большие успехи сделаны в лечении врожденных гемолитических анемий, вызванных несовместимостью резус-фактора.
Для выбора лечения анемии необходимо составить представление, в каком состоянии, раздражения или угнетения, находятся органы кровотворения и прежде всего костный мозг. Для этого можно воспользоваться пункцией грудины и исследованием пунктата костного мозга, но в большинстве случаев можно делать правильное заключение и по анализу периферической крови. Каждый практический врач должен уметь читать и расшифровывать лабораторные данные; не констатировать наличие тех или иных сдвигов в крови, а понять их смысл.
Наличие в периферической крови большого количества полихрома-тофилов и ретикулоцитов будет говорить о повышении регенерации в костном мозгу.
Умеренно выраженные полихроматофилез и ретикулоцитоз скорее благоприятный признак, а резко выраженные — свидетельствуют о пере-
Таблица
|
|
Анемия алиментарная |
Анемия инфекционная |
Анемия Якш—Гайема |
Анемия гемолитическая |
Анемия апластическая |
|
Окраска кожи |
Бледная |
Бледная |
Восковидно-бледная |
Слабо иктеричная |
Лимонно-желтая |
|
Геморрагии |
Не бывают |
Не бывают |
Изредка |
Не бывают |
Наблюдаются |
|
Слизистая рта |
Бледная |
Бледная |
Бледная |
Нормальная |
Иногда с мелкими кровоизлияниями |
|
Кишечные явления |
Не наблюдаются |
Не наблюдаются |
Диспепсия |
Не бывают |
Пониженная секреция сока |
|
Моча |
Норма |
Норма |
Норма |
Уробилин |
Норма |
|
Температура |
Нормальная |
Нормальная |
Нормальная |
Временами субфе-брильная |
Иногда высокая, скачкообразная |
|
Гемоглобин |
40—60% |
40—60% |
20— 40% |
30—60% |
10—25% |
|
Эритроциты |
2,5—3,5 млн. |
2,5- 3,5 млн. |
2—2,5 млн. |
2,5—4 млн. |
1—1,5 млн. |
|
Цветной показатель |
< 1 |
< 1 |
< 1 |
< 1 |
> 1 |
|
Лейкоциты |
Норма |
10—12 тыс. |
15—25 тыс. |
10—12 тыс. |
1—3 тыс. |
|
Лейкоцитарная формула |
Норма |
Небольшой нейтро-филез |
Лимфоцитоз, моноци-тоз, миелоцитоз |
Лимфоцитоз |
Лимфоцитоз, нейтро-пения, анэозинофи-лия |
|
Вид эритроцитов |
Анизоцитоз, пойкило-цитоз, ретикулез умеренный |
Анизоцитоз, пойкило-цитоз и умеренный ретикулез |
Анизо- и пойкилоци-тоз, много нормо-бластов и ретику-лоцитов |
Микроцитоз без пой-килоцитоза, много ретикулоцитов |
Слабый анизоцитоз, .иногда микроцитоз, нет регенеративных форм |
|
Тромбоциты |
Норма |
Норма |
Понижены |
Норма |
Меньше нормы |
|
Осмотическая стойкость |
Норма |
Норма |
0,50—0,38о/0 |
0,7—0,4% |
0,48—0,35о/0 |
|
Селезенка |
|
|
Увеличена |
Увеличена |
Слегка увеличена |
Дифференциально-диагностическая таблица анемий
Таблица
|
Симптомы |
Тромбофлеби-ческая |
Гемолитическая |
Болезнь Гоше |
Болезнь Банти |
Болезнь Нимана—Пика |
|
Анемия |
Не сильная |
Значительная |
Умеренная |
Умеренная |
Нерезкая |
|
Лейкоцитоз |
Лейкопе- |
Норма |
Лейкопения |
Лейкопе- |
10—30 тыс. |
|
|
ния или |
|
|
ния |
|
|
|
норма |
|
|
|
|
|
Селезенка |
Сильно |
Увеличена |
Значительно |
Громадная |
Громадная |
|
|
увеличена |
|
увеличена |
|
|
|
Печень |
Увеличена |
Незначительно |
Значительно |
Умеренно |
Громадная |
|
|
|
увеличена |
увеличена |
увеличена |
|
|
Окраска |
Бледная |
Слабо жел- |
Желтая с |
Желто- |
Желтовато- |
|
кожи |
|
тушная |
бронзовым |
грязного |
коричневая |
|
|
|
|
оттенком |
оттенка |
|
|
Другие |
Кровавые |
Уробилину- |
Типичные |
Уробили- |
Пенистые |
|
симптомы |
рвота и |
рия, умень- |
клетки в |
нурия, |
клетки в |
|
|
стул, тром- |
шение осмо- |
пунктате се- |
фиброаде- |
пунктате се- |
|
|
бопения |
тической |
лезенки, тром- |
ния се- |
лезенки, фи- |
|
|
|
стойкости |
бопения |
лезенки |
зическая |
|
|
|
эритроцитов |
|
|
отсталость |
раздражении, за которым может последовать истощение кровотворения. Тогда наступит и резкое снижение или даже исчезновение полихромато-филов и ретикулоцитов. Наличие макроцитов говорит о сохранившейся регенераторной способности костного мозга, наоборот, микроцитоз свидетельствует о некоторой неполноценности эритропоэза, о регенерации, идущей ненормально быстрым темпом (при гемолитической анемии).
Появление мегалоцитов указывает уже на патологический эмбриональный тип кровотворения.
Появление нормобластов у детей грудного возраста — явление физиологическое, свидетельствующее о хорошей регенераторной функции костного мозга, но нормобластоз, резко выраженный у детей первых недель жизни, — явление патологическое (несовместимость крови по Rh). Появление большого числа нормобластов в крови у детей старшего возраста указывает на чрезмерное раздражение эритропоэза, близкое к истощению. Появление же макро- и мегалобластов говорит о переходе к патологическому кровотвореиию.
Появление эритробластов при отсутствии полихроматофилов свидетельствует о дегенеративном состоянии костного мозга. Точно так же базофильная пунктация эритроцитов, тельца Жолли, Кабо указывают на патологическую регенерацию.
Наличие низкого цветового показателя (ниже 1) говорит о раФ стройстве нормальной регенерации, о выпуске в кровь незрелых эритроцитов, которые растут быстрее, чем гемоглобин. Когда цветовой индекс выше 1 (гиперхромные анемии), налицо наличие усиленного раздражения эритроцитов внутри сосудов при недостаточной их регенерации. В зависимости от того, в каком состоянии находится эритропоэз, мы и должны ставить прогноз и применять средства либо успокаивающие, либо стимулирующие функцию костного мозга. В схеме 3 можно видеть развитие заболеваний кровотворного аппарата с явлениями раздражения и угнетения.
У нашего больного с алиментарной анемией нет признаков раздражения, а очень слабый ретикулез (2%о) и пойкилоцитоз говорят скорее 84
Дифференциальная таблица спленомегалий
Схема 8
Схема развития заболеваний кровотворного аппарата
Неполноценность кровотворного аппарата, вредности эндогенного характера, трофотоксические и трофопени-ческие факторы, бактериальные, химические и термические вредности
.С явлениями раздражения и гиперфункции
С явлениями угнетения и гипофункции
Эритропоз
Ренаратинная фаза
анемии. Анемия после кровотечений
Полиглобулия юворожденных при пороках сердца
|
|
|
|
|
Анемия недоношен- |
|
Эритобласти- |
|
Апластическая арегенераторная анемия |
|
и |
|
Полицитемия Вакеза |
—" |
ных, алиментарные и инфекционные анемии |
|
ческая анемия Якш—Гайема. Пернициозная |
|
Гранулопоэз
Лейкоцитоз ней-трофильного типа.
Нейтрофильная фаза борьбы с инфекцией
Миелондная реакция при инфекциях
Миелоз Хлорома
Лейкопения при инфекционных заболеваниях
Агранулоцитоз
Лимфопоэз
Лимфоцитоз. Лимфатическая фаза выздоровления
Лимфатическая реакция при инфекциях
Лимфаденоз
Лимфопения при инфекционных заболеваниях
Лимфогранулематоз. Лимфосаркоматоз
Монопоэз и регикуло-эндо-телиальная система
Моноцитарная фаза защиты
Моноцитарная янгина. Гнстиоцитоз при септических заболеваниях
Моноцитарная лейкемия. Болезнь Гоше—Пика—Ни-мана
Моноления при инфекционных заболеваниях
Громбопоэз
Увеличение после кровотечений и инфекций
Увеличение поели спленэктомии
Увеличение мега-кариоцитов при полицигемии
Тромбопения при инфекционных заболеваниях
Болезнь Верльгофа
о некотором угнетении эритропоэза. У девочки же с анемией Якш — Гайема картина крови свидетельствует о несомненном угнетении эритропоэза и вместе с тем налицо и состояние некоторого раздражения; об этом говорит наличие высокого ретикулеза (30%о), макроцитоза, поли-хроматофилии и нормобластоза. В состоянии раздражения находится и лейкопоэз, о чем свидетельствует высокий лейкоцитоз и наличие в крови незрелых форм нейтрофилов.
Если анализ крови обнаруживает пониженную регенераторную способность органов кровотворения, то вполне рационально применение раздражающей или стимулирующей терапии. Наиболее нежно действующей формой такой протеинотерапии являются внутримышечные или подкожные инъекции крови человека. Кровь разрушается и продукты распада стимулируют кровотворение. Меньшее значение имеет поступление в кровь гормонов, ферментов, электролитов. Обычно вводят по 15—20 мл крови с промежутками в 2—3 дня, всего 10—15 инъекций. Эта форма лечения особенно целесообразна при анемиях алиментарного и инфекционного происхождения. Инъекция молока и его продуктов (казеозана, лактана) и других белковых препаратов является уже более сильной раздражающей терапией и ею нужно пользоваться с большой осторожностью, ибо можно легко вызвать перераздражение кровотворного аппарата и тем самым привести к истощению функциональной способности костного мозга.
Можно также испробовать как стимулирующую терапию диатермию длинных трубчатых костей или освещение их ртутно-кварцевой лампой (особенно у детей, страдающих рахитом).
При наличии раздражения костного мозга следует прибегать к переливанию крови как методу, максимально разгружающему от работы. Внутривенное переливание крови действует благотворно на состав крови. Оно рефлекторно перестраивает нервную систему, содействуя мобилизации резервов крови из депо, изменяет физико-химические свойства крови и обмен веществ, замещая недостающее количество крови введением эритроцитов. К сожалению, это улучшение состава крови кратковременно (если при этом не происходит улучшения функции костного мозга) и потому приходится делать повторное переливание крови через 4—5 дней. Количество переливаемой крови обычно не должно превышать 10—15 мл на 1 кг веса. Детям грудного возраста одновременно вводят 40—60 мл, детям старшего возраста — 80—150 мл. Чаще всего пользуются свежей цитратной и консервированной кровью соответствующей группы. Очень хороший эффект дает переливание концентрированной взвеси эритроцитов, что исключает возможность реакции в пост-трансфузионном периоде. Ильпо предложил введение плазмы, лишенной 02, так как при этом в силу аноксии легче образуются гемопоэтины, стимулирующе влияющие на гемопоэз.
Переливание крови необходимо применять при всех тяжелых формах малокровия, когда требуется быстрое улучшение состава крови, например при тяжелых формах апластической и пернициозной анемии, анемии Якш — Гайема, постгеморрагических и постинфекционных анемиях. Противопоказанием являются только тяжелые расстройства компенсации сердечно-сосудистой системы, тяжелые острые нефриты и хронические нефропатии с резким нарушением функции печени, тяжелые эксудативные формы туберкулеза. Для лечения апластической анемии наиболее целесообразны переливания эритроцитной массы или новой трансфузионной массы [крови, заготовленной без стабилизатора с помощью ионообменных адсорбентов. Можно применять также и переливание лейкоцитной массы (М. С. Дульцин)].
Для лечения анемии на почве несовместимости крови по резус-фактору необходимо произвести так называемое заменное переливание крови. Цель такого мероприятия — удалить из организма эритроциты, подвергающиеся гемолизу, продукты их распада и антирезус агглютинин. С этой целью ребенку в первые же часы жизни вводят внутривенно через пупочные сосуды свежецитратную одноименную группу резус-отрицательной крови в количестве около 300 мл с одноименным выпусканием 250 мл крови ребенка. Если переливание делается не в первые часы после рождения, то кровь вводят и выпускают через вены головы или конечностей и из лучевой артерии. Этот метод заменного переливания крови спасает жизнь ребенка.
Лечение анемических состояний должно быть по возможности этио-патогенегическим, и только тогда оно дает длительный, прочный терапевтический эффект. С другой стороны, надо всегда учитывать, что при анемиях страдают функции внутренних органов, центральной нервной системы, процессы газообмена и поэтому всегда нужно обеспечивать ребенку наиболее оптимальные условия жизни, питания, режима. В большинстве случаев постельного режима и даже госпитализации не требуется, наоборот, надо ребенку предоставить возможность широко пользоваться воздухом, светом, прогулками, умеренными физическими упражнениями, легким спортом (коньки, лыжи), но избегать переутомления и удлинять часы отдыха, покоя, сна. Детям школьного возраста необходима некоторая разгрузка от дополнительных занятий и освобождение от учебы на 1—2 дня в неделю. Весьма целесообразно назначение водолечебных процедур, легкого массажа. Необходимо устранить дефекты в диетическом режиме, например одностороннее молочное или углеводное питание, наоборот, давать пищу в соответствии со вкусами ребенка, богатую полноценными белками, углеводами, солями, витаминами, с умеренным содержанием жира, поскольку жиры могут оказывать некоторое анемизирующее действие. Желательно обогащать пищу продуктами, богатыми железом и витаминами, стимулирующими гемо-поэз (А, В, С, В12, В6, фолиевой кислотой). Из продуктов, богатых железом, можно назвать печень, язык, творог, горох, чечевицу, фасоль, мясо, овсяную крупу, муку пшеничную, а из фруктов и ягод — землянику, изюм, чернослив, из овощей — морковь, брюкву, свежую капусту, картофель.
Широкое применение нашло лечение анемии печенкой ввиду богатства ее полноценными аминокислотами, витаминами (В!2 и фолиевой кислотой), железом, медью и фактором Касля. Детям дают от 50 до 100 г печенки в раннем возрасте и до 150—200 г более старшим; печенку лучше всего слегка проварить и промолоть и давать в виде прибавки к бульону, каше или в тушеном и слегка протертом виде или как паштеты. К сожалению, редко удается провести полный курс из-за отказа детей. В этих случаях можно прибегнуть к назначению камполона. Камполон (очищенный препарат печени) дает лучшие результаты при внутримышечном введении его по 1—2,5 мл ежедневно или через день. Антианемин — это препарат печени, содержащий и элементы кобальта. Печеночная терапия дает быстрый эффект как в отношении улучшения состава крови, так и общего состояния. Особенно эффективна она при злокачественном малокровии, при инфекционных анемиях и отчасти при алиментарных анемиях.
Несомненным эффектом обладает и применение препарата из свиного желудка (муковит) как содержащего один из факторов Касля. Его дозы — по 1—2—3 таблетки в сутки за 2—3 приема в слабокислом растворе (N/10 НС1) за 1 — П/г 4 До еды.
Из медикаментозных средств широкое распространение имеют препараты железа. В желудке неорганическое железо образует соединение с белками и углеводами, всасывается в двенадцатиперстной кишке, затем по лимфатическим путям поступает в общий ток крови и из него быстро захватывается селезенкой и печенью. Андрианова, использовав метод радиоактивных изотопов, доказала, что сахарат железа, введенный внутривенно, уже через 20—24 ч появляется в молодых эритроцитах в виде гемоглобинового Fe. Максимальное же количество его депонируется печенью и костным мозгом. Введение белков облегчает всасывание и усвоение Fe. Обычно детям назначается Ferrum hydrogenio ге-ductum в дозе 0,1—0,2 два раза в день в течение 3—4 недель, одновременно желательно назначать соляную кислоту или желудочный сок.
Из других препаратов железа можно назначать Ferrum carbonicum по 0,2—0,5; Ferrum lacticum по 0,2—0,5; Ferrum pyrophosphoricum cum ammonio citrici no 0,2—0,5.
Из органических препаратов применяется, но с меньшим эффектом, Lig. ferri albuminati по lJ2—1 чайной ложке, Ferratin по 0,1—0,25. Для хорошего всасывания железа необходимо образование в слизистой оболочке кишечника особого железо-фосфорного белкового комплекса — ферратина. Органические препараты железа могут вовсе не расщепляться в кишечнике и потому менее полезны, ибо лечебное действие оказывают только чистые ионы железа. Желательно также отдавать предпочтение соединениям двухвалентного железа, а не трехвалентным окисным. Препараты железа особенно эффективны при алиментарной и инфекционной гипохромной анемиях.
Хорошим раздражителем костного мозга являются препараты меди. Назначается обычно 0,5—1%-ный Cupri sulfurici crystallisati по 5—10 капель детям раннего и по 15—20 капель — детям старшего возраста. Медь дает быстрое нарастание числа эритроцитов, но с недостаточным содержанием в них гемоглобина. Поэтому целесообразно одновременное назначение и железа и меди.
За последнее время Андриановой и Богомоловой предложен препарат гемостимулин, который содержит растворимый белок, железо, микроэлементы тяжелых металлов и аскорбиновую кислоту. Дача железа при этом может быть уменьшена в 10 раз по сравнению с обычной. Этот препарат дается детям грудного возраста но 0,15 3 раза в день, детям старшего возраста — по 0,2—0,25 3 раза в день. Он оказывает хорошее стимулирующее влияние на эритропоэз, уменьшает раздражение эритроидиого отростка костного мозга, восстанавливает созревание зритробластов и нормализует процессы гемоглобинизации. Наблюдения К. Ф. Ширяевой подтвердили эффективность этого препарата и доказали его преимущества перед другими.
Препараты мышьяка в настоящее время применяются редко и только у детей старшего возраста, когда желательно вызвать раздражение костного мозга. Они показаны обычно в виде Sol. arsenicalis Fowled по 1—5 капель в зависимости от возраста, вместе с T-rae ment-hae, Chinae compositae внутрь и в виде 0,25%-ного раствора Natrii arse-nicici подкожно.
За последние годы при анемиях вошло в практику назначение фолиевой кислоты. Она дается внутрь в дозе по 'Д—7г мг. Эффект наступает через 2—3 недели в виде нарастания процента гемоглобина и числа эритроцитов. Фолиевая кислота также стимулирует биосинтез витамина В12, чем, возможно, и объясняется противоанемическое ее действие. Но, с другой стороны, известно, что введение витамина BV2 с витамином С повышает отложение фолиевой кислоты в печени. Некоторые авторы
указывают, что действие В!2 менее эффективно, чем одной фолиевой кислоты. Бобкова, Данович и другие видели эффект от Bi2 только при пернициозной анемии; Черняева и Эйдинова считают, что и фолиевая кислота и витамин В!2 эффективны и при пернициозной и алиментарной макроцитарной анемиях. Витамин Bi2 вводят внутримышечно по 5—10 у 1 раз в 2—3 дня.
Очень трудно поддается лечению апластическая анемия. Обычные методы лечения часто не дают эффекта. За последнее время рекомендуется лечение ее трансфузиями эритроцитной массы, а также новой трансфузионной смеси, т. е. крови, приготовленной без стабилизаторов с помощью ионообменных адсорбентов.
Саша 3. получал в клинике полноценную диету: 2 раза лимонно-яичную смесь по 200 мг, 2 раза кашу на отваре со сливками по 150 г и кисель, 1 раз мясной фарш (20 г) с овощным пюре (180 г). С целью пополнения запасов витаминов в организме и воздействия на обмен веществ была назначена витаминотерапия: аскорбиновая кислота по 50 мг, витамин Bi по 2 мг, витамин В2 по 2 мг внутрь вместе с глюкозой. Для ликвидации рахита был проведен курс лечения витамином D по 100 000 ед. в течение 6 дней.
С целью улучшения состава крови ребенку был назначен препарат (гемостимулин) № 4 по 0,15 3 раза в день в течение 28 дней. Эффект был, но не достаточно полный. Поэтому мы провели еще курс лечения противоанемическим витамином Bi2. Всего было сделано 8 инъекций. В результате лечения состав крови значительно улучшился: гемоглобин возрос до 55%, количество эритроцитов — до 4 590 000, аппетит также улучшился, ребенок сделался более живым, активным.
Сложнее дело обстояло с лечением второй больной, девочки с анемией Якш — Гайема. Эта девочка пробыла в клинике очень долго. Я изложу вам лечение только в течение последних 1'/2—2 месяцев.
Девочка находилась на полноценной и длительной диете: получала витамин С, В-комплекс, А и D, но ела не особенно охотно, оставалась мало подвижной. Ввиду наличия у нее дистрофии и пониженного общего тургора ей были назначены массаж и лечебная гимнастика, длительные прогулки на свежем воздухе. За время пребывания в клинике она переболела пневмонией, что несколько ухудшило ее состояние. Для лечения анемии сперва был проделан курс лечения гемостимулином (препаратом № 4) по 0,15 3 раза в день в течение 3 недель. Ввиду недостаточного терапевтического эффекта был проделан дополнительный курс лечения инъекциями камполона (по 1,5 мг через день). Но и этот метод не дал полного эффекта. Поэтому было применено лечение фолиевой кислотой и переливанием крови. Все эти методы дали некоторое улучшение состава крови, но размеры селезенки не уменьшились, равно как не ликвидировалась дистрофия и дизергия больной. Практика показывает, что при анемии Якш — Гайема требуется всегда очень длительное лечение. Этот ребенок будет выписан из клиники неизлеченным. Он будет взят под наблюдение диспансера. Несмотря на тяжесть заболевания мы не теряли надежды после повторных курсов лечения все же добиться и уменьшения размеров селезенки. Можно иметь в виду и спленэкто-мию. А пока надо обеспечить ребенку в домашних услоз-иях полноценное питание, правильный режим, пребывание на даче и периодические повторные курсы лечения противоанемическими средствами и трансфузиями крови.
