
Биология Ярыгин 2003
.pdfНаряду с генетическими факторами в регуляции экспрессии генов на стадии транскрипции принимают участие негенетические факторы — эффекторы. К ним относят вещества небелковой природы, взаимодействующие с белкамирегуляторами и изменяющие их способность соединяться с нуклеотидными последовательностями операторов. В зависимости от результатов такого взаимодействия среди эффекторов различают индукторы, запускающие транскрипцию, и корепрессоры, препятствующие ей.
Индукторы могут инактивировать белки-репрессоры, которые перестают соединяться с операторами, или повышать способность белков-активаторов (апоиндукторов) к связыванию с ними, что облегчает соединение РНК-полимеразы с промотором. В результате такого воздействия на регуляторные белки регулируемые гены активно транскрибируются.
Корепрессоры могут модифицировать апоиндукторы, теряющие при этом способность соединяться с операторами, или активировать репрессоры, находящиеся в неактивном состоянии. Следствием такого взаимодействия эффектора с белками-регуляторами является невозможность соединения РНКполимеразы с промотором и отсутствие транскрипции.
3.6.6.3. Регуляция экспрессии генов у прокариот
Изучение регуляции генной активности у прокариот привело французских микробиологов Ф. Жакоба и Ж. Моно к созданию (1961) оперонной модели регуляции транскрипции. Оперон — это тесно связанная последовательность структурных генов, определяющих синтез группы белков, которые участвуют в одной цепи биохимических преобразований. Например, это могут быть гены, которые детерминируют синтез ферментов, участвующих в метаболизме какоголибо вещества или в синтезе какого-то компонента клетки. Оперонная модель регуляции экспрессии генов предполагает наличие единой системы регуляции у таких объединенных в один оперон структурных генов, имеющих общий промотор и оператор.
Особенностью прокариот является транскрибирование мРНК со всех структурных генов оперона в виде одного полицистронного транскрипта, с которого в дальнейшем синтезируются отдельные пептиды.
Примером участия генетических и негенетических факторов в регуляции экспрессии генов у прокариот может служить функционирование лактозного оперона у кишечной палочки Е. colt (рис. 3.86). При отсутствии в среде, на которой выращиваются бактерии, сахара лактозы активный белок-репрессор, синтезируемый геном-регулятором (I), взаимодействует с оператором (О), препятствуя соединению РНК-полимеразы с промотором (Р) и транскрипции структурных генов Z, Y, А. Появление в среде лактозы инактивирует репрессор, он не соединяется с оператором, РНК-полимераза взаимодействует с промотором и осуществляет транскрипцию полицистронной мРНК. Последняя обеспечивает синтез сразу всех
181
medwedi.ru
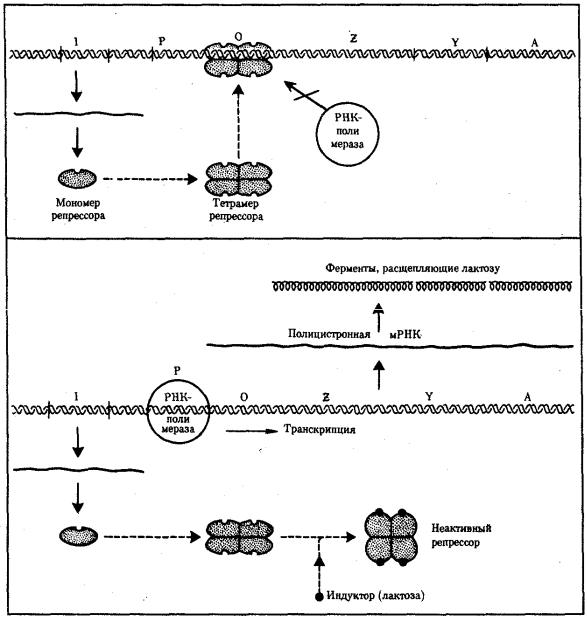
ферментов, участвующих в метаболизме лактозы. Уменьшение содержания лактозы в результате ее ферментативного расщепления приводит к восстановлению способности репрессора соединяться с оператором и прекращению транскрипции генов Z, Y, А.
Таким образом, регуляция экспрессии генов, организованных у прокариот в опероны, является координированной. Синтез полицистронной мРНК обеспечивает одинаковый уровень синтеза всех ферментов, участвующих в биохимическом процессе.
Рис. 3.86. Лактозный оперон Е. Соli
Включение loc-оперона с помощью индуктора — лактозы; объяснение см. в тексте
3.6.6.4. Регуляция экспрессии генов у эукариот
182
Всвязи с особенностями организации отдельных генов эукариот и генома в целом регуляция генной активности у них характеризуется некоторыми отличиями по сравнению с прокариотами.
У эукариот не установлено оперонной организации генов. Гены, определяющие синтез ферментов одной цепи биохимических реакций, могут быть рассеяны в геноме и, очевидно, не имеют, как у прокариот, единой регулирующей системы (ген-регулятор, оператор, промотор). В связи с этим синтезируемые мРНК
уэукариот моноцистронны, т.е. являются матрицами для отдельных пептидных цепей.
Внастоящее время механизмы регуляции и координации активности эукариотических генов интенсивно изучаются. Установлено, что их функционирование несомненно подчиняется регуляторным воздействиям, однако регуляция транскрипции у эукариот является комбинационной, т.е. активность
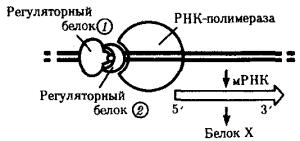
каждого гена регулируется большим спектром генов-регуляторов (рис. 3.87).
Рис. 3.87. Регуляция экспрессии гена, кодирующего белок Х у эукариот, двумя регуляторными белками
У многих эукариотических генов, кодирующих белки и транскрибируемых РНК-полимеразой II, в ДНК имеется несколько областей, которые узнаются разными белками-регуляторами. Одной из них является область, расположенная вблизи промотора. Она включает около 100 пар нуклеотидов, в том числе ТАТАблок, располагающийся на расстоянии 25 пар нуклеотидов от точки начала транскрипции. Установлено, что для успешного присоединения РНК-полимеразы II к промотору необходимо предварительное соединение с ТАТА-блоком особого белка — фактора транскрипции — с образованием стабильного транскрипционного комплекса. Именно этот комплекс ДНК с белком узнается РНК-полимеразой II. Последовательности нуклеотидов, примыкающие к ТАТА-блоку, формируют требуемый для транскрипции элемент, расположенный перед промотором.
Другая область, играющая важную роль в регуляции активности эукариотических генов, располагается на большом расстоянии от промотора (до нескольких тысяч пар нуклеотидов) и называется энхансером (от англ. enhance — усиливать).
183
medwedi.ru
И энхансер, и препромоторный элемент эукариотических генов содержат серию коротких нуклеотидных последовательностей, которые связываются с соответствующими регуляторными белками. В результате взаимодействия этих белков происходит включение или выключение генов.
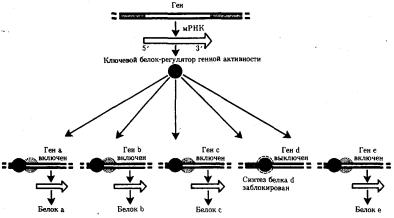
Особенностью регуляции экспрессии эукариотических генов является также существование белков-регуляторов, которые способны контролировать транскрипцию многих генов, кодирующих, возможно, другие белки-регуляторы. В связи с этим некоторые (главные) белки-регуляторы обладают координирующим влиянием на активность многих генов и их действие характеризуется плейотропным эффектом (рис. 3.88). Примером может служить существование белка, который активирует транскрипцию нескольких специфических генов, определяющих дифференцировку предшественников жировых клеток.
Рис. 3.88. Регуляция экспрессии многих генов эукариот одним белком-регулятором
Ввиду того что в геноме эукариот имеется много избыточной ДНК, а в каждой клетке организма транскрибируется всего 7—10% генов, логично предположение о том, что у них преобладает позитивный генетический контроль, при котором активация небольшой части генома оказывается более экономичной, нежели репрессия основной массы генов.
Несомненной особенностью регуляции транскрипции у эукариот является подчиненность этих процессов регулирующим влияниям со стороны гормонов организма. Последние часто играют роль индукторов транскрипции. Так, некоторые стероидные гормоны обратимо связываются особыми белками-рецепторами, образуя с ними комплексы. Активированный гормоном рецептор приобретает способность соединяться со специфическими участками хроматина, ответственными за регуляцию активности генов, в которых рецепторы узнают определенные последовательности ДНК.
Специфичность регулирующего воздействия гормона на транскрипцию обусловлена не только природой самого гормона, но и природой клетки-мишени, синтезирующей специфический белок-рецептор, который влияет на транскрипцию
184
определенного для данной клетки набора генов. Примером участия гормонов в регуляции активности определенных генов может служить влияние тестостерона на развитие тканей организма по мужскому типу при наличии специфического белкарецептора. Отсутствие последнего при мутации соответствующего гена не дает возможности гормону проникнуть в ядра клеток-мишеней и обеспечить включение определенного набора генов: развивается синдром тестикулярной феминизации, или синдром Морриса (см. разд. 3.6.5.2).
Следующая особенность регуляции генной активности у эукариот связана с образованием стойкого комплекса ДНК с белками — хроматина (см. разд. 3.5.2.2). Ведущая роль в компактизации ДНК принадлежит гистонам, поэтому они, несомненно, участвуют и в процессах регуляции генной активности (см. разд. 3.5.4). Непременным условием для осуществления транскрипции у эукариот является предварительная декомпактизация хроматина на соответствующем участке, где временно утрачивается связь с Hi-гистонами и несколько ослабляется связь с нуклеосомными гистонами. Правда, нуклеосомная организация хроматина не утрачивается даже в ходе транскрипции, однако контакт ДНК и негистоновых белков становится возможным и происходит дерепрессия гена.
Отличительной особенностью регуляции экспрессии генов у эукариот является возможность ее осуществления не только на стадии транскрипции, но и на других этапах растянутого во времени процесса реализации наследственной информации. Регуляция на стадии транскрипции является наиболее экономичной, но недостаточно быстро реагирующей на изменение ситуации. Так, возникшая в клетке потребность в каком-либо белке не может быть быстро удовлетворена путем включения транскрипции соответствующего гена. Синтезированный транскрипт должен подвергнуться процессингу, затем зрелая мРНК должна выйти из ядра в цитоплазму и, образуя комплекс с рибосомами, осуществить трансляцию информации, синтезировав пептид, который, лишь пройдя посттрансляционное изменение, формирует активный белок, необходимый клетке.
В том случае, когда клетке нужно прекратить синтез какого-то продукта, после выключения транскрипции соответствующего гена в цитоплазму некоторое время будут продолжать поступать созревающие молекулы мРНК, осуществляющие там синтез пептидных цепей, пока они не деградируют под действием ферментов. Таким образом, для эффективной регуляции экспрессии генов у эукариот должны существовать механизмы, работающие не только на стадии транскрипции, но и на других этапах этого процесса.
Связанная с экзон-интронной организацией генов необходимость процессичга, в том числе сплайсинга, делает возможным регуляцию этих процессов в ядре. В настоящее время обсуждается роль интронных участков ДНК в изменении схемы сплайсинга при синтезе антител (см. разд. 3.4.3.2) или цитохрома b (см. разд. 3.4.3.3). Это создает возможность, используя один и тот же первичный транскрипт, обеспечивать образование матриц для разных пептидов, вырезая из них разные последовательности или изменяя последовательности на 5'- и 3'-концах мРНК.
Очевидно, и транспорт зрелых мРНК из ядра в цитоплазму также
185
medwedi.ru
регулируется определенным образом, так как установлено, что лишь небольшая часть РНК, транскрибируемой с генов, после сплайсинга покидает ядро. Значительное количество ее деградирует. Возможно, это является результатом процессинга, приводящего к появлению «неправильных» матриц.
Существуют механизмы, обеспечивающие регуляцию процессов синтеза пептидных цепей. Они менее экономичны, но отличаются быстротой реагирования на изменения потребностей клетки в данном белке. Регуляция трансляции осуществляется на стадии инициации путем воздействия на один из факторов инициации, катализирующий присоединение к малой субъединице рибосомы тРНК, несущей метионин (формилметионин) (см. разд. 3.4.3). В результате при наличии в цитоплазме мРНК трансляции на ней не происходит. Такая ситуация наблюдается, например, при отсутствии в цитоплазме гема, что ведет к выключению трансляции глобиновых цепей гемоглобина.
Наконец, регуляция процесса реализации наследственной информации может осуществляться и на стадии посттрансляционных изменений. Прекращение этих процессов обусловливает задержку в формировании активных молекул белка при наличии необходимых для этого пептидных цепей. Например, для формирования активной формы белкового гормона — инсулина — из проинсулина должны вырезаться две субъединицы. Торможение этих процессов уменьшает выход конечного активного продукта.
Таким образом, рассмотренный выше пример регуляции экспрессии генов демонстрирует сложнейшие взаимосвязи, которые существуют между ними в геноме. Формирование любого признака поэтому нельзя рассматривать как результат действия одной пары аллельных генов в генотипе. В любом случае регуляция экспрессии ответственного за этот признак гена осуществляется при участии других генов.
3.6.7. Биологическое значение геномного уровня организации наследственного материала
Геномный уровень организации наследственного материала, объединяющий всю совокупность хромосомных генов, является эволюционно сложившейся структурой, характеризующейся относительно большей стабильностью, нежели генный и хромосомный уровни. На геномном уровне система сбалансированных по дозам и объединенных сложнейшими функциональными взаимосвязями генов представляет собой нечто большее, нежели простую совокупность отдельных единиц. Поэтому результатом функционирования генома является формирование фенотипа целостного организма. В связи с этим фенотип организма нельзя представлять как простую совокупность признаков и свойств, это организм во всем многообразии его характеристик на всем протяжении индивидуального развития. Таким образом, поддержание постоянства организации наследственного материала на геномном уровне имеет первостепенное значение для обеспечения нормального развития, организма и воспроизведения у особи в первую очередь видовых
186
характеристик.
В то же время допустимость рекомбинации единиц наследственности в генотипах особей обусловливает генетическое разнообразие их, что имеет важное эволюционное значение. Мутационные изменения, реализующиеся на геномном уровне организации наследственного материала,— мутации регуляторных генов, обладающих широким плейотропным действием, количественные изменения доз генов, транслокации и транспозиции генетических единиц, влияющие на характер экспрессии генов, наконец, возможность включения в геном чужеродной информации при горизонтальном переносе нуклеотидных последовательностей между организмами разных видов, — оказываясь иногда эволюционно перспективными, вероятно, являются основной причиной ускорения темпов эволюционного процесса на отдельных этапах исторического развития живых форм на Земле.
187
medwedi.ru
ГЛАВА 4 КЛЕТОЧНЫЕ
И МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ МЕХАНИЗМЫ ОБЕСПЕЧЕНИЯ СВОЙСТВ НАСЛЕДСТВЕННОСТИ И ИЗМЕНЧИВОСТИ У ЧЕЛОВЕКА
Человек как вид является продуктом биологической эволюции. Процесс возникновения вида Homo sapiens и длительное существование его на Земле, так же как и других видов, обусловлены реализацией таких свойств живого, как наследственность и изменчивость. Важнейшим доказательством родства Человека с другими живыми организмами, населяющими Землю, является в первую очередь сходство химической и морфологической организации их наследственного материала, способа записи наследственной информации и ее использования. Большое сходство наблюдается также в спектре белков, образуемых в организме человека и высших животных, например человекообразных обезьян.
Как у большинства видов, наследственная программа развития, записанная в молекулах ДНК с помощью универсального триплетного кода, организована у человека главным образом в его кариотипе. Хромосомный набор вида Homo sapiens состоит из 23 пар хромосом, содержащих 30—40 тыс. генов. Изучение структуры кариотипа и отдельных хромосом с использованием методик дифференциального (избирательного) окрашивания показало, что характер распределения красителя в разных хромосомах сходен у человека и человекообразных обезьян — шимпанзе и гориллы, имеющих 24 пары хромосом. Это сходство позволило сделать вывод, что одна из крупных хромосом человеческого кариотипа, очевидно, появилась в результате слияния двух акроцентрических хромосом обезьяноподобного предка (см. разд. 3.5.3.3).
Изучение процессов мутагенеза обнаружило, что отдельные гены человека могут изменять свою структуру с частотой, соизмеримой с таковой у других живых организмов (10-5—10-6 на один ген на поколение). Правда, в силу социальности человек создает в ходе своей деятельности новую среду с более высокими дозами и более широким спектром мутагенов, что не может не сказываться на интенсивности мутационного процесса в наследственном материале не только человечества, но и других видов живых организмов.
Таким образом, молекулярно-генетические механизмы обеспечения наследственности и изменчивости у человека имеют много общего с таковыми у других видов. Это делает возможным использование сведений, получаемых в ходе экспериментов на животных, для изучения наследственности и изменчивости у человека.
4.1.МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ МЕХАНИЗМЫ НАСЛЕДСТВЕННОСТИ И ИЗМЕНЧИВОСТИ
188
У ЧЕЛОВЕКА
Благодаря большому объему человеческого генома и более низкому давлению естественного отбора, связанному с социальной природой человека (см. § 1,9), в генофонде человечества за тысячелетия его существования в результате постоянно идущего мутационного процесса накоплено большое число аллелей многих генов. Это является причиной формирования у людей разнообразных вариантов признаков и свойств как на структурном, так и на биохимическом уровнях. В основе индивидуальных различий по многим белкам лежат изменения соответствующих генов. Изучение аминокислотного состава вариантов белков человеческого организма, интенсивности их синтеза, функциональной активности дает ценные сведения об организации и экспрессии его наследственного материала.
Удобной моделью для изучения молекулярно-генетических механизмов наследственности и изменчивости у человека является гемоглобин — специфический белок эритроцитов, легко выделяемый из организма без применения трудоемких биохимических методик. В результате длительного изучения этого белка накопилось много фактов, свидетельствующих об изменчивости его первичной структуры и свойств. В настоящее время обнаружено около 400 различных разновидностей гемоглобина, встречающихся как в нормальном развитии на разных стадиях онтогенеза, так и приводящих к различным заболеваниям.
Молекула гемоглобина состоит из четырех полипептидных цепей (двух α- и двух β-цепей), каждая из которых соединена с небелковым компонентом — гемом, содержащим железо. Две названные полипептидные цепи имеют варианты, контролируемые разными, но близкими нуклеотидными последовательностями, которые образуют два семейства генов (см. разд. 3.6.4.3). Различные нуклеотидные последовательности экспрессируются на определенных стадиях индивидуального развития — у эмбриона, плода, после рождения (см. § 6.2). При этом полипептиды, сменяющиеся в зависимости от стадии онтогенеза, незначительно различаются по аминокислотному составу. Так, Aγ и Gγ-глобины различаются по одной аминокислоте в 136-м положении (аланин или глицин). Вариант Aγ-глобина (TAγ) в 75-м положении вместо изолейцина имеет треонин. Цепь δ отличается от β-цепи лишь десятью аминокислотными остатками.
Из многочисленных мутаций гемоглобина большинство достаточно редки и лишь немногие из них встречаются чаще других, например HbS, HbC, НЬЕ. Большая часть вариантов гемоглобина (около 350) различается единичными аминокислотными заменами, причиной которых являются генные мутации, связанные с заменой оснований в нуклеотидных последовательностях α- или β- глобинового семейства. Многие аминокислотные замены существенно не влияют на функцию гемоглобина и не приводят к патологическим проявлениям. Как правило, это замены в обращенных наружу участках полипептидных цепей тетрамера.
Замены аминокислот, нарушающие нормальную спиральную структуру цепей, часто вызывают неустойчивость гемоглобина. Замена в участках, которыми α- и β- цепи контактируют друг с другом, влияют на сродство гемоглобина к кислороду.
189
medwedi.ru
Нарушения функций гемоглобина, возникающие в результате таких изменений структуры α- и β-глобиновых генов, ведут к появлению заболеваний, которые можно разделить на четыре основные группы.
1.Гемолитические анемии. Проявляются в распаде эритроцитов, зависящем от неустойчивости гемоглобина (описано около 100 вариантов нестабильных гемоглобинов с мутациями в гене β-цепи).
2.Метгемоглобинемии. Обусловлены ускоренным окислением
двухвалентного железа до трехвалентного и образованием гемоглобина М (известны пять таких мутаций в генах α- и β-цепей, состоящих в замене одного основания).
3.Эритроцитоз. Заключается в образовании большего, чем обычно, количества эритроцитов, что обусловлено повышенным сродством гемоглобина к кислороду, который с трудом высвобождается в тканях (таких мутаций известно около 30).
4.Серповидно-клеточная анемия. Заключается в замене гемоглобина НЬА на
HbS, который отличается растворимостью и кристаллизацией в условиях гипоксии, что приводит к изменению формы эритроцитов, и проявляется фенотипическим многообразием симптомов (см. рис. 3.21).
Заболевания первых трех групп наследуются по доминантному типу, так что гетерозиготы по мутантному гену страдают нарушением здоровья. Наследование серповидно-клеточной анемии при обычных условиях осуществляется по рецессивному типу, но в условиях сильной гипоксии, например при нахождении на высоте свыше 3000 м над уровнем моря гетерозиготы НbА HbS также страдают анемией.
Описанные мутантные формы гемоглобина возникают в результате изменений структуры генов по типу замены оснований. Мутации иного характера приводят к появлению аллелей глобинов, обусловливающих другие виды патологии. Так, нарушение процесса рекомбинации между аллельными генами (неравноценный кроссинговер) приводит к изменению числа нуклеотидов в них. Следствием этого может быть сдвиг рамки считывания. Нередким результатом таких структурных изменений генов является подавление синтеза той или иной цепи гемоглобина, приводящее к развитию патологических состояний, известных под общим названием талассемии.
Деления одного нуклеотида в 139-м триплете α-глобинового гена, состоящего из 141 триплета, приводит к сдвигу рамки считывания и прочитыванию в новой рамке терминирующего 142-го кодона. При этом (α-глобиновая цепь удлиняется на пять дополнительных аминокислот. Такой особенностью α-цепей характеризуется гемоглобин Vayne. Когда деления располагается ближе к 5'-концу, активный продукт не синтезируется и развиваются различные формы α-, β- и γ-талассемий.
Некоторые варианты гемоглобинов возникают в результате дупли-каций. Так, гемоглобин Grady несет дупликацию 116—118 аминокислотных остатков в γ-цепи. В гемоглобине Cranston удлинение р-цепи до 158 аминокислотных остатков является результатом дупликации AG-последовательности после 144-го триплета и последующего сдвига рамки с пропитыванием терминального кодона.
190
