
Билет 38.
Лейкозы у детей.




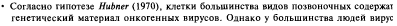

























2 Вопрос. Синдром внутриутробной задержки развития. Особенности недоношенного ребенка. Вскармливание
ЗАДЕРЖКА РОСТА (ВНУТРИУТРОБНОГО РАЗВИТИЯ) ПЛОДА
Под задержкой роста плода (ЗРП) понимают отставание размеров плода от предполагаемых при данном сроке беременности. Наибольшее распространение получило определение синдрома задержки роста плода как масса плода при рождении ниже десятого процентиля для данного срока беременности.
СИНОНИМЫ ЗАДЕРЖКИ РОСТА ПЛОДА
Задержка внутриутробного развития плода, внутриутробная задержка развития плода, синдром задержки развития плода, гипотрофия плода, fetal - rowth retardation (F- R), small for - estational a- e (S- A), small for date. В настоящее время термины «задержка внутриутробного развития плода» и «внутриутробная задержка развития плода» не употребляют, так как они избыточны, включают одновременно два понятия с одинаковым смыслом — «внутриутробный» и «плод».
КОД ЗАДЕРЖКИ РОСТА ПЛОДА ПО МКБ-10
Класс XV. Беременность, роды и послеродовый период (O00–O99)
Медицинская помощь матери в связи с состоянием плода, амниотической полости и возможными трудностями родоразрешения (O30–O48).
O36 Медицинская помощь матери при других установленных или предполагаемых патологических состояниях плода.
Класс XVI. Отдельные состояния, возникающие в перинатальном периоде (P00–P96)
Расстройства, связанные с продолжительностью беременности и ростом плода (P05–P08)
P05 Замедленный рост и недостаточность питания плода.
P07 Расстройства, связанные с укорочением срока беременности и малой массой тела при рождении, не классифицированные в других рубриках.
ЭПИДЕМИОЛОГИЯ ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
Частота развития синдрома задержки роста плода варьирует в широком диапазоне: 5,0–17,6%.
КЛАССИФИКАЦИЯ ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
По данным ультразвуковой фетометрии выделяют следующие формы ЗРП:
· симметричная форма* — пропорциональное уменьшение всех размеров тела плода по отношению к средним для данного срока беременности;
· асимметричная форма — уменьшение только размеров живота плода по отношению к среднему для данного срока беременности (отставание более чем на 2 нед или размер менее 5-го процентиля для данного гестационного срока), остальные размеры в пределах физиологической нормы;
· смешанная форма — отставание размеров живота более чем на 2 нед и отставание других фетометрических показателей в пределах 10–25 процентилей.
ЭТИОЛОГИЯ ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
Факторы риска, способствующие задержке роста плода:
· социальнобытовые (возраст менее 17 и более 30 лет, беременность вне брака, профессиональные вредности, тяжёлый физический труд, эмоциональное перенапряжение, курение, алкоголизм, наркомания, масса тела матери менее 50 кг);
· соматические (хронические специфические и неспецифические инфекции, экстрагенитальные заболевания);
· акушерскогинекологические (инфантилизм, нарушения менструальной функции, первичное бесплодие, гинекологические заболевания, аномалии матки, невынашивание беременности в анамнезе, осложнённое течение предшествующих беременности и родов);
· факторы, связанные с настоящей беременностью (токсикозы, гестоз, угроза прерывания беременности, многоплодие);
· плодовые (конституциональные, наследственные синдромы, внутриутробные инфекции, аномалии развития плода).
ПАТОГЕНЕЗ ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
У пациенток с последующим развитием синдрома задержки внутриутробного развития плода уже в I триместре беременности происходит неполноценная инвазия трофобласта в стенку спиральных артерий, вследствие чего развиваются гемодинамические нарушения маточноплацентарного кровообращения. Замедление кровотока в спиральных артериях и межворсинчатом пространстве приводит к снижению интенсивности газообмена между матерью и плодом. На ранних сроках гестации (до 22 нед) при недостаточно развитых механизмах саморегуляции плода (уменьшение количества клеток в гиперпластическую фазу клеточного роста) развивается симметричная форма задержки внутриутробного развития плода.
Во второй половине беременности ведущим патогенетическим звеном служит нарушение маточноплацентарного кровотока, которое приводит к хронической гипоксии и к задержке роста плода. На фоне хронической гипоксии происходит перераспределение плодового кровотока, направленное на обеспечение адекватного функционирования ЦНС. При этом основной поток артериальной крови направляется к головному мозгу плода — так называемый brain-sparin-effect. Клинически при этом формируется асимметричная форма задержки внутриутробного развития плода.
КЛИНИЧЕСКАЯ КАРТИНА И ДИАГНОСТИКА ЗАДЕРЖКИ РОСТА ПЛОДА
Диагностика задержки роста плода возможна с помощью наружного акушерского исследования (измерение и пальпация) и ультразвукового сканирования. Скрининговым методом диагностики задержки роста плода служит определение ВДМ, отставание которой от гестационного возраста на 2 и более сантиметра даёт основание заподозрить нарушение роста плода.
Более объективную информацию даёт ультразвуковая фетометрия, которая позволяет установить диагноз, определить форму и степень задержки роста плода. Ультразвуковая фетометрия должна проводиться в динамике. Оптимальный интервал между исследованиями должен составлять не менее двух недель.
Симметричная задержка роста, при которой отмечают пропорциональное уменьшение всех фетометрических показателей (размеров головы, живота, длины бедра), встречается у 10–30% беременных с синдромом ЗРП.
Правильная диагностика данной формы задержки внутриутробного развития плода возможна при точном знании срока беременности или при динамической эхографии, когда выявляют отставание темпов прироста фетометрических показателей. К ультразвуковым критериям, значимым для выявления задержки роста плода, относят вычисление отношения окружности головки к окружности живота плода. При симметричной форме задержки внутриутробного развития плода значения окружности головки и окружности живота у плода снижены в равной степени, поэтому это отношение имеет относительную диагностическую информативность. В таких случаях используют вычисление отношения длины бедра к окружности живота. Соотношение более 24,0 дает основание предположить задержку роста плода.
В то же время симметричное отставание фетометрических показателей не всегда позволяет с уверенностью установить диагноз ЗРП, так как маленькие размеры плода («small for date») могут быть обусловлены конституциональными особенностями родителей, то есть генетически детерминированы.
Асимметричная форма задержки внутриутробного развития плода характеризуется отставанием размеров туловища (живота) при нормальных размерах головки и бедра и наблюдается у 70–90% беременных с синдромом задержки роста плода. Диагностика асимметричной формы задержки роста плода не представляет затруднений при проведении ультразвуковой фетометрии, при этом диагностически значимым является отношение окружности головки к окружности живота плода. При асимметричной форме задержки внутриутробного развития плода это отношение превышает гестационные нормы (при физиологическом развитии плода это отношение до 32 нед превышает 1,0; на 32–34 нед оно приближается к 1,0; после 34 нед — ниже 1,0).
На основании результатов ультразвуковой фетометрии, помимо формы, можно определить степень задержки роста плода. При 1 степени отмечают отставание показателей фетометрии от нормативных на 2 нед, при II степени — на 3–4 нед, при III степени — более чем на 4 нед. Степень тяжести асимметричной формы задержки внутриутробного развития плода коррелирует с такими проявлениями хронической плацентарной недостаточности, как преждевременное созревание плаценты, уменьшение её толщины, а также маловодие.
При задержке внутриутробного развития плода независимо от её формы для определения компенсаторных возможностей плода необходимо оценить его функциональное состояние. Задержка роста плода (чаще асимметричная форма) нередко сочетается с гипоксией, которую выявляют при КТГ, допплерометрии плодовоплацентарного и плодового кровотока, изучении биофизического профиля плода.
При выраженной задержке внутриутробного развития плода (II–III степени) на кардиотокограммах можно наблюдать снижение вариабельности сердечного ритма, ареактивный нестрессовый тест; биофизический профиль плода характеризуется угнетением двигательной и дыхательной активности, мышечного тонуса. При допплерометрии отмечают нарушения кровотока в артерии пуповины, аорте, средней мозговой артерии, венозном протоке плода.
Характеристика особенностей внутриутробного развития при симметричной и ассиметричной форме задержки роста плода представлена в табл. 28-1. Отставание фетометрических параметров при симметричной форме задержки внутриутробного развития плода происходит во второй половине беременности, нередко сопровождаясь гемодинамическими нарушениями маточноплацентарного и плодовоплацентарного кровообращения. При выявлении симметричной формы задержки роста плода существенно увеличен риск хромосомной патологии у плода, что нередко требует проведения инвазивной пренатальной диагностики.
Асимметричная форма задержки внутриутробного развития плода наблюдается после 30 нед, пороки развития плода встречаются редко.
ЛЕЧЕНИЕ ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
Тактика ведения беременности и родов при задержке внутриутробного развития плода зависит от этиологии данной патологии, срока беременности, формы и степени выраженности задержки роста плода и направлена на коррекцию нарушений в системе мать-плацента-плод (см. «Плацентарная недостаточность»).
Для оценки темпов роста плода и его функционального состояния на фоне проводимой терапии необходимо проводить повторные УЗИ (через 7–14 дней) с допплерометрией кровотока в системе мать-плацента-плод (каждые 3– 5 дней), а также кардиомониторное наблюдение (ежедневно). Если на фоне проводимой терапии нормализуются темпы прироста показателей развития плода и его функциональное состояние находится в пределах нормы (компенсированная форма плацентарной недостаточности), можно продлить беременность. Родоразрешение проводят не ранее 37 нед беременности после подтверждения зрелости лёгких плода.
При неэффективности лечения (отсутствие прироста показателей развития плода в течение 2 нед) или ухудшении состояния плода (субкомпенсированная форма плацентарной недостаточности: систолодиастолическое отношение в средней мозговой артерии плода менее 2,2) необходимо досрочное родоразрешение, независимо от срока гестации.
При декомпенсированной форме плацентарной недостаточности (ЗРП II и III степени, отсутствие диастолического компонента кровотока и/или ретроградный кровоток в артерии пуповины, выраженные признаки гипоксии плода по данным КТГ) показано досрочное родоразрешение путём операции КС. При II степени ЗРП показания к абдоминальному родоразрешению определяются состоянием плода и сопутствующей акушерской патологией.
После рождения ребёнка с задержкой роста плода плаценту следует взвесить и внимательно осмотреть для выявления инфарктов, отложений фибрина, артериовенозных пороков, определения места прикрепления пуповины. Плаценту необходимо отправить в лабораторию патоморфологии для установления возможной причины задержки роста плода.
ПРОФИЛАКТИКА ЗАДЕРЖКИ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
Предгравидарная подготовка и устранение факторов риска задержки роста плода.
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТКИ
Основным средством для выявления задержки роста плода служит 3-кратное скрининговое УЗИ при беременности (в 12 и/или в 22 нед — для определения точного гестационного срока, а в 32 нед — для подтверждения соответствия размеров плода уже извест-ному сроку беременности). Подтвердить или исключить диагноз задержки роста плода можно с помощью измерения ВДМ и окружности живота во время регулярных визитов в женскую консультацию.
ПРОГНОЗ ПРИ ЗАДЕРЖКЕ ВНУТРИУТРОБНОГО РАЗВИТИЯ ПЛОДА
Плод с задержкой роста, развитие которого происходит в условиях недостаточной плацентарной перфузии, имеет повышенный риск перинатальных повреждений. Они наблюдаются у 65% новорождённых. Отмечается высокая частота гипоксии при беременности и асфиксии в родах, мекониальная аспирация. Задержка внутриутробного развития плода приводит к нарушению функционального созревания ЦНС, играющей основную координирующую и интегрирующую роль в процессах развития других органов и систем в антенатальном периоде. В раннем неонатальном периоде это приводит к нарушению становления тонических и рефлекторных реакций, а в последующей жизни у таких детей нередко наблюдаются неврологические нарушения от минимальных мозговых дисфункций до значительных психомоторных и соматических расстройств. Кроме того, новорождённые, родившиеся с гипотрофией, относятся к группе риска по развитию транзиторного гипотиреоза, реализации внутриутробной инфекции (вследствие относительного иммунодефицита). В зрелом возрасте у них достоверно чаще, по сравнению с родившимися без задержки роста плода, наблюдаются сердечно-сосудистые и неврологические заболевания.
Анатомо-физиологические особенности недоношенного ребенка
Недоношенными считаются дети, которые рождаются раньше 10 лунных месяцев внутриутробной жизни с массой от 1000 до 2500 г и ростом менее 45 см.
Недоношенный ребенок имеет своеобразные пропорции тела. Длина головы составляет примерно 1/3 – 1/4 длины тела, лицевая часть черепа обычно недоразвита, кости черепа нередко находят друг на друга, а малый родничок и боковые – открыты.
Ушные раковины плотно прилегают к черепу, они тонкие, нежные, легко деформируются.
Пупочное кольцо располагается низко над лобком. У девочек большие половые губы не прикрывают малых, у мальчиков нередко яички не опущены в мошонку.
Кожа у недоношенных детей дряблая, морщинистая, так как обычно подкожный жировой слой у них развит очень плохо, все тело покрыто пушком, особенно обильным на спине, плечах.
Плач у недоношенных детей слабый, пискливый. Обычно они вялы, много спят, их трудно разбудить для кормления.
Несовершенна у них и терморегуляция: температура тела зависит от температуры окружающей среды и легко может снижаться при охлаждении и повышаться при перегреве.
У недоношенного ребенка нередко отсутствует сосательный, а иногда и глотательный рефлекс в связи с функциональным недоразвитием нервной системы.
Для недоношенного ребенка характерна функциональная незрелость дыхательного центра, являющаяся причиной расстройств ритма и глубины дыхания. Причем чем меньше масса недоношенного ребенка при рождении и чем сильнее степень недоношенности, тем чаще у него бывают расстройства дыхания.
У недоношенных детей вследствие незрелости легочной ткани и поверхностного дыхания часто наблюдаются заболевания легких.
У преждевременно родившихся детей очень понижена сопротивляемость организма к любым неблагоприятным условиям, в том числе и к инфекциям. Вот почему они так подвержены различным болезням – гнойничковым, желудочно-кишечным и другим, почти все страдают рахитом и анемией, легко простуживаются.
Следовательно, недоношенные дети в. силу своих анатомо-физиологических особенностей нуждаются в особых условиях ухода, без соблюдения которых в прежние годы они очень часто погибали.
Выживаемость детей, родившихся преждевременно, обычно тем выше, чем меньше срок недоношенности. Бытующее у некоторых людей мнение, что при восьмимесячной беременности дети умирают чаще, чем при семимесячной, неверно. Чем дольше к моменту преждевременных родов ребенок находился в лоне матери, тем более жизнеспособным, более зрелым он рождается.
При правильной организации ухода и вскармливания и создании всех других необходимых условий недоношенные дети уже с первых дней жизни хорошо физически развиваются. Например, их масса в течение 1-го года нередко увеличивается в 5 – 8 раз.
ОСОБЕННОСТИ УХОДА И ОРГАНИЗАЦИЯ ВЫХАЖИВАНИЯ
Период постнатальной адаптации к окружающей среде у недоношенных детей растягивается на 1—2 мес. Вследствие незрелости органов и систем при неадекватных условиях возможны тяжелые срывы адаптации. Поэтому организация оптимальных условий выхажи-вания имеет для недоношенных детей чрезвычайно важное значение.
Температурный режим должен учитывать несовершенство терморегуляции и особую опасность охлаждения. Целесообразно создание специализированных родильных домов для приема преждевременных родов (перинатальных центров), в которых осуществляется мониторирование плода. Температура воздуха в родильном доме должна быть не менее 22—23; ребенка принимают в теплые стерильные пеленки или непосредственно после рождения и отсечения пуповины помещают на специальный столик с подогревом (в инкубатор). Глубоконедоношенных детей в некоторых странах заворачивают в металлизированные пеленки для предотвращения потерь тепла. Перевод недоношенного ребенка из родильного дома в стационар 2-го этапа выхаживания (как правило, на базе клинических детских больниц) при наличии специально оснащенных реанимационных машин ( с инкубатором и кислородным баллоном) может осуществляться уже в первые часы жизни при отсутствии явных противопоказаний к транспортировке (внутричерепные кровоизлияния, гемолитическая болезнь). В специализированных отделениях недоношенных детей размещают в боксированных палатах (2—3 ребенка в боксе). Детей, родившихся с массой тела менее 1500 г, а также более зрелых, но тяжелобольных недоношенных выхаживают в инкубаторах (кувезах), в которых поддерживают в зависимости от степени незрелости и возраста ребенка температуру 32—36 °С (в инкубаторах интенсивногоухода температура воздуха регулируется автоматически по показателям кожных датчиков для поддержания температуры тела ребенка 36—37 °С). Относительную влажность в инкубаторах на протяжении первой недели жизни ребенка постепенно снижают с 90 % до 60—70 %; концентрация кислорода зависит от состояния ребенка и в среднем составляет 35— 40 %. При подаче кислорода в кувез для профилактики его токсического воздействия наиболее целесообразно применять интенсивность оксигенации в зависимости от показателей Ро2 в крови ребенка (транскутанный мониторинг), которые не должны превышать 60 %.
Продолжительность пребывания ребенка в кувезе зависит от его индивидуальных особенностей. Все медицинские манипуляции проводят по возможности в кувезе. Положение ребенка в кувезе периодически изменяют, переворачивая его на другой бок или на живот. Температура воздуха в палатах колеблется от 23 до 25 °С, палаты регулярно проветривают (3—6 раз в сутки). В отделении 2-го этапа необходимо соблюдать строгий санитарно-эпидемиологический (влажная уборка, кварцевание воздуха, цикличное заполнение палат) и лечебно-охранительный режимы. Необходимы четкий контроль за состоянием здоровья кормящих матерей; ношение персоналом и матерями марлевых масок (со сменой каждые 4 ч); гигиенические ванны для детей (назначают индивидуально); внедрение микрометодов и неинвазивных методов обследования; специальные помещения для сбора и обработки грудного молока, для сбора белья; применение разовых предметов ухода и инструментов (иглы, шприцы).
Второй этап выхаживания недоношенного является начальным этапом реабилитации. Практически все недоношенные дети нуждаются в физической реабилитации: массаж, упражнения в воде, для чего необходимы специальное помещение с ваннами и обученный персонал. К реабилитации незрелых детей необходимо привлекать родителей, прежде всего мать (общение в палате, «кенгуру» — контакт «кожа к коже»). Детям, находящимся в отделении с целью реабилитации, необходимо в летнее время организовывать прогулки на веранде или в саду. Выписка недоношенного ребенка из стационара на педиатрический участок осуществляется при наличии стойкой адаптации к внешней среде: самостоятельное сосание, регулярная прибавка массы тела (при выписке 2200—2300 г и более), достаточная терморегуляция. Незадолго до выписки мать обучают приемам ухода, массажа и упражнениям в воде. Преемственность между стационаром и поликлиникой обеспечивается передачей подробной медицинской документации (выписка) с рекомендациями на ближайшие 1—3 мес.
ОСОБЕННОСТИ ВСКАРМЛИВАНИЯ
При определении способа кормления и назначении его объема и состава необходимо учитывать индивидуальные особенности незрелого ребенка, сниженную толерантность к пище и повышенную потребность в энергетических субстратах. Энтеральное вскармливание при отсутствии противопоказаний начинают обычно через 2—6 ч после рождения (сцеженное грудное молоко матери; более зрелых условно здоровых недоношенных можно приложить к груди).
Крайне незрелые и находящиеся в тяжелом состоянии дети обычно в первые 24—48 ч жизни получают только парентеральное питание. Оптимальная пища для недоношенного ребенка — материнское нативное грудное молоко. При отсутствии молока у матери используют пастеризованное донорское грудное молоко (нагревают до 68—70°С в течение 30 мин), так как пастеризация меньше, чем стерилизация, денатурирует белки молока, но все же частично разрушает его защитные факторы. Поэтому в крупных клиниках создаются банки грудного молока — сцеженное грудное молоко подвергают пастеризации в щадящем режиме (62,5 "С в течение 30 мин) и затем замораживают при температуре -18...-20 °С. Замороженное грудное молоко можно хранить в течение 3 мес.
Недоношенных детей с достаточно сформированным сосательным рефлексом, без тяжелой патологии обычно вскармливают из бутылочки в течение 1—2 нед (иногда чередуют прикладывания к груди и сосание из бутылочки); незрелым и тяжелобольным детям молоко вводят через назогастральный зонд иногда до конца 1-го — начала 2-го месяца жизни. По мере улучшения общего состояния часть кормлений через зонд заменяют кормлением из соски. Прикладывание к груди недоношенного ребенка осуществляют по индивидуальным показаниям, при активном сосании и массе тела 1800-2000 г.
Частоту кормлений также подбирают индивидуально. Для детей, вскармливаемых через зонд, возможны 2 варианта кормления: дробное порционное (7 или 10 раз в сутки, с 6-часовым ночным перерывом) или пролонгированное введение молока с помощью шприце-вых насосов (введение порции молока в течение 2—3 ч, обычно 5—6 раз в сутки с небольшими перерывами). Последний способ вскармливания особенно показан детям с синдромом срыгиваний, с явлениями частичного пареза кишечника или с дыхательной недостаточностью, а также при необходимости увеличения калорийности пищи маловесным и гипотрофичным детям.
В связи с тем, что в первые дни после рождения емкость желудка у недоношенных детей мала, объем одного кормления в 1-е сутки составляет 5—10 мл, на 2-е — 10—15 мл, на 3-й — 15—20 мл.
Расчет питания недоношенным детям необходимо проводить по калорийности. В первые 3—5 дней ребенок получает 30—60 ккал/кг в сутки, к 7—8-му дню — 60—80 ккал/кг, к концу 1-го месяца — 135—140 ккал/кг. С двухмесячного возраста детям, родившимся с массой тела более 1500 г, калорийность снижают до 130—135 ккал/кг; маловесным детям калорийность сохраняют на уровне 140 ккал/кг до 3 мес. Суточная потребность недоношенных детей в пищевых ингредиентах зависит от вида вскармливания. При естественном вскармливании (грудным нативным или пастеризованным молоком) ребенок должен получать в 1-м полугодии 2,2—2,5 г/кг белков, 6,5— 7 г/кг жиров, 12—14 г/кг углеводов; во 2-м полугодии 1-го года жизни 3—3,5 г/кг белков и 5,5—6 г/кг жиров. При смешанном и искусственном вскармливании потребность в белках составляет соответственно 3—3,5 и 3,5—4 г/кг; калорийность повышают на 10—15 ккал/кг.
Недоношенный ребенок нуждается в достаточном количестве жидкости. В качестве питья используют смесь раствора Рингера с 5 % раствором глюкозы (1:1). Общий суточный объем жидкости (87,5 % от объема молока + питье + внутривенные инфузии) к концу 1 -и недели составляет 70—80 мл/кг для детей с массой тела менее 1500 г и 80—100 мл/кг для более зрелых детей; в возрасте 10 дней — 125—130 мл/кг, к 15-му дню — 160 мл/кг, к 20-му — 180 мл/кг, к концу 1-го и на 2-м месяце — 200 мл/ кг (возможны варианты в зависимости от потери жидкости при фототерапии, эксикозе или, напротив, при склонности к отекам). Как правило, недоношенные дети нуждаются в дополнительном введении витаминов. В первые 2—3 дня жизни всем недоношенным детям вводят витамин К (викасол) в связи с недостаточным его синтезом в организме для профилактики геморрагических нарушений по 0,001 г 2—3 раза в день перорально или внутримышечно по 0,1—0,3 мл. Аскорбиновую кислоту применяют в первые месяцы жизни в дозе 30—100 мг в сутки в зависимости от вида вскармливания, тиамин и рибофлавин — по 2—3 мг в сутки (за исключением детей, получающих кефир). У недоношенных детей также более высокая потребность в витамине Е вследствие усиления процессов перекисного окисления липидов мембран. Поэтому обычно детям, не имеющим диспепсических расстройств, дают перорально 5 % раствор токоферола по 2—3—5 капель в день в течение 10—12 дней; тяжелобольным детям токоферол вводят внутримышечно.
Специфическую профилактику рахита недоношенным детям проводят строго индивидуально в зависимости от состояния ребенка, вида вскармливания, сезона года. Возможны разные схемы профилактики: уплотненный метод с использованием 0,5 % спиртового раствора эргокалыдиферола до 10 000—12 000 ME в день в течение 20 дней (курсовая доза 200 000— 300 000 ME); метод дробных доз — 500—2500 ME масляного раствора витамина D3 (0,0625 % или 0,125 %) в день в течение нескольких месяцев, на курс 200 000-400 000 ME. Прочие витамины назначаются недоношенным детям по клиническим показаниям. Детям с выраженной незрелостью или тяжелобольным комплекс витаминов-метаболитов, включающий витамины B1, B6, B12 и липоевую кислоту, применяют в виде ректальных суппозиториев. Недоношенные дети очень чувствительны к минеральному составу питания. Как правило, вследствие нарушения процессов всасывания незрелые дети при грудном вскармливании испытывают относительный дефицит кальция, при смешанном и искусственном - дефицит фосфора и некоторых микроэлементов (железо, цинк, медь). Большинство микроэлементов оптимально усваиваются при вскармливании нативным грудным молоком. При назначении препаратов кальция целесообразно ориентироваться на уровень ионизированного кальция в плазме крови ребенка.
При отсутствии материнского или донорского молока для питания недоношенных детей уже со 2-й недели жизни можно применять специально адаптированные молочные смеси, которые имеют более высокую энергетическую ценность (81 ккал в 100 мл) и более высокое содержание белка, что важно для питания незрелых детей. Это отечественная смесь «Новолакт-ММ», импортные смеси «Препилтти», «Претугтели», «Премалалак», «Ненатал». Помимо пресных смесей, используется ацидофильная смесь «Малютка», после 2 мес — кефир. Начиная с 3—4-й недели, недоношенному ребенку дают свежие фруктовые соки (обычно яблочный или гранатовый); с 2,5—3 мес — тертое яблоко и желток (при отсутствии противопоказаний). Возраст и порядок введения прикорма определяют индивидуально. При невозможности энтерального вскармливания (язвенно-некротический энтероколит, врожденные аномалии развития желудочно-кишечного тракта, упорная рвота и эксикоз на фоне различных заболеваний) ребенка переводят на частичное или полное парентеральное вскармливание. Существует 2 схемы парентерального питания: скандинавская (с использованием для внутривенного вливания аминокислот, глюкозы и жировых эмульсий типа липофундина и т. п.) и способ гипералиментации (только глюкоза и растворы аминокислот). Для недоношенных детей рекомендуют последний способ, так как они плохо переносят жировые эмульсии. Парентеральное питание требует точного расчета количества вводимых белков, углеводов и жидкости, постоянного контроля электролитного состава крови и КОС, мониторирования газового состава крови, АД и пульса.
