
Лекции УГМУ / Аритмии
.pdf
−в основе фибрилляции лежит явление быстрого асинхронного разряжения нескольких эктопических предсердных фокусов;
−множественные волны возбуждения могут следовать случайными путями через миокард предсердий, используя те участки, где уже восстановилась возбудимость. Волны возбуждения достигают атриовентрикулярного узла через непостоянные интервалы времени. Только часть их проводится к желудочкам. Одни волны возбуждения слишком слабы или слишком диффузны, чтобы пройти через атриовентрикулярный узел, другие же достигают узла во время его рефрактерного периода. В результате
11
ритм возбуждения желудочков становится абсолютно нерегулярным, поскольку атриовентрикулярный узел возбуждается в совершенно случайной последовательности.
Функциональные нарушения, характерные для фибрилляции предсердий, связаны с прекращением их эффективных сокращений. Множественные волны возбуждения, проходя по предсердной мускулатуре, вызывают некоординипрованные волны сокращений, изменяющие полости камер предсердий, однако последние не способны к эвакуации крови в желудочки. Кроме того, имеет место регургитация крови из желудочков в предсердия перед закрытием створок клапана. Потеря того вклада, который вносят предсердия в наполнение желудочков, в покое может не иметь большого значения. Однако резервные возможности сердца значительно снижаются как в связи с прекращением сокращения предсердий в последний момент перед систолой желудочков, так и нерегулируемым ритмом сокращений желудочков. Потеря предсердной «добавки» ограничивает ударный объем примерно на 29%. Кроме того, выпадают нервные регуляторные влияния, что снижает сердечный резерв в связи с отсутствием тахикардии при физической нагрузке.
Фибрилляция желудочков. Хаотичное распространение волн возбуждения по мускулатуре желудочков препятствует их координированным сокращениям точно так же, как и в предсердии. Поэтому фибрилляция желудочков может продолжаться лишь в течение короткого периода и обычно является непосредственной причиной смерти. Электрографические записи спонтанной фибрилляции желудочков в связи с этим обнаруживаются редко и представляют собой широкие, нерегулярные волны различной амплитуды и конфигурации.
Приступы фибрилляции желудочков могут быть и скоротечными (преходящими) и служить причиной периодических потерь сознания.
Механизмы формирования эктопических очагов возбуждения.
Термином re-entry обозначают явление, при котором электрический
12
импульс, совершая движение по замкнутому кругу (петле, кольцу) вокруг фиксированной анатомической структуры, такой инфарктный рубец, или зоны функционального замедления и блокировки проводимости в жизнеспособном миокарде, возвращается к месту своего возникновения
(circus movement).
Первоначально считалось, что сердце взрослого млекопитающего представляет собой терминально дифференцированный орган.
В настоящее время показано, что оно вырабатывает новые кардиомиоциты вырабатываются, а микроциркуляторное русло формируется на протяжении всей жизни.
Было также показано, что сердце взрослого млекопитающего содержит популяцию резидентных эндогенных стволовых и прогениторных клеток, обладающих определяющими их характеристиками: самообновлением, клоногенностью и мультипотентностью. Вскоре после этого с помощью различных мембранных маркеров и факторов транскрипции было идентифицировано несколько типов эндогенных кардиогенных стволовых клеток и эндогенных кардиогенных клеток-предшественников
Описание различных популяций эКСК привело к парадоксальной ситуации, когда сердце, ранее описанное как невозобновляемый орган, стало органом с наибольшим количеством различных типов резидентных стволовых и прогениторных клеток.
Стволовые клетки в миокарде:
-резидентные сердечные стволовые клетки
-эмбриональные стволовые клетки (ЭСК)
-стволовые клетки костного мозга (ККМ)
-мезенхимальные стволовые клетки (МСК)
Счисто теоретической точки, аутологичные стволовые клетки могут вызвать аритмии с помощью трех различных механизмов:
- в процессе дифференцировки к конечному зрелому фенотипу
13
стволовые клетки могут эволюционировать через промежуточные стадии, на которых внутренние электрофизиологические свойства клеточных мембран нестабильны, что, возможно, и способствует нарушению ритма;
-приживление стволовых клеток может быть связано с повышенной и гетерогенной адренергической иннервацией сердца, что может усилить пространственную неоднородность электрофизиологических свойств и инициацию желудочковой аритмии
-местная травма или отек могут способствовать развитию аритмий
Факторы, которые могут привести к усилению автоматизма.
Исследования клеточной ЭСК выявили у них триггерную активность. Если стволовые клетки имеют аномальную электрофизиологию и/или проявляют спонтанную электрическую активность, они могут стать источником электрического возбуждения.
Размеры водителя ритма первого порядка – синоаурикулярного (синусового) узла составляют 10-30 мм в длину, 5-7 мм в ширину и 1-2 мм толщины (глубины). Размеры водителя ритма второго порядка – атриовентрикулярного узла – 5-6 мм в длину, 2-3 мм в ширину.
Собственная кардиостимуляторная активность имплантированных клеток не может преодолеть нормальный синусовый ритм, если они занимают небольшую площадь (например, 200 мкм на 20 мкм). Напротив, образуя более крупные плотные области имплантации клетки полученные из hESCs, могут генерировать кардиостимуляторные потенциалы, что часто используется для биопацикуляторного лечения брадиаритмий с помощью биопейсмейкеров
Факторы, которые могут привести к повтормому входу – re entry.
Возникновение зоны функционального замедления и блокировки проводимости может быть обусловлено рядом механизмов, связанных с клетками-предшественниками. Стволовые клетки способствуют замедлению
14
проводимости между кардиомиоцитами. Появление в миокарде электрически неуправляемых клеток, в больших количествах, последние могут выступать в качестве поглотителей тока, тормозящих распространения потенциала действия. При отсутствии электрической связи стволовые клетки могут привести к увеличению площади блокады проводимости.
Факторы, которые могут привести к усилению триггерной активности. Сердечные эмбриональные клетки могут дифференцироваться как в кардиомиоциты, так и в пейсмейкерные (узловые) клетки. Накапливаются экспериментальные данные, касающиеся влияния микроокружения на дифференцировку кардиальных стволовых клеток и образование пейсмейкерных клеток.
В качестве механизма развития аритмий может выступать ослабление межклеточных контактов в результате сниженной экспрессии коннексинов (политопные интегральные мембранные белки
–белки щелевых контактов)
Длительность реполяризации имеет решающее значение для электрической стабильности сердца. Формирование реполяризационной неоднородности клеток – еще один механизм развития аритмий.
Лечение аритмий
15
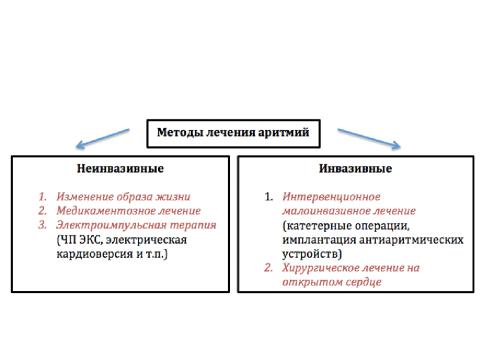
Кардиостимуляторы
Кардиовертеры Введение эмбриоидных клеток в миокард желудочков
продемонстрировало принципиальную возможность формирования новых островков клеток с кардиостимуляторной активностью. В настоящее время ведутся исследования по разработке биологических кардиостимуляторов, основанные на способности различных типов стволовых клеток дифференцироваться в пейсмейкерные клетки.
Нарушения проводимости: ускорение проводимости, замедление проводимости (блокады)
Нарушения проводимости миокарда. Нарушение проведения импульсов по проводниковой системе сердца получило название блокады. Блокады бывают частичными или полными. Блокада может быть врожденной, и в этом случае адаптация к низкой частоте сокращений желудочков начинается во внутриутробной жизни, обычно сердце во всех других отношениях нормально. Когда отсутствуют какие-либо другие дефекты, прогноз хороший, по крайней мере, у тех, кто выживет в раннем детстве. Блокада чаще бывает приобретенной, встречается в более пожилом
16
возрасте и обычно связана с фиброзом миокарда, развивающимся вследствие болезни коронарных артерий сердца. В других случаях она возникает после хирургических вмешательств, произведенных по поводу врожденных дефектов или пороков митрального или аортального клапана; если она упорно сохраняется или возобновляется по окончанию раннего послеоперационного периода, то прогноз становится неблагоприятным.
Возникновение блокад чаще всего связано со следующими причинами: 1) органические повреждения проводящей системы (некроз, фиброз, воспаление и др.); 2) замедление проводимости вследствие изменений функционального потенциала проводящих волокон (уменьшение амплитуды и скорости распространения деполяризации снижает возбудимость клеток и замедляет проведение импульса).
Обычно выделяют следующие блокады проведения: 1) полные или частичные; 2) двусторонние и односторонние (антроградные − нарушено проведение от центра к периферии и ретроградные – нарушено проведение от периферии к центру); 3) неполные и полные.
Постоянные (фиксированные) блокады, не зависящие от изменений частоты ритма. В основе их лежат либо анатомические повреждения, врожденные аномалии и дефекты проводящей системы, либо глубокие изменения электрических свойств клеточных мембран: частичная деполяризация, неполная реполяризация, снижение возбудимости и изменение характера электрического ответа.
Проведение импульса по блокированному волокну может быть:
а) недекрементным – то есть потенциал действия сохраняет свою амплитуду, крутизну и продолжительность, поддерживая устойчивую скорость проведения импульса;
б) декрементным − имеет место изменение свойств волокна вдоль его длинника (продольная блокада), и потенциал действия прогрессирующе утрачивает свою способность вызывать возбуждение лежащих дистальнее участков волокна. Отмечается постепенное уменьшение высоты и крутизны
17
фазы О ПД, укорочение ее длительности, снижение потенциала покоя. В результате шаг за шагом угасает сила стимула, проведение тормозится, пока не наступает полная остановка импульса. Подобная ситуация складывается при поражении атриовентрикулярного узла, содержащего быстрые и медленные клетки. Если имеет место поражение быстрых клеток, то в них уменьшается величина мембранного потенциала покоя, что приводит к ослаблению начального Na+-тока, крутизны и высоты фазы О ПД. Если потенциал покоя снижается до величины менее −60 мВ, Na+-ток полностью инактивируется, и становится невозможной быстрая деполяризация мембраны. Медленные каналы продолжают работать, и возбуждение клеток зависит от Ca2+−Na+-деполяризующего тока.
Непостоянные блокады:
1.Латентные блокады − отсутствуют в обычных условиях и появляются при изменении условий прихода импульса в проводящие пути.
2.Преходящие блокады − появляются временно при некоторых обстоятельствах и исчезают при устранении этих обстоятельств. Примером может служить преходящая ишемия.
3.Перемежающиеся блокады − характеризуются частыми и повторными переходами от нормального проведения к блокадами и наоборот.
4.Пароксизмальные блокады − зависят от частоты сердечного ритма:
а) тахизависимые − частота импульсов возрастает так, что какой-то участок проводящей системы (участок блокады) к приходу нового импульса находится в состоянии незакончившегося рефрактерного состояния − блокады фазы 3 ПД, или «блокады фазы 3»;
б) брадизависимые − усиление скорости спонтанной диастолической деполяризации может приводить к замедленному проведению или к остановке импульса.
В поврежденных, но не разрушенных, автоматических клетках мембранный потенциал бывает снижен уже к началу диастолы, то есть имеет место небольшая гипополяризация мембраны (первое условие блокады), и
18
кроме того ускоряется диастолическая деполяризация (второе условие). При удлинении сердечного цикла их мембранный потенциал уменьшается до такой низкой величины, что клетка утрачивают способность нормально реагировать на преходящие к ней импульсы.
Поскольку процесс развивается в 4 фазу ПД, эти блокады называют «блокадами фазы 4 ПД», или просто «блокадами фазы 4».
Блокада может быть обусловлена дефектами в области синоатриального узла, атриовентрикулярного узла или пучка Гиса.
Синоатриальная блокада. Патология достаточно редкая и обычно бывает обусловлена дистрофическими изменениями в миокарде, резкими нарушениями электролитного баланса, применением слишком больших доз наперстянки, усилением функции блуждающего нерва и т.д.
Импульс, генерируемый синусовым узлом, иногда не вызывает сокращения предсердий и желудочков, то есть происходит выпадение полного цикла сокращения сердца. Такое выпадение может наблюдаться через одно, два, три и т.д. сокращения сердца.
Атриовентрикулярная блокада. Может быть частичной или полной. При частичной блокаде могут иметь место замедление проведения с удлинением интервала Р-Q или выпадение сокращений. По выраженности этих явлений различают четыре степени блокады.
Блокада I степени характеризуется удлинением интервала Р−Q более 0,21 секунды (в норме 0,08−0,12 секунды).
При блокаде II степени происходит постепенное удлинение времени проведения импульса и, наконец, временный прерыв передачи импульсов, когда желудочки не получают импульсов от предсердий, и сокращение желудочков выпадает. В ходе наступившей длинной паузы восстанавливается проводимость, и следующий синусовый импульс вызывает сокращение всего сердца. Подобные периодические выпадения желудочкового комплекса с последующим восстановлением называют периодами Венкебаха-Самойлова. В основе формирования этих периодов лежит избирательное понижение
19
проницаемости клеточных мембран проводниковой системы сердца для ионов натрия при сохранении проницаемости для калия.
Блокада III степени − интервал Р-Q несколько удлинен, при этом выпадает каждое второе или третье сокращение желудочков, а на ЭКГ отсутствуют каждый второй или третий комплекс QRST.
Полная атриовентрикулярная блокада (блокада IY степени). Ее особенностью является идиовентрикулярный ритм, при котором желудочки сокращаются медленно и независимо от сокращений предсердий. На ЭКГ связи между зубцами Р и комплексом QRS нет, но конфигурация комплекса QRS нормальная. Расстояния Р−Р и R−R остаются постоянными. При этом предсердия сокращаются в обычном синусовом ритме 60−72 удара в минуту (о чем свидетельствует расстояние Р−Р), а желудочки – в более замедленном ритме − 30−40 сокращений в минуту, определяемом атриовентрикулярным узлом (о чем свидетельствует расстояние R−R).
Временная атриовентрикулярная блокада может быть вызвана, в частности, применением слишком больших доз наперстянки. Причиной стойкой атриовентрикулярной блокады обычно бывает тромбоз коронарной ветви, снабжающей кровью ткань узла.
Блокада ножек пучка Гиса (внутрижелудочковая блокада или продольная блокада). Патология связана с нарушением проведения импульсов ниже бифуркации пучка Гиса. Причиной блокады может быть тромбоз коронарных сосудов или дифтерийный миокардит.
Отличительной особенностью патологии является асинхронное возбуждение двух желудочков. При этом импульс с предсердия передается только на один желудочек, другой же либо не получает импульса, либо последний приходит через перегородку желудочков в ослабленном виде. Желудочек с пораженной ножкой пучка Гиса сокращается слабее − явление, получившее название гипосистолии. Чаще наблюдается блокада правой ножки, поскольку левая ножка, в свою очередь, делится на две основные части − передневерхнюю и задненижнюю.
20
