
2 курс / Биохимия / Доп информация и конспекты / Тканевое дыхание
.docx
 Тканевое
дыхание
Тканевое
дыхание
 Энергия
окисляющихся веществ используется
клетками для синтеза АТФ из АДФ.
Фосфорилирование АДФ в клетках происходит
путем присоединения неорганического
фосфата Н3РО4.
Реакция идет с затратой энергии.
Энергия
окисляющихся веществ используется
клетками для синтеза АТФ из АДФ.
Фосфорилирование АДФ в клетках происходит
путем присоединения неорганического
фосфата Н3РО4.
Реакция идет с затратой энергии.
Субстратное фосфорилирование
Субстратное фосфорилирование АДФ идет за счет энергии макроэргических связей некоторых соединений.
Этот процесс может происходить как в матриксе митохондрий, так и в цитоплазме клеток независимо от присутствия кислорода.

Окислительное фосфорилирование
Окислительное фосфорилирование АДФ - превращение АДФ в АТФ происходит с использованием энергии переноса электронов от органических веществ к кислороду. Энергию для окислительного фосфорилирования поставляют окислительно-восстановительные реакции. Процесс может происходить только в аэробных условиях с участием ферментов цепи переноса электронов (ЦПЭ) и АТФ-синтазы (АТФ-азы).
 Окислительное
фосфорилирование АДФ - основной механизм
синтеза АТФ в организме. Оно происходит
в митохондриях, которые являются
основными поставщиками АТФ и могут
рассматривать как "энергетические
станции" клетки.
Окислительное
фосфорилирование АДФ - основной механизм
синтеза АТФ в организме. Оно происходит
в митохондриях, которые являются
основными поставщиками АТФ и могут
рассматривать как "энергетические
станции" клетки.
Митчелл
Работу ЦПЭ изучал в 60-х годах прошлого века английский биохимик Питер Митчелл. Он создал хемиосмотическую теорию.
Согласно хемиосмотической концепции, движение электронов по дыхательной цепи является источником энергии для транслокации протонов через митохондриальную мембрану. Возникающая при этом разность электрохимических потенциалов (ΔμH+) приводит в действие АТФ-синтазу, катализирующую реакцию АДФ + Фн (Н3РО4) = АТФ + Н2О В дыхательной цепи есть только 3 участка, где перенос электронов сопряжен с накоплением энергии, достаточным для образования АТФ на других этапах возникающая разность потенциалов для этого процесса недостаточна. Максимальная величина коэффициента фосфорилирования, таким образом, составляет 3, если реакция окисления идет с участием НАД, и 2, если окисление субстрата протекает через флавиновые дегидрогеназы.
Структурная организация ЦПЭ
Комплекс |
Название |
Рабочая часть |
I |
NADH-дегидрогеназа |
FМN (FeS) |
III |
QH2-дегидрогеназа |
Цитохром bc1 (Fe3+) |
IV |
цитохром-с-оксидаза |
Цитохром аа3 (Fe3+, Сu2+) |
II |
сукцинатдегидрогеназа |
FАD (FeS) |
NAD+-зависимые субстраты: пируват, α-кетоглутарат, изоцитрат, малат, глутамат, лактат.
FAD-зависимые субстраты; сукцинат, ацил-KoA, глицерол-3-фосфат митохондриальный.
АТФ-аза
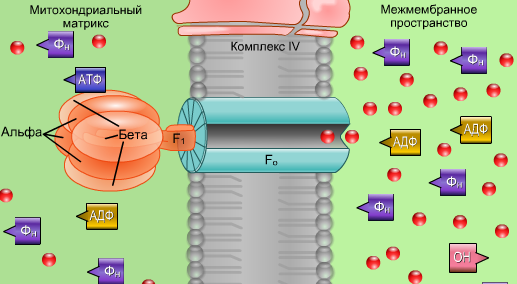
АТФ-аза состоит из субъединиц, которые формируют два компонента фермента: F0-компонент, который образует протоновую пору и F1-компонент, который обращен внешней стороной в митохондриальный матрикс. F1-компонент состоит из трех пар - альфа и бета субъединиц формирующих вращающийся цилиндр. Одна пара связывает АДФ и Фн, вторая пара синтезирует АТФ, а третья обычно свободная.
Когда протоны двигаются через протоновую пору F0-компонента их энергия используется на вращение альфа- и бета- парах из связанных с ними АДФ и Фн синтезируется новая молекула АТФ, а к свободным субъединицам присоединяются новые субстраты АДФ и Фн.
Продолжение синтеза АТФ требует постоянной концентрации АДФ и Фн. Адениннуклеотидтранслоказа обменивает митохондриальный АТФ на цитоплазматический АДФ. Транспорт Фн в матрикс происходит по механизму антипорта гидроксильным ионнам (ОН-). Благодаря работе этих двух транспортных систем и ЦПЭ генерирующей мембранный потенциал, АТФ-аза может продолжать синтез АТФ.
Коэффициент окислительного фосфорилирования
Коэффициент окислительного фосфорилирования Р/О показывает, какое количество неорганического фосфата затрачивается для фосфорилирования АДФ при использовании 1 атома кислорода на образование 1 молекулы воды. Коэффициент окислительного фосфорилирования числено равен количеству молей АТФ, синтезированных в результате окислительной реакции.
Для субстратов НАД-зависимых дегидрогеназ Р/О = 3.
Для субстратов ФАД-зависимых дегидрогеназ Р/О = 2.
Аскорбиновая кислота (витамин С) благодаря антиокислительным свойствам способна восстанавливать ионы Fe3+ в геме цитохромов а и а3 и активировать цитохром-с-оксидазу. В этом случае Р/О = 1.
Ингибиторы
Ингибиторы ферментов ЦПЭ подавляют активность ферментных комплексов I, III и IV. В результате их действия скорость восстановления коферментов NAD+ и FAD при этом снижается, что уменьшает скорость окислительных процессов, потребление кислорода и коэффициент Р/О:
▪ ингибиторы NADH-дегидрогеназы – барбитураты (снотворные), ротенон (инсектицид), пиерицидин (антибиотик);
▪ ингибиторы QH2-дегидрогеназы – антимицин А (антибиотик);
▪ ингибиторы цитохром-с-оксидазы – цианиды (СN-), угарный газ (СО), сероводород (Н2S);
Ингибиторы АТФ-синтазы снижают активность фермента, скорость фосфорилирования АДФ и коэффициента Р/О – олигомицин (антибиотик).
Ингибиторы ЦПЭ повышают: Соотношение NADH/NAD
Разобщители окисления и фосфорилирования
Разобщители окисления и фосфорилирования - липофильные протофоры легко проникают через липидный бислой и переносят протоны через внутреннюю мембрану митохондрии в матрикс, минуя АТФ-синтазу. Скорость образования метаболической воды и дыхания не изменяется или даже возрастает, но сопряжение окисления и фосфорилирования АДФ при этом ослабевает, Р/О снижается. Энергия окисления рассеивается в виде тепла, что приводит к повышению температуры тела человека (пирогенное действие).
▪ экзогенные разобщители – 2,4-динитрофенол (препарат для похудения), дикумарол (антикоагулянт), стрептомицин (антибиотик).
▪ эндогенные разобщители – жирные кислоты (ненасыщенные), гормоны щитовидной железы (тироксин), желчный пигмент биллирубин, UCP1(термогенин - белок, обнаруженный в митохондриях адипоцитов бурой жировой ткани), UCP 2 (белок, обнаружен во всех тканях млекопитающих, кроме паренхимальных гепатоцитов), UCP3 (обнаружен в скелетных мышцах).
Динитрофенол подавляет окислительное фосфорилирование АДФ, так как: Переносит Н+ через внутреннюю мембрану митохондрий в матрикс
