
13 ИБС
.pdfИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА
Cоставил ассистент Малашенко С.В., ВГМУ-2003.
Актуальность проблемы
Ишемическая болезнь сердца (ИБС) – группа заболеваний, обусловленных абсолютной или относительной недостаточностью коронарного обращения. Поэтому ишемическая болезнь – это коронарная болезнь сердца. В связи с большой социальной значимостью: высокой смертностью и инвалидизацией людей Всемирной организацией здравоохранения в 1965 г. она выделена как “самостоятельное заболевание”. Ишемическая болезнь в настоящее время широко распространена во всем мире, особенно в экономически развитых странах. На долю ИБС приходится около 70% случаев смерти от сердечнососудистых заболеваний. Болеют чаще мужчины в возрасте 40-65 лет. В последние десятилетия отмечена тенденция к «омоложению» этого
заболевания. |
|
|
|
|
|
Ишемическая болезнь сердца – это сердечная форма атеросклероза |
|||
и |
гипертонической |
болезни, |
проявляющаяся |
морфологически |
ишемической дистрофией миокарда, инфарктом миокарда,
кардиосклерозом. В очень редких случаях, ишемия миокарда может быть обусловлена недостатком поступления кислорода к сердечной мышце вследствие порока развития коронарных артерий, а так же при крайне резко возрастающей потребности миокарда в кислороде (причем приток крови может быть даже усилен, но все же недостаточен). Например, известны случаи гибели спортсменов высокого класса во время соревнований от ишемии миокарда, при этом никакой патологии коронарных сосудов в анамнезе они не имели, не была она обнаружена и на вскрытии.
Ишемическая болезнь сердца течет волнообразно, сопровождаясь коронарными кризами, т.е. эпизодами острой (абсолютной) коронарной недостаточности, в большинстве случаев возникающими на фоне хронической (относительной недостаточности коронарного кровообращения). В связи с этим различают острую и хроническую формы ишемической болезни сердца.
Острая ишемическая болезнь сердца морфологически проявляется ишемической дистрофией миокарда и инфарктом миокарда, хроническая ишемическая болезнь сердца (ХИБС) – кардиосклерозом (диффузным мелкоочаговым и постинфарктным крупноочаговым),
осложняющимся иногда хронической аневризмой сердца. Здесь стоит внести следующий комментарий. В более ранних морфологических классификациях выделяли донекротическую стадию инфаркта миокарда - 1 стадию. Однако, по определению инфаркт - это сосудистый некроз, то есть 1-ая стадия фактически звучит как донекротическая стадия сосудистого некроза, то есть некорректно. В связи с этим предложено заменить 1-ую (донекротическую) стадию на ишемическую дистрофию
2
миокарда, а в течении собственно инфаркта миокарда выделять 2 стадии: 1) некротическая стадия; 2) стадия рубцевания (см. ниже).
Ишемическая дистрофия миокарда, или острая очаговая дистрофия миокарда, развивается при относительно кратковременных эпизодах коронарного криза, когда возникают характерные для инфаркта миокарда клинические и электрокардиографические изменения при отсутствии некроза кардиомиоцитов (отсутствует повышение активности ферментов в сыворотке крови: трансаминаз, лактатдегидрогеназы, КФКМВ и др.). Если при этом состоянии наступила смерть больного, то на
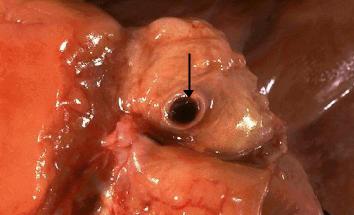
аутопсии в участках ишемии обнаруживается дряблый и более бледный миокард, иногда пестрый и отечный. Нередко в коронарной артерии обнаруживается свежий тромб.
Рис.1. Свежий тромб обтурирующий просвет коронарной артерии.
Следует отметить, что далеко не всегда эти признаки четко определяются на вскрытии, что создает известные трудности для морфологической диагностики. Для убедительного выявления участков выраженной ишемии миокарда предложен ряд методов. Макроскопически при обработке поверхности разреза миокада раствором солей тетразолия, теллурита калия, участки ишемии выглядят светлыми на темном фоне неизмененного миокарда, потому что в участках ишемии активность окислительно-восстановитсльных ферментов резко ослаблена и поэтому зерна формазана, а также восстановленный теллур не выпадают.
Микроскопически находят дилатацию капилляров, стаз и сладжфеномен эритроцитов, отек интерстициальной ткани, периваскулярные кровоизлияния, скопления лейкоцитов по периферии зоны ишемии. Мышечные волокна теряют поперечную исчерченность, лишены гликогена, они интенсивно окрашиваются эозином, фуксином, пиронином и реактивом Шиффа, что свидетельствует о некробиотических изменениях. Окрашенные акридиновым оранжевым, они дают в люминесцентном микроскопе не оранжевое, а зеленое свечение, что позволяет отличить зону ишемии от интактного миокарда. Поляризационно-оптически выявляется обилие контрактур.
Ранние электронно-микроскопические и гистохимические изменения сводятся к уменьшению числа гранул гликогена, снижению активности окислительно-восстановительных ферментов (особенно дегидрогеназ и диафораз), набуханию и деструкции митохондрий и саркоплазматической сети. Эти изменения, связанные с нарушением тканевого дыхания,
3
усилением анаэробного гликолиза и разобщением дыхания и окислительного фосфорилирования, появляются уже через несколько минут от начала ишемии.
Осложнением ишемической дистрофии миокарда чаще всего является острая сердечная недостаточность (морфологический ее эквивалент - острое общее венозное полнокровие и отек легких), она же становится непосредственной причиной смерти.
Инфаркт миокарда – это ишемический некроз сердечной мышцы. С точки зрения клиники он характеризуется: 1) характерными симптомами - (это не обязательный критерий); 2) изменениями ЭКГ; 3) ферментемией. Морфологически, как правило, это ишемический (белый) инфаркт с геморрагическим венчиком.
Инфаркт миокарда принято классифицировать по ряду признаков: o по времени его возникновения;
o по локализации в различных отделах сердца и сердечной мышцы; o по распространенности;
o по течению.
Инфаркт миокарда – понятие временнόе.
Первичный (острый) инфаркт миокарда длится примерно 8 недель с момента приступа ишемии миокарда. Если инфаркт миокарда развивается спустя 8 недель после первичного (острого), то его называют повторным инфарктом. Инфаркт, развившийся в течение 8 недель существования первичного (острого), его обозначают как
рецидивирующий инфаркт миокарда. Это деление имеет определенное значение, т.к. считается, что при адекватном лечении острого инфаркта миокарда (а это первые 8 недель), рецидивирующий инфаркт миокарда развиваться не должен.
Инфаркт миокарда локализуется чаще всего в области верхушки, передней и боковой стенок левого желудочка и передних отделов межжелудочковой перегородки, т. е. в бассейне передней межжелудочковой ветви левой венечной артерии, которая функционально более отягощена и сильнее других ветвей поражается атеросклерозом. Реже инфаркт возникает в области задней стенки левого желудочка и задних отделов межжелудочковой перегородки, т. е. в бассейне огибающей ветви левой венечной артерии. Когда атеросклеротической окклюзии подвергаются основной ствол левой венечной артерии и обе его ветви, развивается обширный инфаркт миокарда. В правом желудочке и, особенно в предсердиях инфаркт развивается очень редко.
Топография и размеры инфаркта определяются не только степенью поражения определенных ветвей венечных артерий, но и типом кровоснабжения сердца (левый, правый и средний типы). Поскольку атеросклеротические изменения обычно интенсивнее выражены в более развитой и функционально отягощенной артерии, инфаркт миокарда чаще наблюдается при крайних типах кровоснабжения – левом или правом. Эти особенности кровоснабжения сердца позволяют понять, почему, например,

4
при тромбозе нисходящей ветви левой венечной артерии в разных случаях инфаркт имеет различную локализацию (передняя или задняя стенка левого желудочка, передний или задний
отдел межжелудочковой перегородки).
Рис.2. Тромбоз нисходящей ветви левой передней коронарной артерии. В просвете вскрытой коронарной артерии свежие красные тромботические массы. Зона инфаркта со стороны эпикарда выглядит темно-красной.
Размеры инфаркта определяются степенью стеноза венечных артерий, функциональной способностью коллатерального кровообращения, уровнем закрытия (тромбоз, эмболия) артериального ствола, от функционального состояния миокарда. Так, например, у стариков длительно страдающих стенокардией, коллатеральное кровоснабжение лучше
выражено, чем у более молодых людей, поэтому размеры инфаркта у них, как правило, меньше. При гипертонической болезни, сопровождающейся гипертрофией мышцы сердца, инфаркты имеют более распространенный характер.
Топографически различают:
o субэндокардиальньный инфаркт; o субэпикардиальный инфаркт;
o интрамуральньный инфаркт (при локализации в средней части стенки сердечной мышцы);
o трансмуральный инфаркт (при некрозе всей толщи сердечной мышцы).
При вовлечении в некротический процесс эндокарда (субэндокардиальный и трансмуральный инфаркты) в нем развивается реактивное воспаление, на эндотелии появляются тромботические наложения. С одной стороны, плотный тромб, фиксированный к поврежденной стенке сердца, укрепляет ее, что имеет положительное значение. С другой стороны, этот тромб может сыграть отрицательную роль - стать источником тромбоэмболии. При субэпикардиальном и трансмуральном инфарктах нередко наблюдается реактивное воспаление наружной оболочки сердца – фибринозный перикардит.
По распространенности некротических изменений в сердечной мышце, различают:
o мелкоочаговый; o крупноочаговый;

o трансмуральный инфаркт миокарда.
Рис.3. Трансмуральный инфаркт миокарда. В межжелудочковой перегородке и передней стенке левого желудочка имеется некроз сердечной мышцы (белый инфаркт с геморрагическим венчиком), занимающий всю толщу миокарда.
Втечении инфаркта миокарда различают две стадии: o некротическую стадию;
o стадию рубцевания.
Внекротической стадии область инфаркта представляет собой
некротизированную ткань, которая макроскопически выглядит как тусклый, дряблый, западающий на разрезе участок бело-желтого цвета, окруженный зоной кровоизлияний (геморрагический венчик). Она образуется в результате того, что спазм сосудов по переферии инфаркта сменяется паратическим их расширением и развитием кровоизлияний. Микроскопически очаг некроза представлен погибшими кардиомиоцитами с разрушенными ядрами, отсутствием поперечной исчерченности саркоплазмы, ее гомогенезацией, глыбчатым распадом и гиперэозинофилией. Периваскулярно выявляют мелкие участки сохранившихся кардиомиоцитов. Область некроза отграничена от сохранившегося миокарда зоной полнокровия и лейкоцитарной инфильтрации, в основном нейтрофильной (демаркационное воспаление). Вне очага некроза отмечается неравномерное кровенаполнение, кровоизлияния, исчезновение из кардиомиоцитов гликогена, появлением в них липидов, деструкция митохондрий и саркоплазматической сети, некроз единичных мышечных клеток.
6
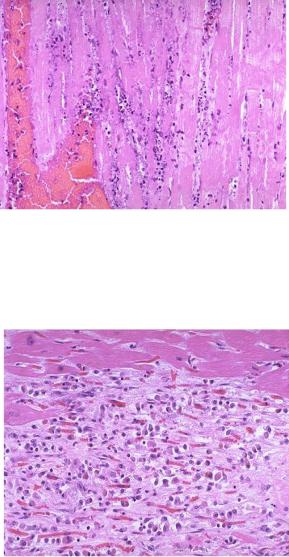
Рис.4. Острый инфаркт миокарда (2-е сутки). В кардиомиоцитах отмечается утрата поперечной исчерченности, глыбчатый распад и гиперэозинофилия саркоплазмы. Краевое стояние и выход за пределы микроциркуляторного русла лейкоцитов, осуществляющих лизис погибших кардиомиоцитов.
Стадия рубцевания (организации) инфаркта начинается по существу тогда, когда на смену лейкоцитам приходят макрофаги и молодые клетки фибробластического ряда. Макрофаги принимают участие в резорбции некротических масс, в их цитоплазме появляются липиды, продукты тканевого детрита. Фибробласты, обладая высокой
ферментативной активностью, участвуют в фибриллогенезе.
Рис.5. Организующийся инфаркт миокарда (1-2 недели). Вверху сохраненные кардиомиоциты. В зоне организации большое количество макрофагов среди многочисленных вновь образованных капилляров, фибробластов и небольшого количества коллагеновых волокон.
Организация инфаркта происходит как из зоны демаркации, так и из “островков” сохранившейся ткани в зоне некроза. Этот процесс продолжается 7–8 недель, однако, эти сроки подвержены колебаниям в зависимости от размеров инфаркта и реактивности организма больного. Новообразованная соединительная ткань в начале рыхлая (грануляционная), затем она созревает в грубоволокнистую рубцовую, в которой вокруг сохранившихся сосудов видны островки гипертрофированных мышечных волокон. Таким образом, при организации инфаркта на его месте образуется плотный рубец. В таких случаях говорят о постинфарктном крупноочаговом кардиосклерозе.
Сохранившийся миокард, особенно по периферии рубца, подвергается регенерационной гипертрофии.
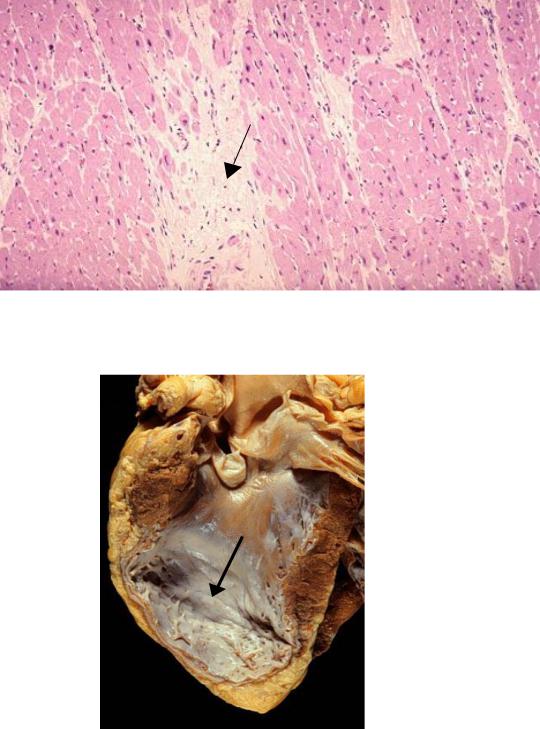
очаговый постинфарктный Грубоволокнистая соединительная ткань в зоне миокарда (показана переферии которой
кардиомиоциты.
в области рубца может хроническая
аневризма сердца (патологическое выпячивание стенки), в зоне которой часто происходит образование тромбов. Эти тромбы могут иметь благоприятное значение т.к. они укрепляют истонченную стенку аневризмы и тем самым препятствуют ее разрыву, однако они же могут стать источником тромбоэмболий
(неблагоприятное значение).
Рис.7. Хроническая аневризма сердца/ В зоне перенесенного инфаркта миокарда сформировалась хроническая аневризма (показана стрелкой). Эндокард, выстилающий ее стенку белесый.
Осложнениями инфаркта являются кардиогенный шок, фибрилляция желудочков, асистолия, острая сердечная недостаточность, миомаляция (расплавление некротизированного миокарда), острая
аневризма и разрыв сердца (гемоперикард и тампонада его полости), пристеночный тромбоз, перикардит.
Смерть при инфаркте миокарда может быть связана как с самим инфарктом миокарда, так и с его осложнениями. Непосредственной причиной смерти в ранний период инфаркта становятся фибрилляция желудочков, асистолия, кардиогенный шок, острая сердечная недостаточность, приводящие к развитию отек легких.. Смертельными осложнениями инфаркта миокарда в более поздний период (чаще на 5-7
сутки) являются разрыв сердца или его острой аневризмы с
кровоизлиянием в полость перикарда, а также тромбоэмболии (например, сосудов головного мозга) из полостей сердца, когда источником тромбоэмболии становятся тромбы на эндокарде в области инфаркта.
8
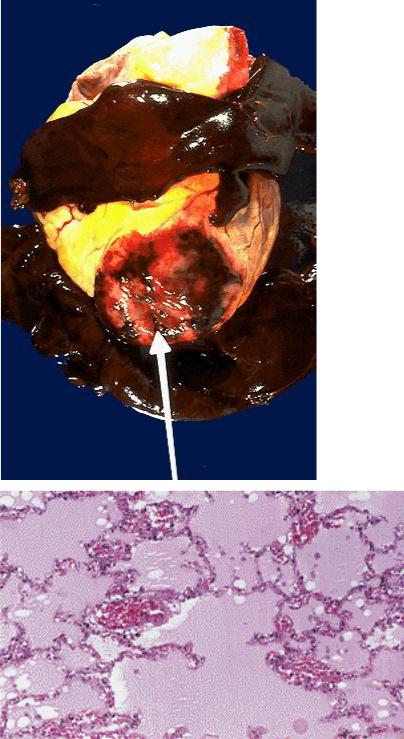
Рис.8. Трансмуральный инфаркт миокарда с разрывом и гемотампонадой. В зоне инфаркта вследствие миомаляции произошел разрыв некротизированной сердечной мышцы (показан стрелкой), который обычно имеет щелевидный вид. Имеется гемотампонада перикарда (темно-красные свертки крови).
Рис.9. Альвеолярный отек легких.
