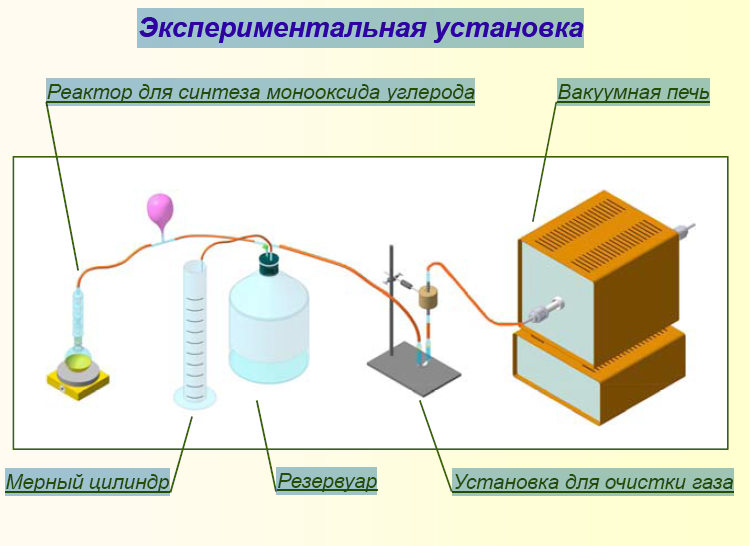
ЛЕКЦИЯ 9
-
Свойства карбида кремния( физические и химические), особенности строения.
Свойства карбида кремния:
1. Высокая температура плавления,
2. Высокая прочность,
3. Низкая плотность,
4. Низкий коэффициент теплового расширения,
5. Высокий показатель микротвердости,
6. Высокая химическая устойчивость,
7. Высокое сопротивление износу.
Применение карбида кремния:
1. Авиа- и ракетостроение,
2. Термобарьерные материалы,
3. Композиционные материалы,
4. Приборостроение,
5. Электроника,
6. Абразивные и режущие инструменты,
7. Сенсорика.
Физические свойства:
Является твердым, тугоплавким веществом. Кристаллическая решетка аналогична решетке алмаза. Является полупроводником.
Существует около 250 модификаций карбида кремния.
Карбид кремния бывает α и β.
|
|
Tпл. |
Теплопроводность |
|
α-SiC |
2970 |
490 |
|
β-SiC |
Выше 2100 переходит в α |
320 |
Химические свойства:
Является химическим соединением кремния с углеродом, что осуществляется при высоких температурах, при этом он содержит около 70% Si и приблизительно 30 % С. Обладает высокой устойчивостью и для разложения его в инертной атмосфере требуется очень высокая температура – до 2830 градусов. При нагревании входит в реакцию с кислородом, также в присутствии кислорода растворяется в щелочах. Растворить карбид кремния способны окисляющие кислоты и их смеси, а разложить его можно при помощи сильно перегретого пара, температура которого достигает 1300 градусов.
Окисляется выше 10000С:
SiCтв+O2(г)= SiO2(тв)+CO2
ΔG = –925 кДж/моль
Не взаимодействует при высоких температурах даже с : Cl (до 6000С) , Br (до 8000С),
S (пар) (до 3000С) , F (до 3000С)
Взаимодействие с щелочами:
SiC + 2NaOH = Na2SiO3 + 3Н2O + CO2
Всего существует 4 вида синтеза:
-
Карботермическое восстановление диоксида кремния.
-
Химическое осаждение из газовой фазы (CVD)
-
PVD
-
Термическая деструкция полимерных кремнийорганических соединений.
-
Карботермическое восстановление диоксида кремния.
SiO2(тв/ж)+3C(тв)=SiCтв+2СО2 ;
дельтаH=618,5 кДж/моль
Механизм:
SiO2 (тв./ж.) + 3C (тв.) = SiО (г.) + 2С (тв.) + CO (г.)
SiO (г.) + 2C (тв.) = SiС (тв.) + CO (г.)
Основные процессы, протекающие в системе SiO2+3C:
I
SiO2 + C → SiO + CO
SiO + 2C → SiC + CO
Si(г) + C → SiC
II
2SiO2 + SiC → 3SiO + CO
SiO2 + Si → 2SiO
III
SiO + SiC → 2Si + CO
2Si(г) + CO → SiC + SiO
Si (ж) → Si (г)
Ключевым фактором является морфология исходных фаз.
При температуре ниже 1500º С скорости процессов распределены как: – I > II > III.
При температурах от 1500 до 1800º С, скорость процессов в группах I и II приблизительно равна
Выше 1800º С в системе в основном протекают процессы из группы III.
Химическое осаждение карбида кремния из газовой фазы.
Например:
CH3SiCl3 → ·CH3 +·SiCl3; 2·SiCl3 → ··SiCl2 + SiCl4
(CH3)2SiCl2 → 2·CH3 + ··SiCl2
(CH3)3SiCl → 3·CH3 + ···SiCl;
2···SiCl → Si + ··SiCl2
Образование карбида кремния в данном случае происходит благодаря присутствию водорода:
··SiCl2 + H2→ Si +2HCl
·CH3 → C +3H
Si + C→ SiC
Выводы:
-
Двух стадийный процесс: 1-моноксид кремния, 2- взаим. с монооксида с остатком C;
-
Лимитирующиц процесс – 1 стадия;
-
Оставшийся диоксид взаимодействует с продуктом => снижение выхода;
-
Дисперсность исходных материалов увеличивает скорость реакции;
-
Природа исходных компонентов в большей степени определяет конечный продукт или прочие условия.
-
Химическое осаждение из газовой фазы (CVD метод) и физическое осаждение из газовой фазы (PVD метод).
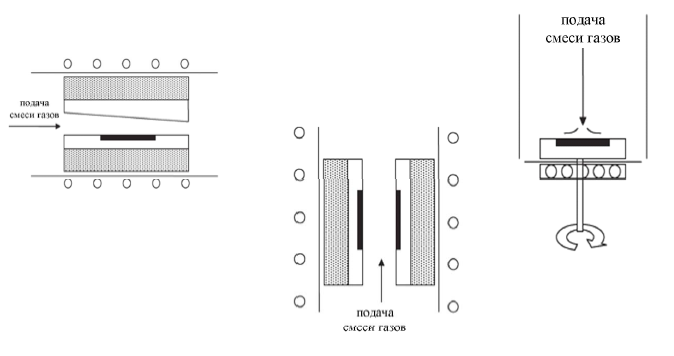
Схематическое изображение CVD реакторов:
горизонтальный реактор с горячей стенкой,
самовытяжной реактор с горячей стенкой
и вертикальный реактор с холодной стенкой
Пример:
CH3SiCl2 = CH3 + SiCl3;
2SiCl3 = SiCl2 + SiCl4
SiCl2 + H2 = Si + 2HCl
CH3 = C + 3H
Si + C = SiC
Выводы:
-
Осаждение SiC в результате разложения прекурсора на горячей подложке;
-
Область высок. температур способствует формированию кристаллических структур;
-
Низкие температуры приводят к образованию аморфных покрытий.
Прекурсоры: SiCl2; Si2Cl4; S4Cl6; SinCln+2
Физическое осаждение из газовой фазы (PVD) – синтез SiC
Ниже 2100К: 3Si + 2CO = 2SiC + SiO
Выше 2100К: обратная реакция.
Данная система, которая образуется является составом взаимодействия конденсирующих фаз и начинает взаимодействовать при 0,1 Мпа и t=2090К причем не зависит от SiC в исходном составе.
При количестве меньше 0,5 моль в системе образуется монооксид кремния и СО.
При увеличении от 0,5 моль до 4 моль в системе продуктов увеличивает Si и SiO.
Равновесный состав стремится к SiO и Si с увеличением температуры.
При t ниже 1800К: Si + 2CO = 2Cтв + SiO2 тв
1800 – 2000 К: Siтв + 2CO2 = 0,67 SiCтв + 0,33 SiO2 тв + 1,33 CO
2000 K: Si + 2CO2 = 0,5SiC + 1,5CO2 + 0,5SiO
При 1600-1800 при SiC > 0,5 моль происходит взаимодействие Si(г) и СО приводит к Si2С и SiC2 летучих кластеров.
Удельное мольное содержание кластеров примерно равно давлению на поверхности.
При SiC > n моль остается избыток.