
Семестр 1 / 112_О-2Б12_Бочкарев В.Д
..docxМинистерство образования и науки Российской Федерации
Федеральное государственное автономное образовательное учреждение высшего образования
«Национальный исследовательский Томский политехнический Университет»

Центр цифровых
образовательных технологий
15.03.01 «Нефтегазовое дело»
Индивидуальное домашнее задание
№1
Вариант – (112)
по дисциплине:
Химия 1.6
Исполнитель:
|
|
||||
студент группы |
О-2Б12 |
|
Бочкарев Вячеслав Дмитриевич |
|
27.12.2021 |
|
|
|
|
|
|
Руководитель:
|
|
||||
преподаватель |
|
|
Вайтулевич Елена Анатольевна |
|
|
|
|
|
|
|
|
Томск - 2021
Практическое задание 1. Основные химические понятия и законы.
Некоторый газ массой 2,5 г занимает при н. у. объем 2 л. Чему равны: а) молекулярная масса газа; б) молярная масса; в) абсолютная масса одной молекулы этого газа?
Напишите названия данных веществ и их структурные формулы: Cr2 O3, Be(OH)2, HMnO4, MgSO4, CuCl2, Ca(HCO3)2.
Как вывести формулу ангидрида данной кислоты? Показать на примере кислот Н2SiO3, Н3РО4, HClO4, H2CrO4.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Sb → SbCl2 →SbOHCl → Sb(OH)2 →Sb(NO3)2
Решение:
Уравнение Менделеева-Клапейрона
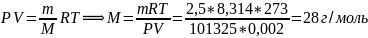 или
Молярная масса. Молярная масса =
молекулярной массе или 28 у.е., абсолютная
масса одной молекулы
или
Молярная масса. Молярная масса =
молекулярной массе или 28 у.е., абсолютная
масса одной молекулы
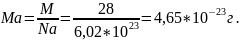 ,
где Na
это число Авагадро.
,
где Na
это число Авагадро.
Cr2
O3
– Оксид хрома III ![]()
Be(OH)2
– Гидроксид
берилия
![]()
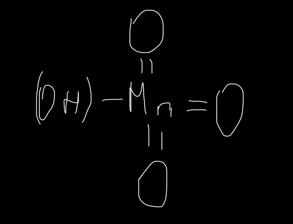
HMnO4 – Марганцевая кислота
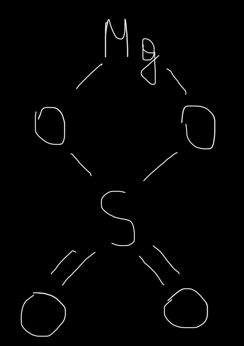
MgSO4 – Сульфат магния
![]()
C uCl2
– Хлорид меди II
uCl2
– Хлорид меди II
Ca(HCO3)2 – Гидрокарбонат кальция
Н2SiO3 = H2O + SiO2
2Н3РО4 = 3H2O + P2O5
2HClO4 = H2O + Cl2O7
H2CrO4 = H2O + CrO3
Реакции невозможны, так как сурьма имеет степени окислени в соединениях -3, +3, 5.
