
Семестр 1 / 422_О-2Б12_Бочкарев В.Д
..docxМинистерство образования и науки Российской Федерации
Федеральное государственное автономное образовательное учреждение высшего образования
«Национальный исследовательский Томский политехнический Университет»

Центр цифровых
образовательных технологий
«Нефтегазовое дело»
Индивидуальное домашнее задание
№ 4
Вариант – 422
по дисциплине:
Химия 1.6
Исполнитель:
|
|
||||
студент группы |
О-2Б12 |
|
Бочкарев Вячеслав Дмитриевич |
|
31.12.2021 |
|
|
|
|
|
|
Руководитель:
|
|
||||
преподаватель |
|
|
Вайтулевич Елена Анатольевна |
|
|
|
|
|
|
|
|
Томск - 2021
Практическое задание 4. Дисперсные системы и растворы.
Приведите названия шести способов выражения концентрации растворов и определение способа, который называется «массовая доля растворенного вещества». Какой объем воды и какая масса КОН потребуются для приготовления 10 л раствора с массовой долей 40 % и плотностью 1,40 кг/л?
Давление водяного пара при 80 °С равно 47375 Па, а давление пара водного раствора неэлектролита при этой же температуре равно 33310 Па. Какое количество воды приходится на 1 моль растворенного вещества в этом растворе?
Для всех данных веществ написать упрощенные уравнения электролитической диссоциации и выражения для расчета константы диссоциации; для одного из веществ (по выбору) напишите полное уравнение диссоциации: K2SO4, Ca(OH)2, Н3PO4, КНСО3, Fe(OH)Cl2, Zn(OH)2.
Произведение растворимости карбоната серебра (I) равно 6,15·10–12. Определите растворимость этого вещества, ответ выразить в моль/л и в виде коэффициента растворимости.
Решение:
Массовая доля (процентная концентрация) () – отношение массы растворенного вещества к общей массе раствора (%).
Мольная доля (), Молярная концентрация или молярность (СМ или М), Молярная концентрация эквивалентов или нормальность (СЭК или Н), Титр (Т), Моляльная концентрация или моляльность (Сm).
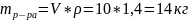
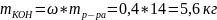
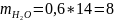
Но, т.к. плотность воды 1 кг/л, то V=8,6 л
Найдем мольную концентрацию
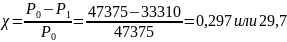 %,
тогда на 1 моль вещества придется 3 моль
растворителя.
%,
тогда на 1 моль вещества придется 3 моль
растворителя.
а) K2SO4=2K++SO42-;
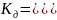
б)
Ca(OH)2=Ca2++2(OH)-;
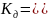
в) H3PO4=H2PO4-+H+;
H2PO4-=HPO42-+H+;
HPO42-=PO43-+H+;
г) KHCO3=K++H++CO32-;
д) Fe(OH)Cl2=Fe3++(OH)-+2Cl-;
е) Zn(OH)2=Zn2++2(OH)-;
Растворимость
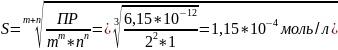
K=S/M(H2O)=1,15*10-4(моль/л)/55,6(моль/л)=2,07*10-4%
