
- •7.2. Окисление
- •Окисление
- •Основные способы
- •7.2.1. Окисление активным хлором
- •Основная область применения
- •При введении в воду хлора происходит его гидролиз, в результате которого образуются хлорноватистая
- •Концентрации хлорноватистой кислоты и гипохлорит – иона в воде при различных значениях рН
- •Окисление цианидов хлором
- •Расход реагентов на окисление цианидов
- •Окисление цианидов диоксидом хлора
- •Окисление сульфидов
- •7.5.2. Окисление кислородом воздуха
- •Последовательные стадии окисления сульфидной гидросульфидной серы
- •Принципиальная схема установки по окислению сульфидов кислородом воздуха
- •7.2.3. Окисление сульфидных соединений диоксидом углерода
- •Схемы реакций
- •7.2.4. Окисление озоном
- •Принципиальная схема установки озонирования сточных вод
- •Основные способы ввода озона в сточную воду
- •Основы расчета реакционных камер барботажного типа
- •Основные типы барботажных реакционных камер (колонн)
- •Общая площадь распыливающих элементов
- •Необходимое количество озона
- •Характеристики генераторов озона
- •Окисление сероводорода
- •Окисление цианидов
- •Обезвреживание шестивалентного хрома гидросульфитом натрия
7.2. Окисление
Окисление
Окисление - химическая реакция, при которой происходит отнятие электронов от атомов или ионов.
Область применения:
•обработка вод, содержащих токсичные примеси или соединения, которые нецелесообразно извлекать из воды;
•обработка вод, которые нецелесообразно очищать другими методами.
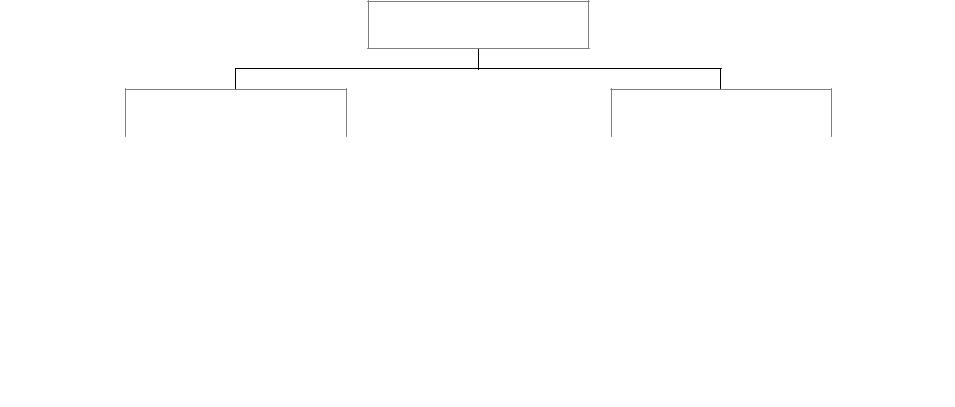
Основные способы
О К И С Л Е Н И Е
Р Е А Г Е Н Т Н О Е |
Б Е З Р Е А Г Е Н Т Н О Е |
|
|
|
|
|
|
|
|
|
|
|
|
|
О К И С Л Е Н И Е |
|
|
О К И С Л Е Н И Е |
|
Э Л Е К Т Р О Х И М И Ч Е С К О Е |
|
|
Р А Д И А Ц И О Н Н О Е |
||||
А К Т И В Н Ы М |
|
|
К И С Л О Р О Д О М |
|
О К И С Л Е Н И Е |
|
|
О К И С Л Е Н И Е |
||||
|
|
|
|
|||||||||
Х Л О Р О М |
|
|
В О З Д У Х А |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О К И С Л Е Н И Е |
|
|
О К И С Л Е Н И Е |
|
|
|
|
|
|
|
||
Д Ы М О В Ы М И |
|
|
О З О Н О М |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
Г А З А М И |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7.2.1. Окисление активным хлором
Основная область применения
Наиболее распространенный способ очистки природных и сточных вод от ядовитых цианидов, а также от органических и неорганических соединений – таких, как сероводород, гидросульфиды, сульфиды,метилмеркаптан и др.
При введении в воду хлора происходит его гидролиз, в результате которого образуются хлорноватистая (HOCl) и соляная (HCl) кислоты. При чем, в сильнокислой среде (рН < 4) в воде присутствует молекулярный хлор, при более высоких значениях рН молекулярный хлор отсутствует. Образующаяся в результате гидролиза хлорноватистая кислота диссоциирует на ион гипохлорита (OCl-) и ион водорода (Н+).
Гипохлориты кальция и натрия, а также хлорная известь гидролизуясь в воде, образуют хлорноватистую кислоту и ион гипохлорита. Соотношение между их количествами также зависит от величины рН.
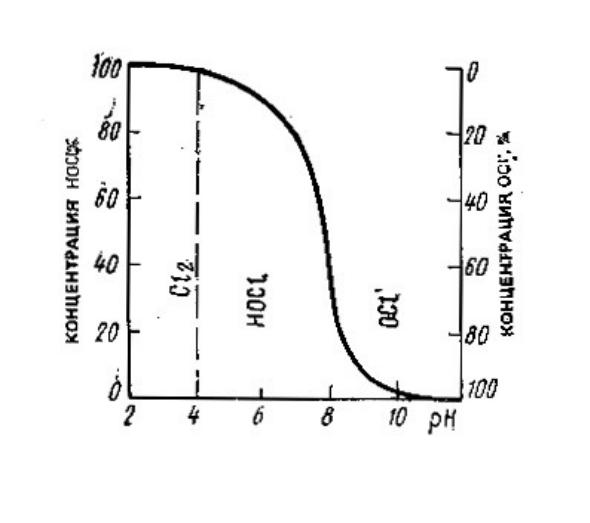
Концентрации хлорноватистой кислоты и гипохлорит – иона в воде при различных значениях рН
Окисление цианидов хлором
Окисление при рН 10
СN 2OH Cl2 CNO 2Cl H2O
Окисление цианатов
2СNO 4OH 3Cl2 2CO2 6Cl N2 2H2O
Окисление при рН 10 (прямое хлорирование цианидов)
CN Cl2 CNCl Cl
Окисление цианидов гипохлоритами или хлорной известью
СN OCl CNO Cl
Расход реагентов на окисление цианидов
XkxQ10a
x nC
Окисление цианидов диоксидом хлора
CN 2ClO2 2OH CNO 2ClO2 H2O
