- •7.2. Окисление
- •Окисление
- •Основные способы
- •7.2.1. Окисление активным хлором
- •Основная область применения
- •При введении в воду хлора происходит его гидролиз, в результате которого образуются хлорноватистая
- •Концентрации хлорноватистой кислоты и гипохлорит – иона в воде при различных значениях рН
- •Окисление цианидов хлором
- •Расход реагентов на окисление цианидов
- •Окисление цианидов диоксидом хлора
- •Окисление сульфидов
- •7.5.2. Окисление кислородом воздуха
- •Последовательные стадии окисления сульфидной гидросульфидной серы
- •Принципиальная схема установки по окислению сульфидов кислородом воздуха
- •7.2.3. Окисление сульфидных соединений диоксидом углерода
- •Схемы реакций
- •7.2.4. Окисление озоном
- •Принципиальная схема установки озонирования сточных вод
- •Основные способы ввода озона в сточную воду
- •Основы расчета реакционных камер барботажного типа
- •Основные типы барботажных реакционных камер (колонн)
- •Общая площадь распыливающих элементов
- •Необходимое количество озона
- •Характеристики генераторов озона
- •Окисление сероводорода
- •Окисление цианидов
- •Обезвреживание шестивалентного хрома гидросульфитом натрия
Окисление сульфидов
В щелочной среде
Na2S 4Cl2 8NaOH Na2SO4 8NaCl 4H2O
В кислой и нейтральной среде
H2S 3Cl2 3H2O H2SO3 6HCl
NaHS 3Cl2 3H2O NaHSO3 6HCl
7.5.2. Окисление кислородом воздуха
Последовательные стадии окисления сульфидной гидросульфидной серы
S2 S SnO62 S2O32 SO32 SO42
В процессе окисления сера изменяет свою валентность от –2 до +6.
При окислении сероводорода, гидросульфида и сульфида в нейтральной и щелочной среде (рН = 7…13,75) основным продуктом реакции является тиосульфат.
Окисление при рН = 9…9,5
2HS 2O2 S2O32 H2O
2HS 3O2 2OH 2S2O32 2H2O
2HS 4O2 2OH 2S2O32 2H2O
рН сточной воды повышается.
Окисление при рН = 12,15…12,75
|
2HS |
2O S O2 |
H O |
|||||||
|
|
|
|
2 |
|
2 |
3 |
|
2 |
|
2S2 2O H O 2S O |
2 |
2OH |
||||||||
|
|
2 |
|
2 |
|
|
2 |
3 |
|
|
2HS |
3O 2OH |
2SO2 |
2H O |
|||||||
|
|
2 |
|
|
|
|
|
3 |
2 |
|
|
|
2S2 |
3O 2SO2 |
|
||||||
|
|
|
|
2 |
|
|
|
3 |
|
|
HS |
2O OH SO2 |
H O |
||||||||
|
|
|
2 |
|
|
|
|
4 |
2 |
|
|
|
S2 |
2O |
|
SO2 |
|
|
|||
|
|
|
|
2 |
|
|
4 |
|
|
|
При окислении гидросульфида и сульфида до тиосульфита величина рН раствора повышается, при окислении гидросульфида до сульфита и сульфата – рН понижается,при окислении сульфида до сульфита и сульфата – рН не изменяется.
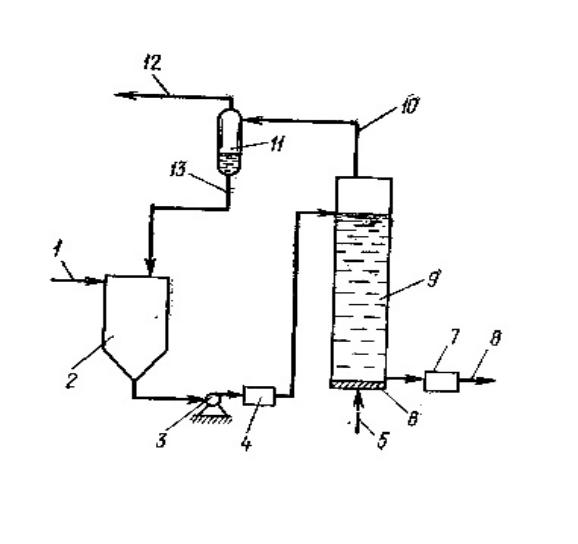
Принципиальная схема установки по окислению сульфидов кислородом воздуха
7.2.3. Окисление сульфидных соединений диоксидом углерода
Схемы реакций
Na2S CO2 H2O Na2CO3 H2S
2NaHS CO2 H2O Na2CO3 2H2S
7.2.4. Окисление озоном