
- •Оглавление
- •Предисловие
- •Глава 1. Исторический очерк
- •Глава 2. Возбудитель туберкулеза
- •Глава 3. Патогенез и патологическая анатомия туберкулеза
- •3.2 Клинически выраженный туберкулез
- •3.3 Морфология локальных изменений
- •Глава 4. Эпидемиология туберкулеза
- •Глава 5. Анатомо-физиологические сведения об органах дыхания
- •5.1 Гортань
- •5.2 Грудная стенка
- •5.3 Плевра
- •5.4 Легкие и бронхи
- •5.5 Легочные и бронхиальные артерии
- •5.6 Лимфатическая система легких
- •Глава 6. Методы обследования больных туберкулезом
- •6.1 основные симптомы
- •6.2 Расспрос, физикальные методы
- •6.3 Туберкулинодиагностика
- •6.4 Микробиологические исследования
- •6.5 Методы лучевой диагностики
- •6.6 Эндоскопия
- •6.8 Биопсия плевры, легких и лимфатических узлов
- •6.9 Исследование крови и мочи
- •6.10 Оценка функций дыхания и кровообращения
- •Глава 7. Классификация туберкулеза
- •Глава 8. Первичный туберкулез
- •Глава 9. Диссеминированный туберкулез легких
- •Глава 10. Очаговый туберкулез легких
- •Глава 11. Инфильтративный туберкулез легких
- •Глава 12. Казеозная пневмония
- •Глава 13. Туберкулема легких
- •Глава 14. Кавернозный и фиброзно-кавернозный туберкулез легких
- •Глава 15. Цирротический туберкулез легких
- •Глава 16. Туберкулезный плеврит
- •Глава 17. Туберкулез гортани, трахеи и бронхов
- •Глава 18. Туберкулез легких в сочетании с другими заболеваниями
- •18.1 Туберкулез у ВИЧ-инфицированных и больных синдромом приобретенного иммунодефицита
- •18.2 Туберкулез легких и пневмокониозы
- •18.3 Туберкулез и хронические неспецифические болезни органов дыхания
- •18.4 Туберкулез и сахарный диабет
- •18.6 Туберкулез и алкоголизм
- •18.7 Туберкулез и психические заболевания
- •18.8 Туберкулез и рак
- •Глава 19. Туберкулез и материнство
- •20.1 Туберкулез центральной нервной системы
- •20.3 Туберкулез почек и мочевыводящих путей
- •20.4 Туберкулез мужских половых органов
- •20.5 Туберкулез женских половых органов
- •20.6 Туберкулез периферических лимфатических узлов
- •20.7 Туберкулез брыжеечных лимфатических узлов
- •20.9 Туберкулез кишечника
- •20.10 Туберкулез глаз
- •20.11 Туберкулез кожи
- •Глава 21. Профилактика туберкулеза
- •21.1 Социальная профилактика
- •21.2 Санитарная профилактика
- •21.3 Специфическая профилактика туберкулеза
- •Глава 22. Выявление больных туберкулезом и верификация диагноза
- •22.1 Раннее, своевременное и позднее выявление больных туберкулезом
- •22.2 Организация выявления больных туберкулезом
- •22.3 Обследование на туберкулез и верификация диагноза
- •Глава 23. Лечение больных туберкулезом
- •23.1 Химиотерапия
- •23.1.1 Противотуберкулезные химиопрепараты
- •23.1.3 Профилактика и устранение побочных реакций
- •23.2 Хирургическое лечение туберкулеза легких
- •23.3 Искусственный пневмоторакс и пневмоперитонеум
- •23.4 Патогенетическая и симптоматическая терапия
- •Глава 24. Неотложные состояния при туберкулезе легких
- •24.1 Легочное кровотечение
- •24.2 Спонтанный пневмоторакс
- •24.3 Острое легочное сердце
- •Глава 25. Организация противотуберкулезной работы в России
- •25.1 Роль общей лечебно-профилактической сети
- •25.2 Специализированная противотуберкулезная служба
- •25.3 Государственный санитарно-эпидемиологический надзор
- •25.4 Международное сотрудничество
- •Декларация VII российского съезда фтизиатров 5 июня 2003 г., Москва

шений в иммунном балансе появляется реальная угроза акти вации сохранившейся микобактериальной популяции и забо левания туберкулезом.
Антимикобактериальная эффекторная функция макрофа гов варьирует в зависимости от генетической структуры чело века, его возраста, пола, гормонального фона, наличия или отсутствия сопутствующих заболеваний. Она зависит также от вирулентности МБТ.
Допускают, что особенности генетической структуры чело века детерминируют функциональную активность макрофа гов, Т- и В-лимфоцитов и тем самым способствуют развитию клеточного иммунитета или сдерживают его. Установлена ас социация заболевания туберкулезом с наличием в генотипе человека определенных аллелей — HLA А11-В15 и HLA DR-2. Эти аллели рассматривают как генетические маркеры повы шенной восприимчивости к возбудителю туберкулеза.
Приобретенный иммунитет снижается при СПИДе, сахар ном диабете, язвенной болезни, злоупотреблении алкого лем, длительном применении наркотиков. Противотубер кулезный иммунитет ослабевает при голодании, стрессовых ситуациях, беременности, лечении гормонами или иммунодепрессантами.
Для защиты от возбудителя туберкулеза определенное зна чение имеют гуморальные факторы естественной резистент ности (комплемент, лизоцим, пропердин, интерферон и др.). Они приобретают существенное значение у новорожденных детей, имеющих физиологическую недостаточность иммунной системы и неспособных к формированию клеточного имму нитета. У взрослых этим факторам защиты от МБТ принадле жит второстепенная роль.
В целом риск развития туберкулеза у впервые инфициро ванного человека составляет около 8 % в первые 2 года по сле заражения, в последующие годы он постепенно снижа ется.
3.2. Клинически выраженный туберкулез
Недостаточная активация макрофагов и неэффективный фагоцитоз приводят к неконтролируемому размножению про никших в организм микобактерий и увеличению микобакте риальной популяции в геометрической прогрессии. В течение 20 дней может появиться более 500 млн новых МБТ. Их взаи модействие с полинуклеарными лейкоцитами и макрофагами приводит к массовой гибели фагоцитирующих клеток. При этом в межклеточное пространство поступает большое коли-
46

чество медиаторов и протеолитических ферментов, повреж дающих прилежащие ткани. Следствием является своеобраз ное «разжижение» тканей с формированием особой питатель ной среды, способствующей росту и размножению располо женных внеклеточно микобактерий.
Большая интенсивно размножающаяся популяция мико бактерий индуцирует дисбаланс в иммунной защите: количе ство Т-супрессоров (CD8+) увеличивается, иммунологическая активность Т-хелперов (CD4+) уменьшается, наступает резкое усиление, а затем угнетение ПЧЗТ к антигенам МБТ. Воз можности организма для локализации и отграничения возбу дителя туберкулеза ухудшаются. Воспалительная реакция при обретает распространенный характер. Возникают выраженные нарушения микроциркуляции с повышением проницаемости сосудистой стенки и поступлением в ткани белков плазмы, лейкоцитов и моноцитов. В формирующихся туберкулезных гранулемах преобладает казеозный некроз, их клеточная со ставляющая выражена слабо. Инфильтрация наружного слоя полинуклеарными лейкоцитами, макрофагами и лимфоидными клетками усиливается. Отдельные гранулемы сливаются, общий объем туберкулезного поражения увеличивается. Изме няется биологическая суть происходящего процесса — первич ное инфицирование трансформируется в клинически выраженный туберкулез.
3.3. Морфология локальных изменений
Тканевая реакция в месте локализации МБТ первоначаль но имеет неспецифический характер. Такая реакция наблюда ется в тканях независимо от вида возбудителя. Происходят нарушения микроциркуляции, повышение проницаемости со судистой стенки, локальный отек тканей, инфильтрация зоны поражения лейкоцитами, моноцитами и другими форменны ми элементами крови. Первые специфические морфологиче ские признаки туберкулезного воспаления появляются позд нее, через 2—3 нед после инфицирования МБТ.
Специфическое воспаление. Развитие специфического для туберкулеза воспаления обусловлено иммунологическими сдвигами, которые возникают при взаимодействии макроорга низма с туберкулезным возбудителем. В связи с этим специ фическую воспалительную реакцию при туберкулезе характе ризуют как классический пример воспаления на иммунной основе.
Основообразующим морфологическим элементом туберку лезного воспаления является бугорок, который чаще назы вают туберкулезной гранулемой.
47

Рис. 3.9. Туберкулезные очаги в легком. Фрагмент гистотопографического среза.
Визуализация туберкулезной гранулемы возможна при све товой микроскопии (рис. 3.9).
Важнейшей отличительной чертой туберкулезной грануле мы является наличие центрально расположенной зоны творо жистого, или казеозного, некроза — плотного аморфного тка невого детрита, образовавшегося вследствие повреждения и гибели фагоцитов. Зона казеозного некроза окружена не сколькими слоями эпителиоидных клеток, макрофагов, лим фоцитов и плазматических клеток. Среди эпителиоидных кле ток располагаются крупные многоядерные клетки Пирогова— Лангханса. В наружных отделах клеточного слоя можно уви деть полинуклеарные лейкоциты и фибробласты. Клеточные элементы, расположенные вокруг зоны казеозного некроза, образуют грануляционную ткань. В клетках, расположенных ближе к казеозно-некротическим массам, отмечаются призна ки дистрофии и деструкции.
Специфическое воспаление захватывает различные морфо логические структуры пораженного органа — клетки паренхи мы, лимфатические и кровеносные сосуды. При туберкулезе легкого в специфическую воспалительную реакцию также во влекаются бронхи.
Иммуноморфологические особенности специфического воспаления позволяют считать туберкулез гранулематозным заболеванием.
Функциональное состояние паренхиматозных клеток в зо не поражения существенно нарушается. В них отчетливо вы-
48
являются признаки дистрофии и деструкции. Резко снижается резорбтивная функция лимфатических капилляров. Возника ют повреждения эндотелия лимфатических капилляров с вы ходом лимфы в межклеточное пространство. Наблюдаются грубые нарушения микроциркуляции с тромбозом мелких кровеносных сосудов. Повреждения кровеносных сосудов обусловлены фиксацией в их базальном слое циркулирующих иммунных комплексов (ЦИК), которые в виде очаговых отло жений можно обнаружить при электронной микроскопии. Кровеносные капилляры в туберкулезной гранулеме практи чески отсутствуют. Питание клеточных элементов осуществ ляется в основном путем омывания их тканевой жидкостью.
Клеточный состав гранулемы подвержен динамическим из менениям на разных стадиях ее развития. По преобладанию того или иного типа клеточных элементов выделяют эпите- лиоидно-клеточные, лимфоидные и гигантоклеточные тубер кулезные гранулемы. В случаях преобладания зоны некроза гранулемы называют некротическими
Особенности клеточного состава гранулемы и выражен ность некротических изменений зависят от характера ткане вой реакции в зоне поражения. При продуктивной тканевой реакции в гранулеме преобладают эпителиоидные, макрофагальные, многоядерные гигантские клетки. Внешний отдел клеточного слоя содержит фибробласты, которые синтезируют коллаген. Некротические изменения в центре гранулемы вы ражены слабо, а иногда отсутствуют. Преобладание экссудативной тканевой реакции проявляется увеличением зоны нек роза. Она занимает 1/3 или 1/2 общего объема гранулемы. В клеточном слое преобладают макрофаги и лимфоидные элементы с ограниченным присутствием эпителиоидных и ги гантских клеток на границе с зоной казеозного некроза. Пре имущественно альтеративная реакция характеризуется фор мированием некротических гранулем, в которых клеточный вал выражен крайне слабо, а иногда практически отсутствует.
Преобладание экссудативной тканевой реакции свидетель ствует о прогрессировании туберкулезного воспаления. Ткань, окружающая отдельные гранулемы, пропитывается серознофибринозным экссудатом. Постепенно происходит слияние гранулем. В результате формируется туберкулезный очаг —па- тологическое образование диаметром до 1,5 см (рис. 3.10). Прогрессирование очагов проявляется расширением зоны перифокального воспаления, которое вначале может быть сероз ным, фибринозным или гнойным. Затем возникают признаки специфического воспаления — образуются новые туберкулез ные гранулемы с выраженной зоной некроза, окруженной слоем из немногочисленных эпителиоидных и единичных ги гантских клеток. Грануляционная ткань инфильтрируется макрофагами, лимфоидными элементами, а также полинук-
49

Рис. 3.10. Туберкулезный инфильтрат в легком. Фрагмент гистотопографического среза.
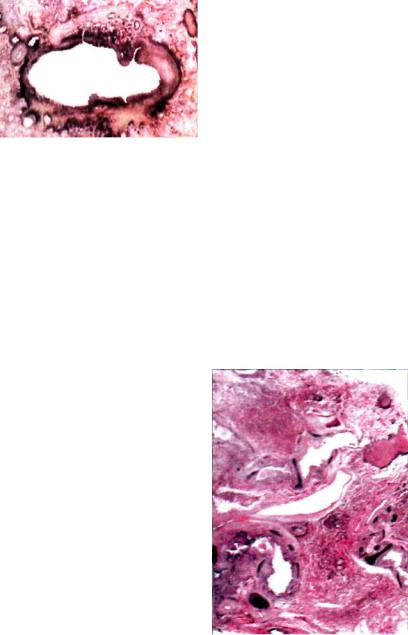
леарами. Прогрессирование процесса приводит к слиянию очагов и появлению туберкулезных инфильтратов с участками казеозного некроза (рис. 3.11). В последующем происходит инфильтрация казеозных масс полинуклеарными лейкоцита ми. Выделяемые лейкоцитами протеолитические ферменты вызывают расплавление масс казеоза. При их отторжении формируются язвы или полости распада, которые затем могут трансформироваться в каверны (рис. 3.12, 3.13). Резкое угнете ние клеточного иммунитета приводит к быстрому прогрессированию патологического процесса с возникновением некро-
Рис. 3.11. Распад в туберкулезной гранулеме. Гистологический препа рат, х 60.
50
|
тических гранулем. Довольно |
||||
|
быстро в пораженном органе |
||||
|
формируются обширные зоны |
||||
|
казеозного некроза. |
|
|||
|
Интенсивность развития |
||||
|
туберкулезного |
воспаления, |
|||
|
выраженность и смена воспа |
||||
|
лительных |
тканевых |
реак |
||
|
ций — пролиферации, экссу |
||||
|
дации и альтерации — в |
зна |
|||
Рис. 3.12. Каверна в легком. |
чительной степени зависят от |
||||
Фрагмент гистотопографическо- |
количества МБТ, попавших в |
||||
го среза. |
организм, |
и их |
вирулентно |
||
сти. В эксперименте установ |
|||||
|
|||||
|
лено, что |
туберкулезная |
гра |
||
нулема в легком животного (собаки) формируется при введе нии 10 МБТ, крупный очаг— 106, каверна — 108 микобакте рий. Экссудативная и альтеративная тканевая реакция доми нирует при увеличивающейся микобактериальной популя ции, высокой вирулентности микобактерий, повышенной чувствительности клеток к возбудителю туберкулеза в сочета нии с недостаточной эффективностью фагоцитоза. В этих ус ловиях туберкулезный процесс прогрессирует и при отсутст вии лечебных мероприятий часто приводит к летальному ис ходу.
Обратное развитие тубер кулезного воспаления в боль шинстве случаев сопровожда ется постепенным рассасыва нием экссудата, уплотнением зоны казеозного некроза и формированием вокруг тубер кулезных гранулем и очагов соединительнотканной капсу лы. В заживлении и после дующем рубцевании гранулематозных очагов большое значение имеет инфильтра ция их фибробластами, обес печивающими формирование коллагеновых волокон. По мере регрессирования патоло гического процесса они под вергаются гиалинозу. В кап суле, окружающей фиброзирующиеся туберкулезные гра нулемы и очаги, иногда мож но обнаружить скопления
Рис. 3.13. Цирротические постту беркулезные изменения легкого. Гистотопографический срез.
51

Рис. 3.14. Токсико-аллергический тромбоваскулит. Гистологический препарат. х 80.
лимфоцитов. Их появление обычно обусловлено высокой эф фективностью защитных иммунологических реакций. Расса сывание экссудата с трансформацией туберкулезных грануля ций в соединительную ткань может привести к фиброзным (цирротическим) изменениям в пораженном органе (рис. 3.14).
Отсутствие в осумкованных очагах специфической грану ляционной ткани указывает на благополучное завершение воспалительного процесса и подтверждает клиническое изле чение туберкулеза с формированием остаточных посттубер кулезных изменений. Эти изменения отличаются большим по лиморфизмом. Они могут быть представлены рубцом, инкап сулированным или кальцинированным фиброзным очагом, участком очагового или диффузного пневмофиброза. Иногда в исходе туберкулезного воспаления формируются плотные осумкованные фокусы или «санированные» полости распада. Реже наблюдаются карнификация легкого и образование бронхоэктазов.
В остаточных посттуберкулезных изменениях среди фиб розных волокон содержатся метаболически неактивные МБТ.
Остаточные посттуберкулезные изменения являются резер вуаром эндогенной туберкулезной инфекции. Они поддер живают нестерильный противотуберкулезный иммунитет, а при неблагоприятных для макроорганизма условиях созда ют угрозу повторного заболевания туберкулезом.
Инволюция туберкулезного воспаления с полным рассасы ванием патологических очагов без каких-либо остаточных из менений и полной элиминацией микобактерий из организ ма — большая редкость. Такой исход возможен при начальных
52
формах туберкулеза с малой протяженностью поражения и быстром восстановлении иммунитета, нарушенного в начале болезни.
Параспецифические тканевые реакции. Проникновение в организм МБТ нередко вызывает различные неспецифические изменения в тканях. Эти изменения этиологически обусловле ны присутствием микобактерий, однако признаков специфи ческого воспаления не имеют. В связи с этим их принято на зывать параспецифическими.
Параспецифические тканевые реакции могут развиваться в сердечно-сосудистой системе, различных паренхиматозных органах. Наиболее часто они возникают при первичном или диссеминированном туберкулезе.
Морфологические проявления параспецифических реакций представлены токсико-аллергическим тромбоваскулитом, а также периваскулярными узелковыми или диффузными ин фильтратами из мононуклеарных макрофагов, лимфоцитов и плазматических клеток. Наиболее выражены такие изменения в лимфатических узлах.
Специальные исследования позволили установить связь параспецифических изменений с реакциями иммунитета. Так, в образующихся при туберкулезе лимфоидных узелках и гистиоцитарных инфильтратах удалось обнаружить антигены МБТ и противотуберкулезные антитела.
Параспецифические реакции при туберкулезе впервые от метили патологоанатомы, которые характеризовали их как «маски» первичного туберкулеза. В зависимости от локализа ции параспецифических изменений были выделены сердечно сосудистая, эндокринная, нервно-дистрофическая, суставная, желудочно-кишечная «маски» заболевания.
При своевременной диагностике туберкулеза и адекватном лечении параспецифические изменения довольно быстро под вергаются обратному развитию без каких-либо остаточных из менений. При отсутствии лечения в зоне параспецифических изменений со временем могут возникнуть поражения специ фического характера.
Выделение в течении туберкулеза двух последовательных периодов — первичного и вторичного — находит отражение и в особенностях патоморфологической картины.
Первичный туберкулез всегда вовлекает в патологический процесс лимфатическую систему. Частичный или тотальный казеозный некроз лимфатических узлов — важнейшая черта первичного туберкулеза. Наличие обширной перифокальной воспалительной реакции вокруг основного очага — также важ ная отличительная особенность первичного туберкулеза. При легочном поражении первичный легочный аффект обычно локализован в хорошо вентилируемых отделах, т. е. в средних и нижних долях легкого. В результате бактериемии, характер-
53

ной для первичного периода туберкулезной инфекции, в лег ких и других органах формируются гематогенные очаги-отсе вы. Нередко возникают распространенные параспецифические реакции. Остаточные посттуберкулезные изменения при первичном туберкулезе формируются медленно. Они посте пенно обызвествляются, иногда подвергаются оссификации.
Вторичный туберкулез развивается на фоне сформировав шихся в процессе первичного периода туберкулезной инфек ции остаточных туберкулезных изменений (кальцинирован ные лимфатические узлы и очаги во внутренних органах). При вторичном туберкулезе специфический воспалительный процесс возникает на фоне ослабленного противотуберкулез ного иммунитета. В связи с этим наклонность к генерализа ции патологического процесса отсутствует. Регионарные лим фатические узлы в патологический процесс не вовлекаются. Туберкулезное поражение обычно имеет органный характер с образованием очага, инфильтрата, каверны. В развитии вто ричного туберкулеза большое значение имеет бронхогенный путь распространения МБТ. В большинстве случаев вторич ный туберкулез поражает легкое, в основном верхние и задние его отделы. В сформировавшихся в исходе вторичного тубер кулеза остаточных изменениях обычно отсутствуют признаки кальцинации или оссификации.
Послепервичные формы туберкулеза возникают при гемато генной или лимфогенной диссеминации МБТ. Во многих внутренних органах формируются множественные туберкулез ные очаги. Образование очагов происходит на фоне преобла дания продуктивной тканевой реакции. Развиваются диффуз ные васкулиты и лимфангиты, которые создают морфологиче скую основу для последующего интерстициального сетчатого фиброза. При прогрессирующем течении диссеминированный туберкулез теряет характерную для него особенность распро странения гематогенным и лимфогенным путем и приобретает черты вторичного туберкулеза.
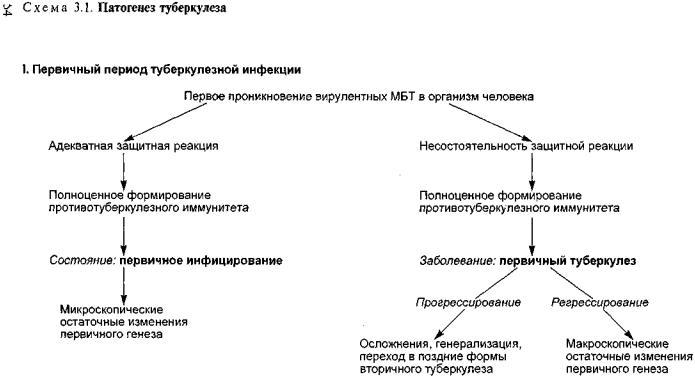
Патогенез туберкулеза представлен на схеме 3.1.
