
- •Абсорбционная спектроскопия в
- •Спектроскопия — разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения (в
- •Электромагнитный спектр
- •Закон Бера-Бугера-Ламберта
- •• Условия применения закона Бугера- Ламберта-
- ••Закон аддитивности
- •Схема энергетических состояний двухатомной молекулы
- •Способы изображения электронных спектров
- •Вид полосы поглощения
- •Характеристики спектра поглощения
- •Энергия
- •Типы молекулярных
- •Классификация полос поглощения.
- •Взаимосвязь электронных спектров и
- •Основные хромофорные группы
- •Взаимосвязь электронных спектров и структуры органических молекул
- •Типы смещений полосы поглощения в УФ-спектре
- •Изменение спектральных характеристик систем с сопряженными связями
- •Механизм возникновения гипсо- и батохромных сдвигов в электронных спектрах
- •Синее смещение полосы поглощения (n → π* переход) карбонильной группы в следующем ряду
- •Гипсохромный и батохромный сдвиги для n → π*
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Электронные спектры поглощения основных классов органических
- •Вид спектра монозамещенных бензола
- ••Количественный спектральный анализ
- •Нефелометрический и турбидиметрический анализ
- •В нефелометрическом и турбидиметрическом анализе используется явление рассеяния света твердыми частицами, находящимися в
- ••Метод с измерением интенсивности рассеянного света под углом 90о (или каким- либо другим)
- •Применение методов, основанных на
Абсорбционная спектроскопия в
видимой и УФ области
Молекулярная спектроскопия
Спектроскопия — разделы физики и аналитической химии, посвящённые изучению спектров взаимодействия излучения (в том числе, электромагнитного излучения, акустических волн и др.)
•Атомный и молекулярный спектральные анализы позволяют определять элементный и молекулярный состав вещества, соответственно. В эмиссионном и абсорбционном методах состав определяется по спектрам испускания и поглощения.
• M* → M + hν |
(эмиссия) |
• M + hν → M* |
(абсорбция) |
Электромагнитный спектр
Излучение |
λ, нм |
Е, эв |
γ-Лучи |
0.1-10-4 |
~ 107 |
Рентгеновские |
10-10-2 |
~ 105 |
лучи |
|
|
Ультрафиолетовое |
10-400 |
~ 10 |
Видимый свет |
400-760 |
|
Инфракрасное |
760- 106 |
~ 10-1 |
Микроволновое |
10-3- 1м |
~ 10-3 |
или СВЧ |
|
|
Радиоволны |
> 1м |
~ 10-6 |
Процессы, происходящие при поглощении или излучении
Изменения в энергетичес-ком состоянии ядер (спект-роскопия γ-резонанса)
Изменения в энергетичес-ком состоянии внутренних электронов атомов (рентгеноспектроскопия)
Изменение энергетического состояния внешних элект-ронов (электронная спектроскопия)
Колебание атомов в молекуле (ИК- спектроскопия)
Колебание атомов в кристаллической решетке; изменение вращательного энергетического состояния (ЭПР)
Изменение энергетического состояния спинов ядер и электронов (спектроскопия ЯМР и ОЖЕ-спектроскопия)
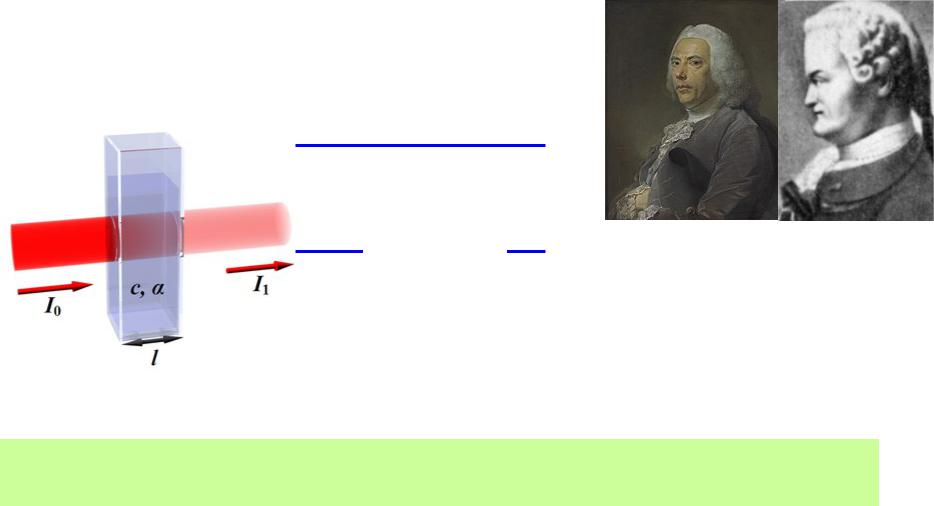
Закон Бера-Бугера-Ламберта
Экспериментально открыт П. Бугером (1729), теоретически выведен И.Г. Ламбертом (1760), для растворов
|
(1852) |
|
|
|
|
|
|
lg (I0/I) = |
|
|
|
||
|
alc |
|
|
|
|
|
|
А = |
|
|
П. Бугер |
И.Г. Ламбер |
|
|
|
|
||||
|
|
lc |
|
|
|
|
а - коэффициент поглощения, константа, за |
||||||
от , но не зависящая от концентрации; |
||||||
l - длина оптического пути; |
|
|||||
ис [моль/л], l[см] ,ca-=концентрация
- молярный коэффициент
Величина молярного коэффициента поглощения пропорциональна вероятности определенного перехода
А = lg |
А – погашение |
I=I0 10 |
-εlc |
(I / I) |
плотность ) |
|
|
|
(оптическая |
|
|
0 |
Т - |
|
|
Т = I/I0 |
пропускание |
|
|
• Условия применения закона Бугера- Ламберта-
Бера
1.Закон справедлив для монохроматического света не слишком большой интенсивности Аλ=ελ lc
2.Пучек света должен быть параллельным 3.Закон справедлив для не слишком
концентрированных растворов ε= f(n)
4.Температура должна быть постоянной в пределах 1-2 градусов
5. Закон соблюдается для систем, где поглощающими центрами являются частицы одного сорта
Cr2O2-7 + H2O = 2HCrO-4 = 2CrO42- + 2H+
Различие в εCr2O2-7 εCrO2-4
•Закон аддитивности
•Поглощение света каким либо веществом не
зависит от присутствия в растворе других веществ, как поглощающих свет, так и не
поглощающих. A=A1 + A2 +…An
•оптическая плотность смеси веществ равна сумме оптических плотностей каждого из них (при условии подчинения закону Бугера
– Ламберта – Бера). Для одной и той же длины волны и толщины слоя для смеси веществ
•A = ε1 ∙l1 ∙c1 + ε2 ∙l2 ∙c2 + …εn ∙ln
∙cn
|
непосредственному измерению оптической |
|
плотности может быть проведен для веществ, |
|
обладающих лишь определенными |
|
особенностями строения(ароматические |
|
соединения, соединения с сопряженными |
|
кратными связями, соединения ряда металлов |
• |
др.) |
Е = Еэл + Екол + Евр |
|
• |
Еэл:Екол:Евр= 1000:100:1 |
• |
Евр = 0,125 -1,25 кДж/моль |
• |
Екол + Евр = 1,25-50 |
|
кДж/моль |
• |
Еэл + Екол + Евр = 60-600 |
|
кДж/моль |
• |
∆Е = Е1 – Е0 |
• |
∆Е =h = hc/λ |
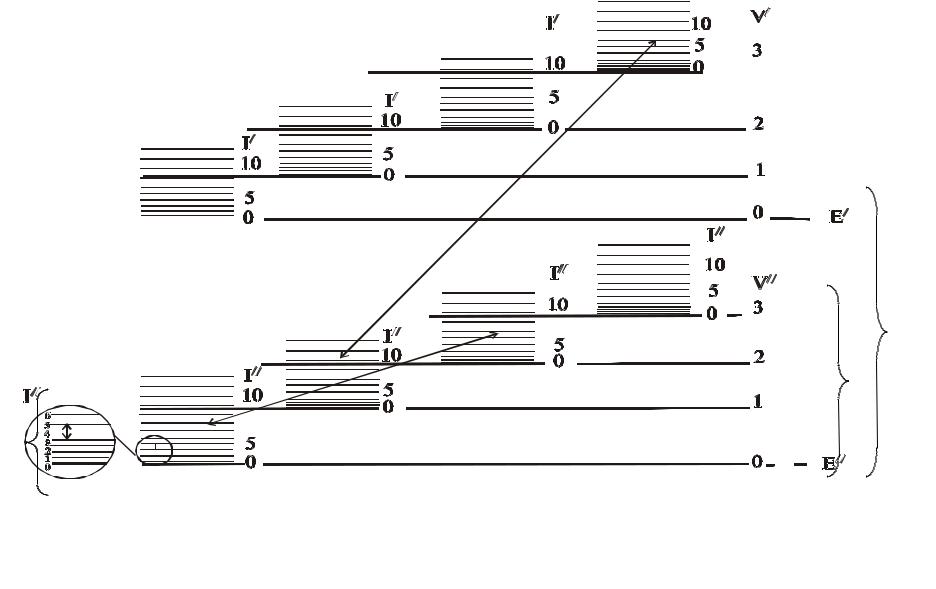
Схема энергетических состояний двухатомной молекулы
Ее
Еv
Еr
Схема энергетических состояний двухатомной молекулы: Ее – различные электронные состояния; Еv –
различные колебательные состояния; Еr – различные вращательные состояния; νе.v.r – переходы, соответствующие электронно-колебательно-вращательному спектру; νv.r – переходы, соответствующие колебательно-вращательному спектру; νr – переходы, соответствующие вращательному спектру

Способы изображения электронных спектров
Электронные спектры поглощения записываются в виде зависимости поглощения от длины волны (Ǻ , нм) или
частотыВеличина(смпоглощения-1) может быть выражена:
процентом поглощения [(I0 – I)/ I0 · 100% ], процентом пропускания [(I/I0) ·
100%], оптической плотностью D ,
коэффициентом молярного поглощения
Область поглощения называется
полосой; совокупность полос (ε) или его логарифмом (lgε)
поглощения-спектр ее поглощения. Спектр – это последовательность квантов энергии электромагнитных колебаний, поглощенных, выделившихся или рассеянных
при многочисленных переходах атомов или молекул из одних
энергетических состояний в

