
- •Физико-химические методы исследования биологически активных веществ
- •Лекция №2
- •Закон Бера-Бугера-Ламберта
- •Способы изображения электронных спектров
- •Водный раствор комплекса мальтола и железа (III) (FeMa3 (III), 12.8 мг/л)
- •Взаимосвязь электронных спектров и структуры органических молекул
- •Гипсохромный сдвиг
- •диэтиловыйводметэтанолгекснолэфир
- •Взаимосвязь электронных спектров и структуры органических молекул
- •Основные хромофорные группы
- •Электронные спектры поглощения основных классов органических соединений
- •Электронные спектры поглощения основных классов органических соединений
- •2 двойные связи (1,4) в
- •Электронные спектры поглощения основных классов органических соединений
- •Электронные спектры поглощения основных классов органических соединений
Физико-химические методы исследования биологически активных веществ
Лекция №2
•Электронная, или УФ-спектроскопия
–Закон Бера-Бугера-Ламберта
–Способы изображения электронных спектров
–Взаимосвязь электронных спектров и структуры органических молекул. Хромофоры и ауксохромы.
–Классификация полос поглощения
–Влияние различных факторов на электронные спектры поглощения
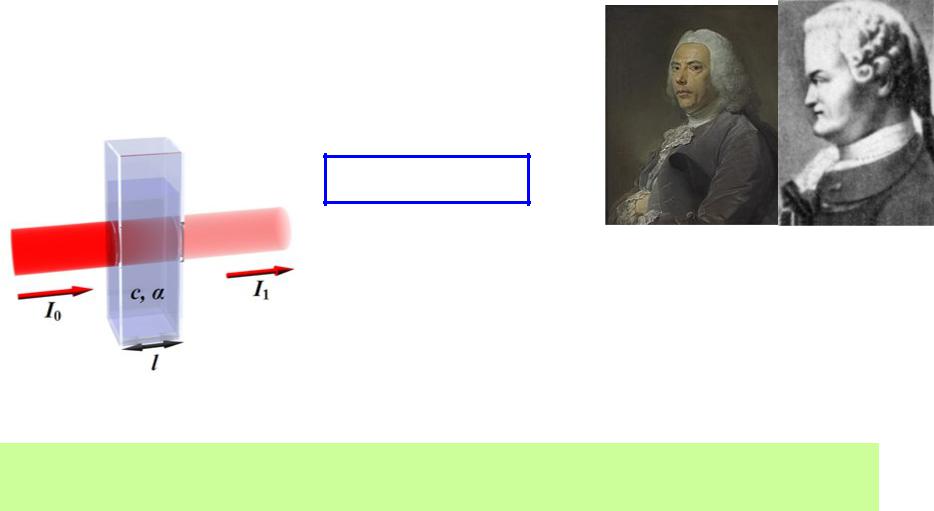
Закон Бера-Бугера-Ламберта
Экспериментально открыт П. Бугером (1729), теоретически выведен И.Г. Ламбертом (1760), для растворов исследован А. Бером (1852)
lg (I0/I) = alc
А = lc |
П. Бугер |
И.Г. Ламберт |
|
|
|
а- коэффициент поглощения, константа, зависящая от
, но не зависящая от концентрации;
1. l - длина оптического пути; c - концентрация
При с [моль/л], b[см] , a = |
- молярный коэффициент поглощения |
Величина молярного коэффициента поглощения пропорциональна вероятности определенного перехода
А = lg (I0/ I) |
А – погашение |
Т = I/I0 |
(оптическая плотность D) |
А = - lgТ |
Т - пропускание |
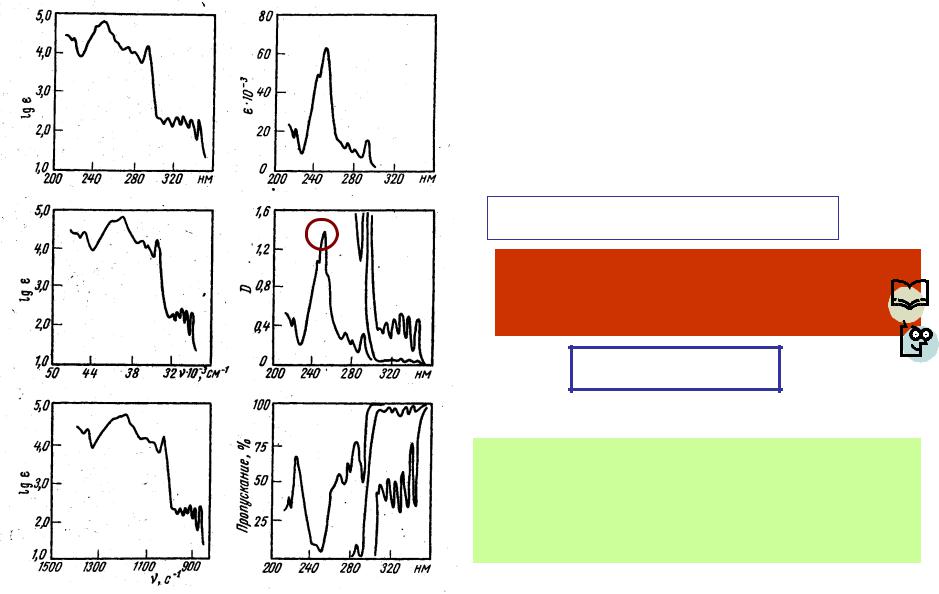
Способы изображения электронных спектров
Электронные спектры поглощения записываются в виде зависимости поглощения от длины волны (Ǻ , нм) или частоты (см-1)
Величина поглощения может быть выражена:
процентом поглощения [(I0 – I)/ I0 · 100% ], процентом пропускания [(I/I0) · 100%],
оптической плотностью D , коэффициентом молярного поглощения (ε)
или его логарифмом (lgε)
максгексан = 235 нм ( 5400).
Области поглощения растворителей, наиболее часто используемых в 
 УФ-спектроскопии
УФ-спектроскопии 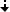
А = 0,2 до 0,7.
сведения о концентрации раствора и толщине кюветы всегда должны сопровождать выдаваемый прибором спектр А = f(λ)
Водный раствор комплекса мальтола и железа (III) (FeMa3 (III), 12.8 мг/л)
O
OH
3-гидрокси-2-метил-4Н-пиран-4-он (мальтол)
O
Взаимосвязь электронных спектров и структуры органических молекул
Для характеристики спектральных изменений, вызванных модификацией структуры, введены специальные термины:
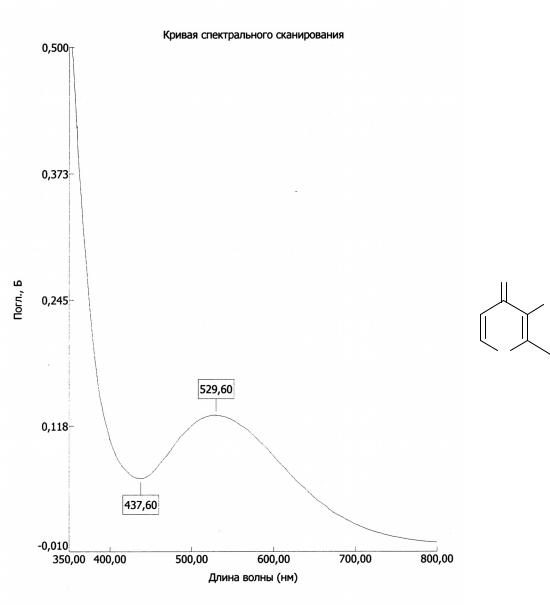
гипсохромный сдвиг (синий сдвиг) – для смещения полос поглощения в коротковолновую область спектра;
батохромный сдвиг (красный сдвиг) – для смещения полос поглощения в область длинных волн;
гиперхромный эффект – увеличение интенсивности поглощения;
гипохромный эффект – уменьшение интенсивности поглощения.
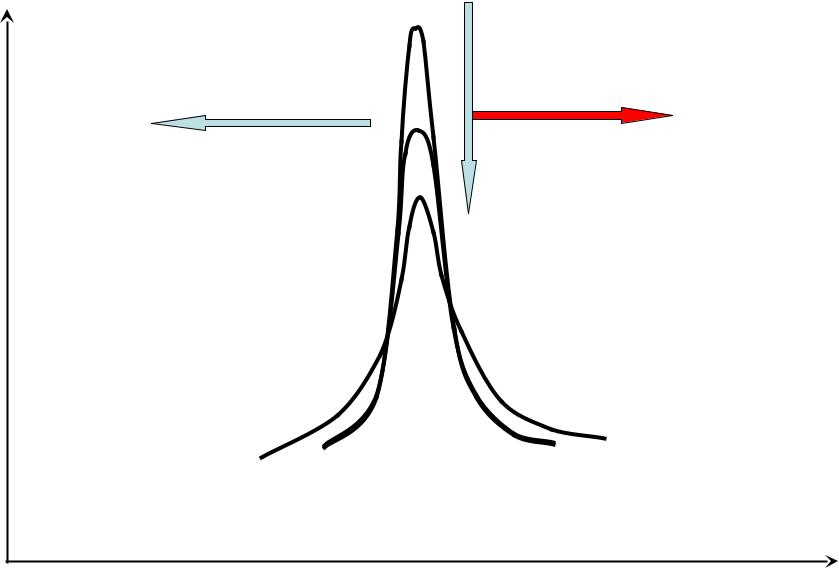
Гипсохромный сдвиг
Оптическая плотность
Гиперхромный эффект
пиГ рхо
оБатохромный сдвиг мны йэ фф ект
Длинна волны, нм
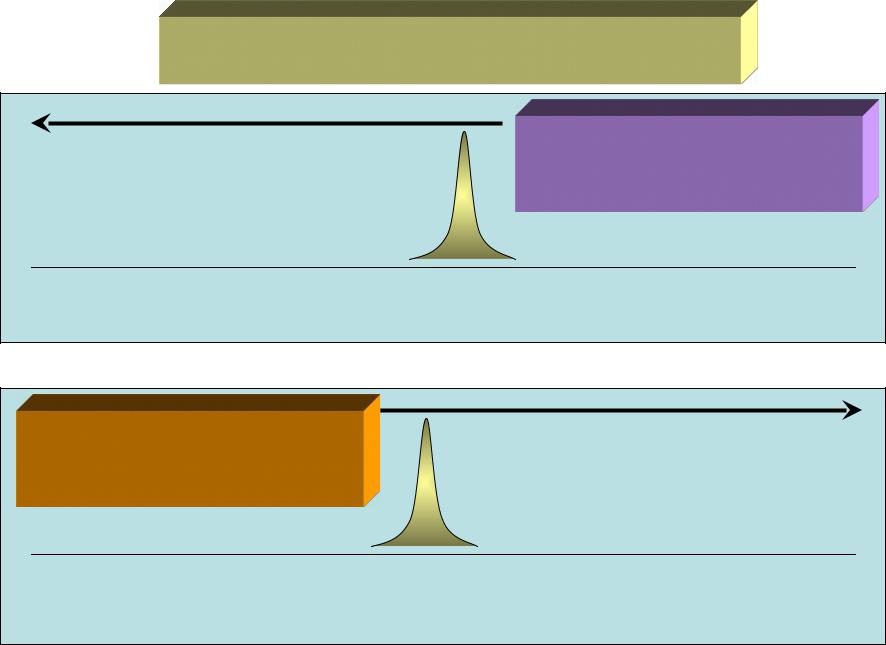
диэтиловыйводметэтанолгекснолэфир
Гипсохромный сдвиг полосы n -> при увеличении полярности растворителя
305 |
312 |
315 |
326 |
327 |
, нм |
Батохромный сдвиг полосы-> при увеличении полярности растворителя
230 237 238 244 нм

Взаимосвязь электронных спектров и структуры органических молекул
Хромофоры
Хромофор -простая функциональная группа, ответственная за поглощение с характеристическими величинами и
X - - Y |
спектр соединения - сумма спектральных |
|
характеристик индивидуальных хромофоров X и Y |
X - Y |
новый, хромофор с новыми спектральными |
|
характеристиками |
Ауксохром – функциональная группа, которая сама по себе не поглощает в близком ультрафиолете, но может влиять на поведение сопряженного с ней хромофора
Типичные ауксохромы: -SH, -NH2 , -OH
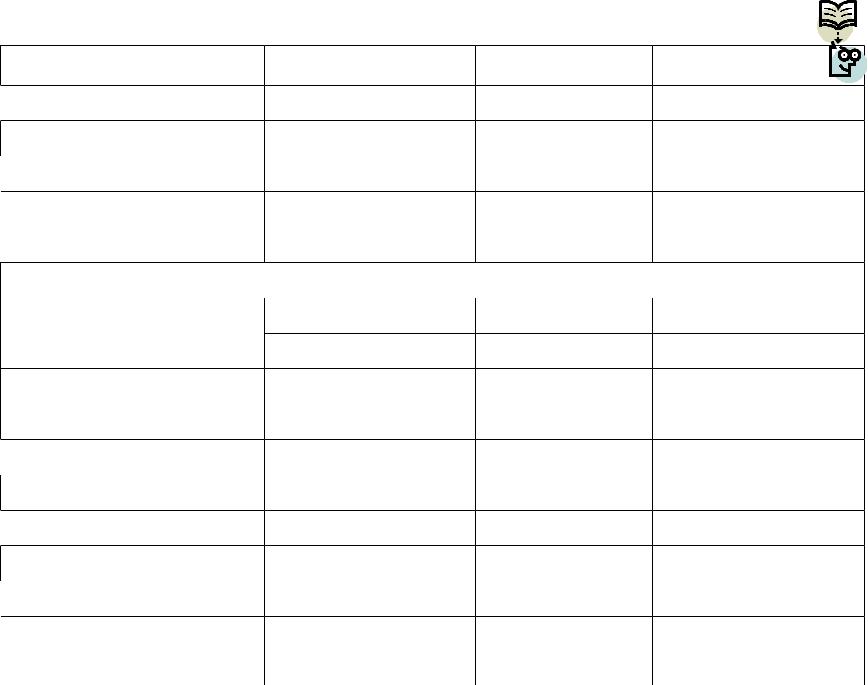
Основные хромофорные группы
Хромофор
 нитрилы
нитрилы
алкины
 алкены
алкены  спирты
спирты  простые эфиры
простые эфиры
кетоны
альдегиды
 амины
амины
кислоты
 сложные эфиры
сложные эфиры
амиды
 тиоспирты
тиоспирты  нитросоединения
нитросоединения  азосоединения
азосоединения
Тип перехода |
λmax |
log(ε) |
n → π* |
160 |
<1.0 |
π→ π* |
170 |
3.0 |
π→ π* |
175 |
3.0 |
n→σ* |
180 |
2.5 |
n→σ* |
180 |
3.5 |
π→ π* |
180 |
3.0 |
n → π* |
280 |
1.5 |
π→ π* |
190 |
2.0 |
n → π* |
290 |
1.0 |
n→σ* |
190 |
3.5 |
n → π* |
205 |
1.5 |
n → π* |
205 |
1.5 |
n → π* |
210 |
1.5 |
n → π* |
210 |
3.0 |
n → π* |
271 |
<1.0 |
n → π* |
340 |
<1.0 |
