
6 курс / Кардиология / Врожденные_пороки_сердца_у_взрослых_Раков_А_В_,_Пелеса_Е_С_,_Шпак
.pdfтестовую окклюзию дефекта (пациентов необходимо лечить совместно со специалистами, имеющими опыт лечения синдрома ЛГ) (Уровень доказательности: С).
2. Сопутствующая операция по Maze может рассматриваться для взрослых пациентов с ДМПП с пароксизмальной и хронической наджелудочковой тахиаритмией (Уровень доказательности: С).
Класс III
1. Пациентам с тяжелой необратимой ЛГ без признаков сброса слева направо не должно выполняться закрытие ДМПП (Уровень доказательности: В).
Хирургическое лечение
Таким образом, решение о хирургическом лечении любого типа ДМПП основано на клинической и эхокардиографической информации, включающей размеры и локализацию дефекта, величину лево-правостороннего шунта, гемодинамические нарушения, а также наличие и степень ЛГ. В общем, закрытие ДМПП рекомендовано всем, у кого есть признаки перегрузки ПЖ и наличие клинически значимого сброса (отношение легочного кровотока [Qp] к системному [Qs] >1,5). Отсутствие клинических симптомов не является противопоказанием к закрытию дефекта
[8].
В детстве может произойти спонтанное закрытие вторичного ДМПП, однако во взрослом возрасте такое закрытие маловероятно. Решение в пользу консервативного ведения пациентов принимают при небольших размерах дефекта и малом сбросе, а также выраженной ЛГ, диагностике порока у беременных (необходимо дожидаться окончания беременности), выраженной дисфункции ПЖ.
При неосложненных вторичных ДМПП хирургическая смертность у детей и взрослых составляет около 1-3%. Из-за высокого риска смерти, например в случаях парадоксальных эмболий, необходимо рассмотреть закрытие ДМПП даже у пациентов с небольшим сбросом. Тем не менее, этот вопрос остается спорным, т.к. у пациентов с небольшим шунтом очень хороший прогноз и риск применения искусственного кровообращения во время операции не оправдан. С развитием методов катетерного за-
51
крытия дефекта, с более низким уровнем смертности и отсутствием искусственного кровообращения рассматриваются вопросы о необходимости закрытия даже маленьких ДМПП.
Долгосрочная профилактика смерти и осложнений достигается в случае закрытия дефекта до 25 лет, когда систолическое давление в легочном стволе менее 40 мм рт.ст. Но даже у возрастных пациентов с большим размером шунта оперативное закрытие может быть применено с низким риском и хорошим результатом в регрессии симптомов.
Противопоказания. Закрытие ДМПП не рекомендуется у пациентов с клинически незначимым шунтом (Qp:Qs коэффициент 0,7 или ниже), а также у пациентов с высокой ЛГ, наличием необратимого склероза легочных сосудов, приводящих к смене шунта. В дополнение к высокому риску хирургической смертности и заболеваемости закрытие дефекта в последнем случае может существенно ухудшить прогноз [21].
Варианты хирургического лечения:
1. Хирургическое закрытие дефекта в условиях искусственного кровообращения: ушивание ДМПП или его пластическое закрытие заплатой аутоили ксеноперикарда
Стандартом в лечении ДМПП является его прямое закрытие
спомощью открытого доступа и экстракорпоральной поддержкой.
В1953 году John Gibbon успешно применил этот способ в своей практике. С тех пор хирургические техники и медицинское оборудование улучшились до такой степени, что уровень смертности при этом хирургическом вмешательстве приближается к нулю.
Обычный способ представляет собой выполнение срединной стернотомии. Производится прямая артериальная и двойная венозная (верхняя и нижняя полые вены) катетеризация. Под искусственным кровообращением пережимается аорта, производится остановка сердца. Затягиваются полые вены и открывают доступ к ПП. Большинство вторичных дефектов могут быть закрыты
спомощью наложения швов полипропиленом (Проленом). Этот способ требует особого внимания при закрытии больших дефектов, т.к. в ходе этого может наблюдаться деформация ПП. Боль-
52
шие дефекты, располагающиеся в верхней части перегородки и закрытые прямым способом, могут исказить аортальное кольцо. Такие дефекты лучше всего закрывать с помощью аутологичного перикарда или синтетических патчей (заплат), выполненных из полиэстерола (Лавсан) или политетрафлорэтилена (рисунок 17). Необходимо убедиться в полном удалении пузырьков воздуха из ЛП и ЛЖ перед остановкой искусственного кровообращения [8].
Хирургическое закрытие первичного ДМПП сложнее в сравнении со вторичным. Заплатка должна быть прикреплена к перегородке на стыке трехстворчатого и митрального клапанов. Для коррекции или профилактики митральной регургитации необходимо выполнить восстановление митрального клапана и, возможно, аннулопластику.
Дефект венозного синуса часто ассоциирован с АДЛВ. Одна или более легочных вен впадают в ПП. Поэтому дефект должен быть исправлен таким образом, чтобы быть уверенным, что дренаж легочных вен осуществляется в ЛП. Это может быть как простым, так и сложным, что зависит от места впадения легочных вен. Много инновационных технологий было разработано для перенаправления тока крови через легочные вены. Легочный венозный возврат не должен быть нарушен в связи с перенаправлением тока крови через легочные вены, так как это неизменно вызывает локализованную ЛГ.
Миниинвазивные подходы
В последние годы существенный интерес возрос к малоинвазивным способам коррекции порока. В большинстве случаев происходят простое уменьшение размера разреза и разнообразные подходы к кровообращению во время операции. Например, частичный или полный субмаммарный разрез кожи, гемистернотомия и ограниченная стернотомия. Целью является лишь достижение наилучших косметических результатов, поскольку никак не связано со снижением заболеваемости и смертности.
53
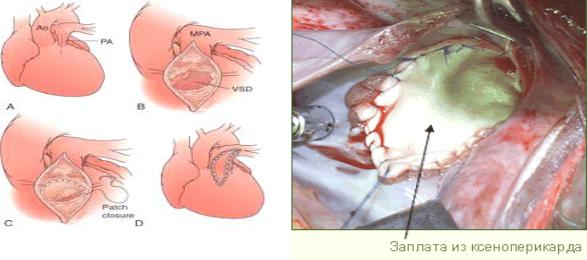
Рисунок 17. Закрытие ДМПП заплатой
2. Эндоваскулярное закрытие ДМПП окклюдером. Чрескожное транскатетерное закрытие дефекта
В последнее время вторичные ДМПП все больше закрываются с помощью доставляемых с помощью катетера имплантируемых устройств. Эти устройства проводятся через бедренную артерию и раскрываются как зонтик, закрывая тем самым дефект в МПП. Лучше всего эти устройства работают при центрально расположенных дефектах.
Хирургическое вмешательство выполняется в условиях рентгеноперационной. У детей используется наркоз, у взрослых в ряде случаев процедура может быть выполнена под местным обезболиванием. Ни разреза грудной клетки, ни использования аппарата искусственного кровообращения не требуется.
Для эндоваскулярной окклюзии ДМПП производят пункцию правой бедренной вены. Далее катетеризируют правые отделы сердца с регистрацией давления в полостях. После катетеризации ЛП определяют точные размеры ДМПП, для чего по оставленному проводнику в ЛП проводят специальный измерительный баллон. Баллон раздувают путем введения определенного количества физиологического раствора, разведенного с контрастным веществом 1:1. Далее под контролем ЧПЭ и рентгеноскопии баллонный катетер низводят к перегородке. При этом окклюзирующим диаметром баллонного катетера считают размер баллона, который обтурирует дефект и при натяжении проскальзывает че-
54

рез него в ПП. После удаления баллона по оставленному проводнику в ЛП проводят доставляющую систему. В зависимости от полученного диаметра измерительного баллона подбирают необходимый размер окклюдера [28, 37, 42].
Устройство представляет собой два диска из нитиноловой проволоки (сплав элементов титана и никеля), заполненные тонкими нитями из дакрона (синтетический полимер). В сложенном состоянии окклюдер располагается в тонком ангиографическом катетере.
Наиболее часто используемым является окклюдер перегородки Amplatzer (ASO) (рисунок 18), т.к. его легко имплантировать и он способен успешно закрывать большие дефекты во многих случаях [15].
Рисунок 18. «Amplatzer» окклюдер
Система «AMPLATZER» была разработана американской корпорацией AGA Medical под руководством профессора Курта Амплатца и в сотрудничестве с профессором Йозефом Машура – ведущим специалистом кардиологического центра детской университетской клиники г. Братислава. Там же была произведена первая в мире имплантация окклюдера в сентябре 1995 г. У человека он впервые был использован в 1995 г. Выбор конкретного устройства весьма труден, так как не проводились многоцентровые рандомизированные исследования. Кроме того, в настоящее время этот метод не применим для закрытия первичного ДМПП и дефекта венозного синуса.
Окклюдер привинчивают к фиксатору и по доставляющему катетеру проводят его в полость ЛП. Под рентгеноскопическим и
55
чреспищеводным эхокардиографическим наблюдением раскрывают первый диск в ЛП и оттягивают окклюдер так, чтобы диск прикрыл дефект со стороны ЛП. Если его расположение по отношению к дефекту и митральному клапану расценивается как удовлетворительное по данным ЭхоКГ, то открывают второй диск со стороны ПП. После раскрытия обоих дисков тракционными движениями определяют надежность его крепления и производят отцепление окклюдера от фиксатора (рисунки 19, 20, 21). Всем больным после эндоваскулярной окклюзии назначают аспирин в течение 6 месяцев после операции [15, 28].
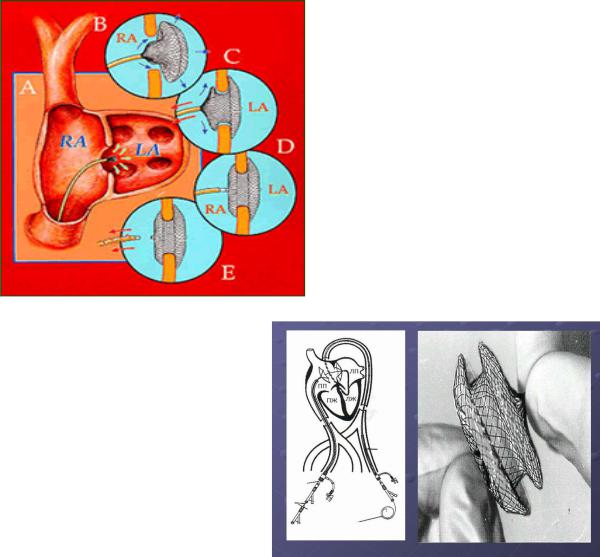
Рисунок 19. Этапы установки Amplatzer
окклюдера:
A – доставляющий катетер с окклюдером внутри проведен в камеры сердца. B – Первый диск окклюдера открыт в ЛП.
C, D – Второй диск окклюдера открыт в ПП, контроль правильности установки. E – доставляющий катетер отсоединен от окклюдера. Процедура установки завершена
Рисунок 20. Установка окклюдера
56
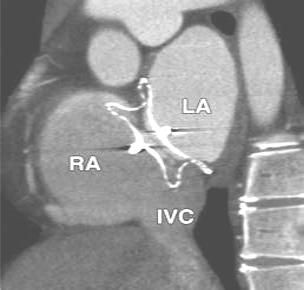
Рисунок 21. Amplatzer окклюдер на МРТ
RA – правое предсердие,
LA – левое предсердие,
IVC – нижняя полая вена
Продолжительность вышеописанной процедуры, включая подготовку пациента, составляет около часа. Через сутки после операции проводится контрольное обследование, и если осложнений не наблюдается, пациента выписывают. После выписки пациент находится под наблюдением кардиохирурга, с периодичностью сначала в один, затем в три месяца выполняется ЭхоКГ для контроля положения окклюдера и герметичности МПП.
Транскатетерное закрытие ДМПП в настоящее время является устойчивой практикой во многих кардиохирургических центрах. Доказано, что в опытных руках это экономически эффективный метод с низкой частотой послеоперационных осложнений, сокращением госпитализации и снижением потребности в препаратах крови.
В любом возрасте закрытие ДМПП сопровождается снижением клинической симптоматики, регрессией размеров ПЖ. Однако лучший результат достигается у пациентов с меньшими функциональными нарушениями и менее высоким положительным давлением в дыхательных путях.
Учитывая постоянное усиление симптомов, ремоделирование ПЖ и возрастание положительного давления в дыхательных путях с возрастом, закрытие ДМПП должно быть рекомендовано как можно раньше после установления диагноза, независимо от клинической симптоматики, даже у взрослых пожилого возраста.
57
На сегодняшний день в Беларуси в каждом областном центре функционируют кардиохирургические отделения. Внедрены новые эффективные диагностические технологии: спиральная многосрезовая КТ; высокопольная МРТ; однофотонная эмиссионная КТ [5, 6]. Расширился диапазон лечебных вмешательств под рентгеновским и ультразвуковым контролем: баллонная ангиопластика и стентирование сосудов; рентгеноэндоваскулярная окклюзия сосудов; эндоваскулярное закрытие ДМПП, ДМЖП и ОАП; эндопротезирование брюшной аорты; радиочастотная абляция опухолей и путей дополнительной иннервации при нарушениях ритма.
Послеоперационный период
Ведение пациента в послеоперационном периоде после закрытия ДМПП, как правило, стандартное. Дренажные трубки удаляются на следующее утро после операции, и кроме случаев возникновения проблем с ритмом, следом удаляются электроды. Большинство пациентов способны есть самостоятельно, и передвигаться на 1-2 день после операции и могут быть выписаны уже на 3-4 день. После транскатетерной окклюзии пациенты могут быть выписаны на следующий день. Для предотвращения тромбообразования пациентам рекомендовано в течение 6 месяцев принимать аспирин в комбинации с клопидогрелем или без данного препарата. Послеоперационное хирургическое наблюдение таких пациентов осуществляется до полного заживления ран и восстановления, и редко превышает 1-2 месяца. Все осложнения должны быть четко распознаны до выписки пациента. Должна быть выполнена как минимум одна ЭхоКГ, подтверждающая полное закрытие ДМПП. Дальнейшее наблюдение и ведение пациента осуществляет кардиолог [18, 29].
Хирургическое лечение может быть ассоциировано с долгосрочным риском возникновения фибрилляции, трепетания предсердий. В течение 6 месяцев после операции существует риск развития инфекционного эндокардита.
Осложнения, специфичные для транскатетерной окклюзии ДМПП
Эмболизация и дислокация окклюдера: частота зависит от варианта окклюзирующего устройства, его выбора и опыта хи-
58
рурга. У опытных хирургов частота такого осложнения менее 1%. Постимплантационные аритмии: частота 1-4%. Проявляются атриовентрикулярными блокадами разной степени, фибрилля-
цией предсердий. Аритмии, как правило, кратковременны и не требуют особого лечения.
Тромбообразование. К факторам риска тромбообразования отнесены типы окклюзирующих устройств, фибрилляция, возникшая в послеоперационный период, неполная эндотелизация поверхности окклюдера, недостаточное антитромботическое лечение и ранее не диагностированные гиперкоагуляционные расстройства (включая резистентность к аспирину). Профилактика – назначение аспирина в течение 6 месяцев.
Перфорация сердца. Частота встречаемости для различных девайсов 0,1-0,4%. Фактор риска – завышенные размеры окклю-
дера [23].
Эрозии девайса. Эрозии окклюдера наблюдаются в 0,1- 0,15%. Фактор риска – избыточный размер девайса. Результатом может быть фистула между правым предсердием и аортой. Хоть это осложнение и редкость, смертность составляет до 10% [27].
Повышение уровня сердечного тропонина I. Транскатетерное закрытие вызывает незначительные повреждения миокарда, степень которых зависит от размера ASO [24].
Остаточный шунт. Около 20% пациентов могут иметь остаточный шунт в течение 24 часов после операции. При последующих наблюдениях частота данного осложнения приближается к
0%.
Другие осложнения включают перикардит, транзиторную ишемическую атаку, внезапную смерть.
Рекомендации по наблюдению после оперативного лече-
ния [14, 18, 29]
Класс I
1.Ранние послеоперационные симптомы, такие как повышение температуры, утомляемость, рвота, боль в груди или абдоминальная боль, могут означать посткардиотомный синдром с тампонадой, который требует немедленной эхокардиографической оценки (Уровень доказательности: С).
2.Ежегодный клинический осмотр рекомендован пациентам
59
после операции, если ДМПП был закрыт, а следующие состояния остались или появились:
А. Легочная артериальная гипертензия (Уровень доказательности: С).
Б. Наджелудочковая аритмия (Уровень доказательности: С). В. Правожелудочковая или левожелудочковая дисфункция
(Уровень доказательности: С).
Г. Сопутствующие пороки или другие заболевания сердца (Уровень доказательности: С).
3.Оценка возможной миграции окклюдера, развития эрозии или других осложнений рекомендованы пациентам через 3-12 месяцев после операции и периодически далее (Уровень доказательности: С).
4.Разрушение окклюдера, которое может проявляться болью в груди или синкопальным состоянием, требует немедленного обследования (Уровень доказательности: С).
Естественное течение порока и прогноз
Определяется размером дефекта и величиной артериовенозного сброса. Дети со вторичными и малыми ДМПП растут и развиваются обычно, не предъявляя никаких жалоб. Первые симптомы неблагополучия могут выявиться лишь на третьем десятке жизни. Однако в дальнейшем заболевание быстро прогрессирует, что приводит к гибели или инвалидизации пациентов. Основной причиной смерти является развитие выраженной правожелудочковой сердечной недостаточности, реже высокая ЛГ [3, 12, 17].
Общие сопутствующие заболевания у пациентов с ДМПП, ухудшающие прогноз заболевания:
1.ЛГ проявляется у 15-20% пациентов с ДМПП. Данная патология встречается не так часто у молодых людей, но практически у 50% пациентов старше 40 лет.
2.Синдром Эйзенменгера – это позднее и редкое осложнение вторичного ДМПП, встречающееся в 5-15% случаев, характеризующееся высокой ЛГ, приводящей к смене шунта с артериовенозного на веноартериальный, осуществляемый справа налево. Обедненная кислородом кровь поступает в системный кровоток, что приводит к развитию системной гипоксемии и цианозу.
60
