
2 курс / Нормальная физиология / Сердце и легкие
.pdf1.3. Строение, функция и регуляция системы кровообращения |
51 |
скоростными возможностями распространения
нервного импульса в центральный аппарат управления и в передаче сигнала на исполнительные
структуры [28].
В регуляции сосудистого тонуса особая роль принадлежит адренергическим вазоконстрикторным во-
локнам, которые оказывают эффект, высвобождая но-
радреналин лишь в непосредственном контакте с наружной поверхностью медии сосуда. Там норадрена-
лин связывается с α-адренорецепторами мембраны
миоцитов и вызывает сокращение гладких мышечных волокон сосудистой стенки.
Нейрогенная вазодилатация, как считают, осно-
вана на пассивном расширении сосудов, возникающем вследствие понижения активности вазоконст-
рикторных нервов [41]. Такие реципрокные соотно-
шения в различных эфферентных нервах, когда одни возбуждаются, а другие тормозятся, определяют ре-
гионарное распределение объемного кровотока.
Заслуживает внимания феномен функционального симпатолиза, когда в интенсивно работающей ткани
снижается чувствительность к вазоконстрикторным
воздействиям нейрогенного происхождения. Данное явление объясняют тем, что продукты, выделяющи-
еся в процессе жизнедеятельности ткани, являются
ингибиторами секреции вазоконстрикторных симпатических медиаторов [22, 45]. Следовательно, мест-
ные механизмы регуляции кровообращения могут подавлять центральные нейрогенные влияния.
–Механические факторы – внутрисосудистое (точ-
нее, интрамуральное) давление и скорость потока крови – две основные силы, инициирующие активные сократительные реакции кровеносных сосудов.
Первый регуляторный механизм, известный как
феномен Остроумова–Бейлисса, заключается в том,
что при повышении внутрисосудистого давления, ведущего к растяжению гладких мышц сосудов и воз-
буждению активной сократительной реакции, умень-
шается внутренний диаметр сосуда. В результате происходит увеличение сопротивления потоку крови и
сохранение неизменным объемного кровотока либо
ограничение степени его увеличения, вызванного повышенным давлением. Обратный эффект – расслаб-
ление гладких мышц, увеличение диаметра сосудов,
снижение сосудистого сопротивления и увеличение (или поддержание неизменным) объемного кровото-
ка – происходит при снижении трансмурального дав-
ления. Изложенное отражает суть миогенной ауторегуляции тонуса сосудов – регуляторного контура, ко-
торый не требует участия центральной нервной сис-
темы и может принимать участие в управлении кровообращением как на системном и органном, так и
на тканевом уровнях [17, 22, 41].
Второй феномен заключается в расслаблении
гладких сосудистых мышц и увеличении диаметра
сосуда в ответ на увеличение скорости потока крови. Предполагается, что увеличение диаметра артерий
при механической стимуляции повышенным кровотоком обусловливается специфической функцией
сосудистого эндотелия [52], так как деэндотелизация артерии предотвращает возникновение этой реакции
[28].
–Химический контур регуляции представлен многи-
ми факторами, влияющими на сокращение и расслабление гладких мышц сосудистой стенки. Раз-
личают два вида химической регуляции тонуса сосудов:
1)вазоактивными продуктами жизнедеятельности тканей – метаболическая регуляция;
2)продуктами, выделяемыми в кровяное русло специализированными структурно-функцио-
нальными образованиями – гормональная регуляция [17, 41, 54].
–Метаболическая регуляция осуществляется хими- ческими веществами, накапливающимися в меж-
клеточной среде тканей и снаружи влияющими на гладкие мышцы близлежащих сосудов.
Среди нормальных продуктов метаболизма всех
органов выраженным вазомоторным эффектом обладает двуокись углерода (СО2 ) – конечный продукт
окислительного метаболизма. Вазомоторный эффект СО2 существенно различается в разных органах, но в
любом случае повышение концентрации СО2 в ткани вызывает вазодилатацию, а снижение – вазокон-
стрикцию.
Дилататорным влиянием на сосуды обладает увеличение в ткани молочной кислоты (лактата) и орга-
нических кислот цикла Кребса, а также ионов водорода (снижение рН). Однако чувствительность сосу-
дов к этим веществам невелика.
Одним из наиболее мощных дилататорных мета-
болитов является аденозин, образующийся в функционирующих тканях из аденозинмонофосфата.
Внутриартериальное введение аденозина вызывает зависимое от дозы расслабление сосудов и увеличе-
ние кровотока в скелетных мышцах, печени, почках, но наиболее резкое – в сердце [28].
Из неорганических ионов наибольшее влияние на тонус сосудов оказывают ионы калия и кальция, на-
личие которых в периваскулярной среде является не-
обходимым условием для проявления нормальных сократительных реакций в мышечных волокнах. Сни-
жение интерстициальной концентрации Са2+ приводит к расслаблению сосудистых гладких мышц, а по-
вышение концентрации – к их сокращению. Изменения тканевого содержания ионов калия вызывают
прямо противоположные сосудистые реакции. Одним из важнейших факторов регуляции сосу-
дистого тонуса является напряжение кислорода (РО2)

52 |
Глава 1. ФИЗИОЛОГИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ. ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ... |
в крови и тканях. Дефицит кислорода возникает вся-
кий раз при увеличении функциональной активности тканей, при недостаточном кровоснабжении, при
снижении РО2 в крови. В любом случае недостаток
кислорода вызывает снижение сосудистого тонуса и увеличение кровотока. Надо подчеркнуть, что речь
здесь идет только о местном влиянии снижения тка-
невого РО2 без учета сопутствующих гипоксии хеморефлекторных, гормональных и других влияний вто-
ричного характера [56]. Сосудорасширяющий эффект
гипоксии существенно различается в разных органах. В наибольшей степени он выражен в сердце и мозге,
менее выражен в скелетных мышцах, еще слабее – в
коже и подчас не выявляется до глубокой гипоксии в почке. Такое органное различие чувствительности к
снижению тканевого РО2 является одним из важных
механизмов перераспределения кровотока в пользу жизненно важных органов и первоочередного их
обеспечения кислородом при гипоксии.
–Сосудистый эндотелий при химических и физических изменениях способен реагировать продукцией сосудорасширяющих и сосудосуживающих ве-
ществ. К первым относятся эндотелиальный релаксирующий фактор (оксид азота – NO), простациклин, эндотелиальный гиперполяризующий
фактор. Вазоконстрикцию вызывают эндотелин, тромбоксан А2, простагландин Н2, ангиотензин II. Считается, что баланс между эндотелиальными
факторами релаксации и констрикции определяет тонус сосудов и, соответственно, величину местного кровотока [57].
–Гормональная регуляция сосудистого тонуса и сердечной деятельности является звеном нейрогумо-
рального управления кровообращением, в котором нервный и гормональный компоненты интегрированы. На систему кровообращения влияют
все гормоны, однако различают: а) непосредственное их влияние в виде сравнительно быстрых и значительных изменений сосудистого тонуса; б)
опосредованное действие, главным образом через изменение общего метаболизма и электролитного баланса [28].
Такие гормоны, как адреналин, вазопрессин, ангиотензин, сосудистые эффекты которых описаны в
предыдущем разделе, обладают выраженным прямым
вазомоторным действием, и, хотя эти вещества не относятся к местным метаболическим факторам, они
составляют важный элемент химический регуляции
тонуса сосудов.
К гормонам опосредованного влияния на кровообращение относятся кортикостероиды, тироксин,
инсулин, адренокортикотропный гормон. Их действие отличается постепенным развитием и большой
продолжительностью эффекта, измеряемой неделями и месяцами.
Большую группу вазоактивных веществ, участву-
ющих в местной регуляции кровообращения, представляют тканевые гормоны – гистамин, брадикар-
дин, серотонин. Они образуются во многих тканях
организма при повреждающих воздействиях или при усилении функциональной активности органа, но, в
отличие от тканевых метаболитов, они не связаны
прямо с энергетическим обеспечением клеток. Как правило, эти вещества вызывают расширение сосу-
дов, а для гистамина и брадикардина характерна спо-
собность еще и увеличивать сосудистую проницаемость.
–Эйкозаноиды составляют группу биологически ак-
тивных веществ, синтезируемых практически во всех тканях организма. Представители этого семейства веществ – простагландины, тромбоксан,
лейкотриены – оказывают выраженное влияние на тонус сосудов и их проницаемость.
Из простагландинов (ПГ) наиболее сильным вазодилатирующим действием обладает ПГЕ 1 è íå-
сколько уступает ему по силе ПГЕ2. Они оказывают
также антиагрегационное влияние на тромбоциты. Сопоставимым по силе сосудорасширяющим дей-
ствием обладает простациклин (ПГI2). Он синтези-
руется в эндотелии сосудов, не разрушается в легких, но инактивируется в крови и печени.
Тромбоксан А2 сокращает коронарные сосуды и
способствует также агрегации тромбоцитов. Лейкотриен В4 усиливает транскапиллярную
фильтрацию жидкости в интерстициальное простран-
ство. Лейкотриены С4, D4, Å4 обладают вазоконстрикторным действием [52]. Кроме того, предполагается
возможное участие эйкозаноидов в регуляции сис-
темного АД, возникновении спазмов сосудов сердца и мозга.
Завершая этот раздел, укажем, что под тонусом
сосудов следует понимать непрерывно поддерживаемую определенную степень сократительной активно-
сти сосудистых гладких мышц, которая не сопровож-
дается утомлением и определяет противодействие растягивающему сосуд давлению крови. Усиление то-
нуса сосудов сопровождается увеличением сопротив-
ления потоку крови, а ослабление – уменьшением сопротивления. Соответственно этому изменяется ско-
рость и объем сосудистого кровотока.
Функциональное назначение регуляции кровообращения
Как мы уже не раз указывали, каждый орган способен эффективно функционировать только при ус-
ловии адекватного кровоснабжения. Изменение де-
ятельности органа должно сопровождаться соответствующими изменениями кровотока. Конечный ре-
зультат многофакторной регуляции кровообращения
1.3. Строение, функция и регуляция системы кровообращения |
|
|
|
|
53 |
|||
достигается за счет детерминированных изменений |
|
рядов, что предупреждает изменение частоты сердеч- |
||||||
сердечного выброса и сопротивления региональных |
|
ных сокращений. |
|
|
||||
отделов сосудистого русла. В этом случае основной |
|
|
Конечное диастолическое давление в желудочках |
|||||
функцией артерий является создание постоянного |
|
определяется отношением между объемом циркули- |
||||||
напора, под которым кровь движется по капиллярам. |
|
рующей крови и емкостью сердечно-сосудистой сис- |
||||||
Оптимальный уровень кровоснабжения тканей |
|
темы, в частности венозной ее части. Снижение объе- |
||||||
обеспечивается перфузионным давлением, создава- |
|
ма циркулирующей крови теоретически может ком- |
||||||
емым кровью в артериальных сосудах организма. Сле- |
пенсироваться уменьшением емкости вен, так что |
|||||||
довательно, одним из важнейших условий гемодина- |
|
уровень давления в центральных венах не меняется |
||||||
мики является артериальное давление. |
|
|
|
[22]. |
|
|
||
Артериальное давление – интегральный параметр, |
|
|
Из представленного ясно, что любое изменение |
|||||
отражающий взаимодействие многих факторов, та- |
|
АД указывает на изменение какого-либо механизма |
||||||
ких, как систолический объем сердца, скорость выб- |
|
(или механизмов) из приведенных на рис. 37, кото- |
||||||
роса крови из желудочков сердца, частота сердечных |
|
рое не полностью компенсировалось другими меха- |
||||||
сокращений, сопротивление стенок артерий растяже- |
|
низмами. |
|
|
||||
нию, суммарное сопротивление кровотоку резистив- |
|
|
Система, следящая за уровнем АД и включающая |
|||||
ных сосудов, суммарный объем емкостных сосудов, |
|
соответствующие компенсаторные механизмы серд- |
||||||
объем циркулирующей крови, ее вязкость, гидроста- |
|
ца и сосудов для поддержания этого давления в отно- |
||||||
тическое давление столба крови. Главным при этом |
|
сительно узких пределах, автоматически согласует ве- |
||||||
является работа сердца [12, 17, 45, |
|
|
|
|
|
|
|
|
52]. |
|
|
|
|
|
|
|
|
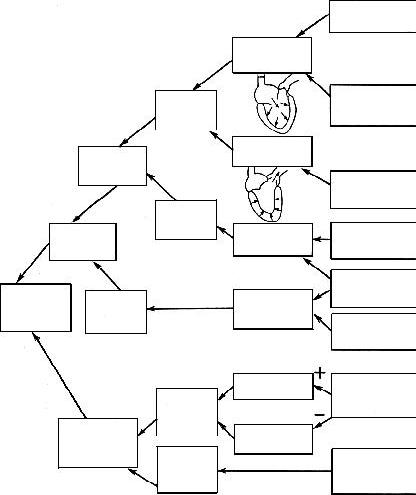
Если изобразить схему факто- |
|
|
|
|
|
|
|
Объем крови |
ров, влияющих на системное АД, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в виде ветвей дерева (рис. 37), то |
|
|
|
|
|
|
Давление |
|
изменения, возникающие в каж- |
|
|
|
|
|
|
наполнения |
|
дой из «ветвей», могут быть ком- |
|
|
|
|
|
|
желудочков |
|
пенсированы. Так, например, |
|
|
|
|
|
|
|
|
уменьшение сердечного выброса |
|
|
|
|
|
Диастоли- |
|
Венозная емкость |
может быть уравновешено соот- |
|
|
|
|
|
ческий |
|
|
|
|
|
|
|
|
|
||
ветствующим увеличением обще- |
|
|
|
|
|
объем |
|
|
|
|
|
|
|
|
|
|
|
го периферического сосудистого |
|
|
|
|
|
|
Растяжимость |
|
сопротивления, так что систем- |
|
|
|
Ударный |
|
желудочков |
|
|
ное АД остается на прежнем |
|
|
|
|
объем |
|
|
Нейрогуморальные |
уровне. Аналогичным образом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
механизмы |
|
уменьшение общего перифери- |
|
|
|
|
|
|
|
регуляции |
ческого сопротивления сосудов |
|
|
|
|
|
Систоличес- |
|
|
может быть полностью компен- |
|
Сердечный |
кий объем |
Изгнание из |
Коронарный |
|||
сировано увеличением сердечно- |
|
|
||||||
|
|
выброс |
|
|
желудочка |
кровоток |
||
го выброса. |
|
|
|
|
|
|
|
|
Уменьшение ударного объема |
|
|
|
|
|
|
|
Симпатические |
сердца может компенсироваться |
Системное |
|
|
|
|
|
|
импульсы |
повышением частоты сердечных |
|
|
|
Частота |
|
Частота водителя |
к сердцу |
|
артериальное |
|
|
|
|||||
сокращений |
|
|||||||
сокращений, так что величина |
давление |
|
ритма |
Холинергические |
||||
|
|
сердечных |
||||||
|
|
|
||||||
сердечного выброса остается не- |
|
|
|
|
|
|
|
импульсы |
изменной. При уменьшении ди- |
|
|
|
|
|
|
|
к сердцу |
астолического объема желудоч- |
|
|
|
|
|
|
|
|
ков величина ударного объема |
|
|
|
|
|
|
Расширение |
Нейрогуморальная |
может сохраняться за счет более |
|
|
|
|
|
Общие |
сосудов |
|
полного изгнания крови при си- |
|
|
|
|
|
сосудо- |
|
регуляция |
столе. |
|
|
|
|
|
двигатель- |
|
|
|
|
Суммарное |
ные влияния |
Суживание |
|
|||
Уменьшение количества раз- |
|
|
|
|||||
|
|
|
|
|||||
рядов симпатических нервов, |
|
|
периферическое |
Местные |
сосудов |
|
||
|
|
сопротивление |
|
Сосудо- |
||||
действующих на водитель ритма, |
|
|
|
|
|
сосудо- |
|
|
|
|
|
|
|
|
расширяющие |
||
может быть уравновешено соот- |
|
|
|
|
|
двигатель- |
|
|
|
|
|
|
|
|
вещества |
||
|
|
|
|
|
ные влияния |
|
||
ветствующим уменьшением ко- |
|
|
|
|
|
|
|
|
личества парасимпатических раз- |
Ðèñ. 37. Факторы, определяющие системное артериальное давление [22] |
|
||||||

54 |
Глава 1. ФИЗИОЛОГИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ. ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ... |
|||
личину венозного возврата крови и сердечного выб- |
мального кровообращения в зависимости от диапа- |
|||
роса так, чтобы суммарный кровоток через капилляр- |
зона колебаний уровня СИ в группах мужчин и жен- |
|||
ную сеть не превышал бы мощности сердечного на- |
ùèí: |
|||
ñîñà. |
– |
гиперкинетический тип кровообращения: |
||
|
Как известно, объективной мерой количества кро- |
|
СИ у мужчин – 5,67–4,32 л/мин/м2, |
|
ви, протекающей по всей сосудистой системе в еди- |
|
у женщин – 6,06–4,70 л/мин/м2; |
||
ницу времени, является минутный объем кровообра- |
– |
эукинетический тип кровообращения: |
||
щения (МОК), или сердечный выброс, то есть коли- |
||||
|
СИ у мужчин – 4,31–2,96 л/мин/м2, |
|||
чество крови, которое поступает в аорту или легоч- |
|
|||
|
у женщин – 4,69–3,33 л/мин/м2; |
|||
ную артерию из левого или правого желудочков серд- |
|
|||
– |
гипокинетический тип кровообращения: |
|||
ца за одну минуту. Факторы, влияющие на внешнюю |
||||
производительность сердца и определяющие величи- |
|
СИ у мужчин – 2,95–1,59 л/мин/м2, |
||
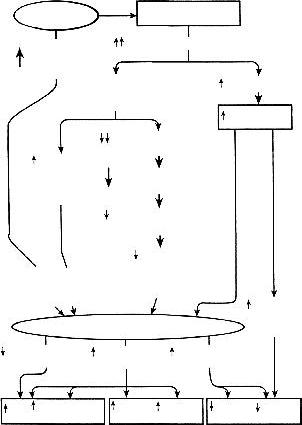
ну МОК, изображены на рисунке 38 (см. также раз- |
|
у женщин – 3,32–1,95 л/мин/м2. |
||
äåë 1.1.4). |
|
Надо особенно подчеркнуть, что выделение этих |
||
|
Считается, что отнесение объемных показателей |
типов кровообращения проводилось среди здорово- |
||
(УО, МОК) к поверхности тела с учетом роста и веса |
го населения, являющегося качественно однородным. |
|||
обследуемого лучше отражает соотношение между |
Гемодинамически эта однородность подтвердилась |
|||
сердечным выбросом и индивидуальными размера- |
тем, что величины частоты сердечных сокращений, |
|||
ми организма [41]. Полученные таким путем ударный |
среднего динамического давления (СДД) и периода |
|||
(УИ) и сердечный (СИ) индексы широко использу- |
изгнания левого желудочка, а также расход энергии, |
|||
ются при исследовании сердечно-сосудистой систе- |
обеспечивающей функционирование сердечно-сосу- |
|||
мы в условиях клиники. |
дистой системы, между всеми тремя типами не раз- |
|||
|
Популяционные исследования показателей сис- |
личались, подтверждая тем самым тождественность |
||
темного кровообращения, проведенные И.К. Шхва- |
типов кровообращения в отношении здоровья. |
|||
цабая с сотрудниками [58], убедительно доказали ге- |
|
Наряду с этим, механизмы, посредством которых |
||
модинамическую неоднородность здорового населе- |
обеспечивалась тензионная и энергетическая одно- |
|||
ния и возможность выделения трех вариантов нор- |
родность, при каждом из этих типов оказались раз- |
|||
|
|
|
|
личными. При гиперкинетическом типе |
|
|
|
|
|
ведущим механизмом поддержания оп- |
|
|
Факторы нейрогуморальной регуляции |
|
тимального СДД является СИ на фоне |
||
|
|
|
|
достоверно более высоких значений УИ, |
|
|
×ÑÑ |
ÑÔÌ |
|
в то время как удельное периферичес- |
|
|
|
кое сосудистое сопротивление (УПСС) |
|||
ÊÄÎ* |
|
|
|
||
|
|
ÎÖÊ |
оказывается самым низким. При эуки- |
||
ÎÏÑÑ* |
ÎÏÑÑ |
ÎÂÏ |
|||
ÂÃÄ |
нетическом типе СИ уменьшается на |
||||
ÎÑÊÊ |
|
|
|||
|
|
|
|
фоне снижения УИ, а УПСС, наоборот, |
|
|
|
ÌÎÊ |
|
возрастает. При гипокинетическом типе |
|
|
|
(ÑÈ) |
|
преобладающее значение для поддержа- |
|
|
|
|
|
ния необходимого СДД имеет артери- |
|
|
|
|
|
альный тонус, соответственно, УПСС |
|
|
Кровоснабжение органов и тканей |
|
оказывается наибольшим, а величины |
||
|
|
СИ и УИ – наименьшими (приложение |
|||
|
|
|
|
||
|
|
|
|
4). |
|
|
Факторы местной регуляции |
|
Распределение МОК между различ- |
||
|
|
ными сосудистыми отделами осуществ- |
|||
|
(ÐÎ2, ÐÑÎ2, метаболиты) |
|
ляется соответственно регионарным ме- |
||
|
|
|
|
таболическим потребностям определен- |
|
Обратная связь |
|
|
Обратная связь |
ным, выработанным в филогенезе и он- |
|
|
|
тогенезе, приоритетам. У человека кро- |
|||
|
|
|
|
воток поддерживается на достаточно |
|
Ðèñ. 38. Основные факторы, влияющие на внешнюю производительность сердца: ВГД – внут- |
высоком уровне и с большим постоян- |
|
ригрудное давление; КДО – конечный диастолический объем (* – гетерометрический меха- |
ством, прежде всего, в сосудистых сис- |
|
низм Франка–Старлинга); МОК – минутный объем крови; ОВП – объем венозного притока; |
темах мозга и сердца. |
|
ОПСС – общее периферическое сосудистое сопротивление (** – гомеометрический меха- |
||
У человека средней массы тела (око- |
||
низм Анрепа); ОСКК – объемная скорость коронарного кровотока; ОЦК – объем циркулирую- |
||
щей крови; СИ – сердечный индекс; СФМ – сократительная функция миокарда; ТВ – тонус |
ло 70 кг) в состоянии покоя сердце пе- |
|
вен; ЧСС – частота сердечных сокращений |
регоняет по системе кровообращения |
1.3. Строение, функция и регуляция системы кровообращения |
55 |
приблизительно 5–6 л крови в минуту. В этом случае
измерения регионарного кровотока показывают, что головной мозг получает 750 мл/мин крови, печень –
1300 мл/мин, почки – 1200 мл/мин, мышцы – 1000
мл/мин, а само сердце – 250 мл/мин. Все это составляет 4,5 л/мин, не считая снабжения кровью кожи,
жировой клетчатки и костей [41].
Cопоставление кровотока и потребления кислорода в различных органах (приложение 5) показыва-
ет, что чем интенсивнее обмен веществ в том или
ином органе, тем выше расход крови в его сосудах, хотя, если исходить из значений этих параметров, вы-
раженных в процентах, то прямой зависимости не
обнаруживается [45].
При физической нагрузке гемодинамические изменения по своему конечному значению представля-
ют системную функциональную гиперемию с преимущественной ориентацией на скелетные мышцы и
жизненно важные органы (табл. 2). Именно на это
направлены регулирующие механизмы перераспределения регионарного сосудистого тонуса и изменений
сердечной деятельности [22, 45, 59].
Во время интенсивной мышечной работы у здорового человека МОК может увеличиться до 25
л/мин, а у спортсмена – до 35–40 л/мин. Регионар-
ный кровоток в этой ситуации также подвергается значительным изменениям. При этом ясно, что серд-
це не может обеспечить все ткани организма одно-
временно максимальным количеством крови, и в норме это никогда не имеет места. В таблице 2 показано,
что физическая работа, которая создает наибольшую
нагрузку на сердце, сопровождается перераспределением крови и ограничением кровотока в участках, ле-
жащих за пределами интенсивно работающих орга-
íîâ.
В системе кровообращения значительная физи-
Таблица 2
Распределение МОК (мл/мин) у людей в состоянии покоя и при нагрузке разной мощности [45]
Органы |
Состояние |
|
Мощность нагрузки |
||
|
покоя |
легкая |
|
средняя |
максимальная |
|
|
|
|
|
|
Скелетные |
1200 |
4500 |
|
12500 |
22000 |
мышцы |
|
|
|
|
|
|
|
|
|
|
|
Сердце |
250 |
350 |
|
750 |
1000 |
|
|
|
|
|
|
Ìîçã |
750 |
750 |
|
750 |
750 |
|
|
|
|
|
|
Почки |
1100 |
900 |
|
600 |
250 |
|
|
|
|
|
|
Органы |
|
|
|
|
|
брюшной |
1400 |
1100 |
|
600 |
300 |
полости |
|
|
|
|
|
|
|
|
|
|
|
Êîæà |
500 |
150 |
|
190 |
600 |
|
|
|
|
|
|
ческая нагрузка вызывает параллельное развитие двух процессов:
а) массивную вазодилатацию в работающих мышцах;
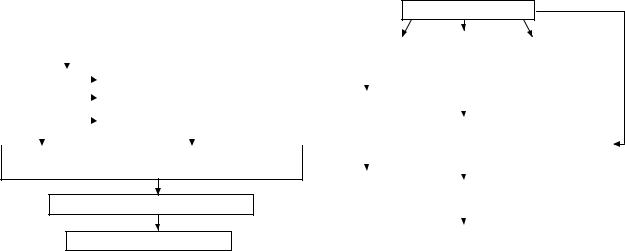
б) напряжение механизмов обеспечения необходимого уровня среднего динамического АД для под-
держания адекватного возросшему метаболизму уровня перфузии работающей мускулатуры. При
этом повышение системного АД обусловлено как
афферентацией с работающих мышц, так и центрогенными эфферентными импульсами (рис. 39).
Возрастание утилизации кислорода при физической нагрузке достигается следующими путями:
1)повышением МОК за счет учащения пульса и более динамичных сокращений желудочков сердца;
2)перераспределением объема циркулирующей крови;
3)увеличением экстракции кислорода из крови работающими тканями.
Кора головного |
Физическая нагрузка |
|
||||
|
мозга |
|
|
|
|
|
|
Центральная |
Метаболизм скелетной мышцы |
||||
|
|
|
|
|
||
|
команда |
|
|
|
|
|
|
Накопление сосудорас- |
Теплопродукция |
||||
|
ширяющих метаболитов |
|
|
|||
|
в скелетных мышцах |
|
Температура |
|||
|
|
|
|
|||
|
|
|
|
гипоталамуса |
||
|
Подъем |
Сопротивление сосудов |
блокирующийПуть,симпатические толькоимпульсык сосудам кожи |
Холинергические симпатическиенервы (активизирующиесяпо мере необходимости) |
||
|
артериальных |
|||||
|
|
скелетных мышц |
|
|
||
|
Активности |
|
|
|
|
|
|
хеморецепто- |
Общее периферическое |
|
|
||
|
ров скелетных |
сопротивление |
|
|
||
|
ìûøö |
|
|
|
|
|
|
|
Артериальное давление |
|
|
||
|
|
ниже “установочной точки” |
|
|||
|
|
Частота |
|
|
||
|
|
импульсации |
|
|
||
|
“установочной |
барорецепторов |
|
|
||
|
точки” |
|
|
|
Активность |
|
|
|
|
|
|
||
|
|
|
|
|
потовых |
|
Сосудодвигательный центр продолговатого мозга |
желез |
|||||
Парасимпатическая Симпатическая |
Симпатическая |
Локальный механизм |
||||
активность |
активность |
активность |
|
|||
×CC |
Сократительная |
Сужение |
Сужение |
Сужение |
Сужение |
|
способность |
âåí |
артериол |
âåí |
артериол |
||
|
||||||
|
Сердце |
Органы тела |
Êîæà |
|||
Ðèñ. 39. Механизмы регуляции функции сердечно-сосудистой системы при физической нагрузке [17]

56 |
Глава 1. ФИЗИОЛОГИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ. ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ... |
Срочная вазодилатация – основной адекватный
механизм компенсации кислородного снабжения клеток при любых стрессорных ситуациях и гемоди-
намических сдвигах. При этом главное значение в
происхождении функциональной гиперемии придается местным метаболическим факторам [52, 59].
Одновременно с проприорецепторов мышц по
центральному и рефлекторному путям повышается эфферентная симпатическая активность. Вызванная
этими влияниями адренергическая вазоконстрикция
распространяется на сосуды кожи и брюшной полости. Надо подчеркнуть, что в работающих мышцах
симпатической вазоконстрикции противостоит мета-
болический механизм так называемого функционального симпатолиза. Все это ведет к перераспределению
МОК и его увеличению по закону Франка–Старлин-
га, так как одновременно увеличивается и венозный возврат крови к сердцу. Последнее обусловлено уве-
личением мышечного кровотока, констрикцией ем-
костных сосудов и мобилизацией в кровообращение депонированного объема крови [59].
Изложенное представляет классическую схему
основных гемодинамических сдвигов при физической нагрузке (см. рис. 39). В этой схеме очевидны
целесообразность и функциональная значимость
каждого из ее компонентов, относящихся как к сердечным (центральным), так и к сосудистым (перифе-
рическим) изменениям. Однако не следует забывать,
что в физиологических условиях именно вазодилатация является основным способом адаптации крово-
снабжения к повышенной функции органа.
Особенно ярко эта особенность проявляется в сердце. Поскольку из коронарной крови извлекается
до 75% всего кислорода даже в условиях покоя, уве-
личение доставки кислорода к миокарду может осуществляться, как правило, лишь за счет усиления кро-
вотока в венечных артериях. И всякий раз, когда кро-
воток недостаточен по сравнению с потребностями сердца в кислороде, развивается ишемия миокарда.
1.4. ПАТОГЕНЕЗ И ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА
Ишемическая болезнь сердца (ÈÁÑ) – нарушение
его функции под влиянием недостаточного кровоснабжения – проявляется болью в предсердечной
области (стенокардией), аритмиями, некрозом участ-
ка миокарда, сердечной недостаточностью. Иногда ИБС протекает бессимптомно, то есть не сопровож-
дается ощущением нездоровья.
Коронарная недостаточность характеризуется несоответствием притока кислорода и субстратов мета-
болизма по венечным артериям к миокарду и потреб-
Таблица 3
Наиболее частые причины коронарной недостаточности
Заболевания и патологические состояния, сужающие венечные артерии:
–Атеросклероз
–Спазм коронарных артерий
–Васкулит
Врожденные и приобретенные пороки сердца:
–Аортальные стеноз и недостаточность
–Митральные стеноз и недостаточность
–Стеноз легочной артерии
Кардиомиопатии
Гипертрофия миокарда
Артериальная гипертония
Сердечные тахиаритмии
Генетически обусловленные сужения просвета венечных артерий и гипоксия миокарда:
–Врожденные аномалии коронарных артерий
–Цианотические врожденные пороки сердца
–Коарктация аорты
ности в них. Причины коронарной недостаточности
условно можно разделить на две группы: коронарогенные и некоронарогенные (табл. 3). Наиболее час-
тыми и значимыми причинами, обусловливающими
снижение коронарного кровотока, являются фиксированный стеноз артерий миокарда вследствие ате-
росклеротического поражения, внутрисосудистая аг-
регация форменных элементов крови и образование тромба, а также спазм венечных артерий сердца [60–
62].
1.4.1. Атеросклероз венечных артерий – морфологическая основа ишемической болезни сердца
Согласно определению Всемирной организации здравоохранения, «атеросклероз – это вариабельная
комбинация изменений в интиме артерий, включа- ющая очаговое накопление липидов, сложных угле-
водов, крови и кровяных веществ, фиброзной ткани,
кальциевых отложений и связанная с изменением средней оболочки (медии)». Однако это определение
отражает лишь морфологическую сущность атеро-
склероза и не затрагивает патогенетических аспектов заболевания.
С учетом современных данных, полученных на
клеточном и молекулярном уровне, более правильным будет рассматривать атеросклероз как «хрони-
ческое очаговое поражение артерий, характеризую-
1.4. Патогенез и патофизиология коронарной ишемической болезни сердца |
57 |
щееся отложением и накоплением во внутренней обо-
лочке сосуда апопротеин В-содержащих липопротеинов и доставляемого ими холестерина и сопровож-
дающееся как структурно-клеточными изменениями,
так и реактивным разрастанием соединительной ткани с образованием фиброзных бляшек в артериаль-
ной стенке» [63, 64]. Этим определением подчерки-
вается, что атеросклероз – это болезнь, которая протекает длительно; первичным субстратом, вызываю-
щим морфологические изменения, свойственные ате-
росклерозу, является холестерин, поставляемый липопротеинами, а завершающим морфологическим
элементом атеросклеротического поражения служит
фиброзная бляшка.
Здесь же надо указать, что в строгом клиническом смысле атеросклероз определяется только наличием
анатомических нарушений артериальной стенки, вызывающих ухудшение кровоснабжения органов и тка-
íåé.
Заслуживает внимания тот факт, что атеросклероз принадлежит к числу немногих заболеваний, в отно-
шении этиологии и патогенеза которых выдвинуто
такое большое количество теорий, гипотез и догадок, что одно их перечисление заняло бы немало места.
Наряду с дискуссионными вопросами об этиоло-
гии атеросклероза, роль холестерина в его патогенезе не оспаривается, однако взгляды Н.Н. Аничкова и
других первых исследователей проблемы атероскле-
роза подверглись существенной ревизии.
В настоящее время установлено, что по крайней мере четыре ведущих механизма способны вызвать характерные для атеросклероза изменения сосудов:
1)дислипидемия;
2)изменение состояния сосудистой стенки;
3)особенности функционирования клеточного рецепторного аппарата;
4)генетический, наследственный фактор [65].
При этом в развитии атеросклероза наиболее изу- чено значение дислипидемии.
Атерогенные изменения состава липидов плазмы крови
Основными липидами плазмы крови являются эфиры холестерина, триглицериды, фосфолипиды и
свободные жирные кислоты. Синтез холестерина осу-
ществляется в печеночных клетках из ацетата, кроме того, часть холестерина поступает в организм из пи-
щи. Триглицериды – это эфиры жирных кислот и гли-
церина. Основная часть триглицеридов синтезируется в печени, откуда они поступают в кровь в составе
липопротеинов очень низкой плотности, незначи-
тельное количество триглицеридов синтезируется в слизистой оболочке кишечника из эндогенных жир-
ных кислот. В крови триглицериды циркулируют в составе самых крупных частиц липопротеинов – хи-
ломикронов – и используются преимущественно жи-
ровой тканью для синтеза жира.
Холестерин циркулирует в крови в виде макромолекулярных компонентов – липопротеинов, имею-
щих различную плотность. Максимальное количество холестерина содержат липопротеины низкой плотно-
сти (ЛПНП), значительно меньше – очень низкой
(ЛПОНП), промежуточной (ЛППП) и высокой (ЛПВП) плотности [64, 65]. Синтезированный в пе-
чени холестерин поступает в кровь в составе ЛПОНП,
где под влиянием липопротеинлипазы ЛПОНП расщепляются до ЛППП; последние захватываются пе-
ченочными клетками и периферическими тканями,
в том числе макрофагами.
Поступление ЛППП и ЛПНП в печеночную клетку – рецептор-опосредованный процесс. Количество
рецепторов в печеночной клетке в значительной мере генетически детерминировано, и при их недостатке
возникает один из вариантов наследственной гипер-
холестеринемии. В печени из ЛПНП образуются ЛПВП, значительная часть холестерина ЛПНП и
ЛППП метаболизируется до желчных кислот.
Из всех липопротеинов наиболее атерогенными являются ЛПНП, тогда как ЛПВП обладают антиате-
рогенным действием, поскольку при поступлении в
макрофаг они способны захватывать холестерин и выводить его из клетки [62, 64, 66].
Основная функция липопротеинов – транспорт
липидов и доставка их в нужный момент в органы и ткани в соответствии с их энергетическими и плас-
тическими потребностями. В этом процессе проис-
ходит целый ряд сложных превращений липопротеинов, в которых принимают участие компоненты кро-
ви и клеток, в том числе ферменты и рецепторы кле-
точных мембран.
В настоящее время хорошо разработаны нормативы содержания липидов и липопротеинов в плаз-
ме крови здоровых людей разного возраста. Однако необходимо иметь в виду, что в эпидемиологических
исследованиях только использование стандартных
методов позволяет получить сравнимые значения уровней липидов и показателей, соответствующих их
нормативам в репрезентативных выборках мужчин и
женщин в данной географической зоне [67]. Изучение различных типов нарушения обмена ли-
пидов, идентификация и классификация их, опреде-
ление вклада различных генов в развитие атеросклероза и его семейных (наследственных) форм явилось
значительным достижением фундаментальной науки.
К настоящему времени установлено, что обмен липидов и липопротеинов в организме контролируют
более 100 генов [68]. Состояния, связанные с нару-
шением этого обмена, получили название дислипопротеинемий (ДЛП).
Дислипопротеинемии и, как частный случай, гиперлипидемии (ГЛП) бывают первичные и вторич-

58 |
Глава 1. ФИЗИОЛОГИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ. ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ... |
ные, обусловленные проявлением других заболева-
ний. Значительную часть составляют первичные ДЛП, связанные с воздействием факторов внешней
среды, а именно, с характером питания. Среди пер-
вичных форм ДЛП наследственно обусловленные составляют 5–7%. Проявление вторичных форм ДЛП
во многом зависит от характера основного заболева-
ния, и при успешном его лечении показатели липидов и липопротеинов нормализуются.
В основу фенотипирования гиперлипидемий,
одобренного Комитетом экспертов ВОЗ [69], легла классификация ГЛП, предложенная Д. Фредриксо-
ном (D. Fredrickson) [70]. Для определения типа ГЛП
применяются методы электрофореза на хроматографической бумаге и в полиакриламидном геле, а так-
же ультрацентрифугирование. Типы ГЛП обознача-
ются римскими цифрами [68–72].
I òèï: гиперхиломикронемия. Синоним: индуцированная жирами липемия. Характерно высокое содер-
жание хиломикронов при нормальном или незначи- тельном повышении уровня ЛПОНП в плазме кро-
ви. Хиломикроны не атерогенны, и при этом типе
ГЛП атеросклероз встречается очень редко.
II òèï: гипер-бета-липопротеинемия. Синонимы: семейная гиперхолестеринемия, множественная бу-
горчатая ксантома. Делится на 2 подтипа: II а – в крови повышено содержание ЛПНП при нормальном со-
держании ЛПОНП; подтип II б – одновременно по-
вышено содержание ЛПНП и ЛПОНП. У пациентов со II типом ГЛП рано развивается атеросклероз, ИБС,
наблюдается отложение ксантом в коже.
III òèï: дис-бета-липопротеинемия. Синонимы: семейная гиперхолестеринемия, индуцированная уг-
леводами гиперлипемия, «флотирующая» бета-гипер-
липемия. При III типе ГЛП отмечается высокая частота атеросклеротического поражения всего сосуди-
стого русла, включая периферические артерии. Кли-
нические признаки атеросклероза проявляются у лиц старше 20 лет поражением сердечно-сосудистой сис-
темы, ксантоматозом век и ладоней; характерно раз-
витие ожирения и диабета.
IV òèï: гипер-пре-бета-липопротеинемия.Синони- мы: индуцированная углеводами липемия, семейная
эссенциальная гиперлипидемия. В крови повышен уровень ЛПОНП при нормальном или сниженном со-
держании ЛПНП и отсутствии хиломикронов. Кли-
нические проявления IV типа ГЛП не являются строго специфичными: при нем могут наблюдаться пораже-
ния как коронарных, так и периферических артерий.
При IV типе ГЛП атеросклероз развивается медленнее, чем при II и III типах, и его клинические прояв-
ления наблюдаются чаще у взрослых и пожилых лю-
äåé.
V òèï: гиперхиломикронемия и гипер-бета-липопро- теинемия. Синоним: комбинированная липемия, вызванная нарушением обмена как жиров, так и углево-
дов. В крови отмечается наличие хиломикронов и по-
вышение концентрации ЛПОНП. Для клиники характерно сочетания диабета и ожирения, клинические
проявления сходны с таковыми при I типе ГЛП. Час-
тота V типа ГЛП в популяции не превышает 1% [68]. Фенотипирование ГЛП позволило обнаружить
связь нарушений обмена липопротеинов с развити-
ем атеросклероза и выделить наиболее атерогенные типы ГЛП. Однако, к сожалению, в приведенной
выше классификации не приняты во внимание сдви-
ги во фракции ЛПВП, полиморфизм апопротеинов и атерогенная самостоятельная фракция липопроте-
èíà (à) [64, 72–74].
Обнаружение антиатерогенной роли ЛПВП [75, 76] – пожалуй, одно из наиболее ярких открытий в
области атеросклероза – способствовало расшире-
нию представлений о нарушениях в обмене липопротеинов и привело к новому понятию о дислипо-
протеинемиях как отклонениях от нормы в липопро-
теиновом спектре крови, встречающихся у людей и проявляющихся в изменении содержания (увеличе-
нии, снижении, отсутствии) одного или более клас-
сов липопротеинов [64].
Сегодня уже ни у кого не вызывает сомнения, что накопление в интиме артерии плазменных ЛПНП,
ЛПОНП и их ремнантных частиц является необходимым условием развития атеросклеротического про-
цесса. Однако на пути проникновения атерогенных
липопротеинов из плазмы крови в артериальную стенку первым барьером является эндотелий, покры-
тый тонким защитным слоем – гликокаликсом. В
связи с этим возникает вопрос, каким путем плазменные липопротеины преодолевают эндотелиальный
барьер и проникают в интиму в количествах, доста-
точных для развития атеросклероза?
На основании современных научных данных, пути и механизмы транспорта липопротеинов из плазмы
крови непосредственно в эндотелиальную клетку и субэндотелиальное пространство (интиму) можно
кратко суммировать в виде следующих основных про-
цессов переноса липопротеиновых частиц [64, 66, 72, 77].
–Регулируемый захват ЛПНП посредством специ-
фического рецептор-опосредованного эндоцитоза, который протекает в физиологических условиях и не приводит к накоплению ЛПНП и холестерина в клетке.
–Нерегулируемый эндоцитоз по типу пиноцитоза, в котором выделяют несколько вариантов:
–нерегулируемый рецептор-опосредованный скевенджер-захват модифицированных липопротеинов;
–транспорт липопротеинов через эндотелиальные межклеточные промежутки (каналы);
–проникновение липопротеинов в интиму ар-
1.4. Патогенез и патофизиология коронарной ишемической болезни сердца |
59 |
терии через участки поврежденного эндотелиального покрова.
В атерогенезе не участвует только первый путь транспорта плазменных липопротеинов. В зависимо-
сти от уровня холестерина ЛПНП и ЛПОНП в крови, содержания модифицированных липопротеинов,
продолжительности гиперлипидемии, наличия тех
или иных гемодинамических, гормональных, иммунологических нарушений, а также факторов риска, о
которых мы скажем ниже, может превалировать тот
или иной путь транспорта липопротеинов либо их комбинации.
Усиленное поступление липопротеинов, особен-
но ЛПНП, в артериальную стенку ведет к накоплению холестерина, обладающего склерогенными, спо-
собствующими разрастанию соединительной ткани,
свойствами. Кроме того, имеет место накопление и самих липопротеинов и их комплексов с гликозами-
ногликанами соединительной ткани [78]. Совокуп-
ность перечисленных факторов создает условия для формирования атеросклеротической бляшки при
участии клеточных структур и внеклеточного матрик-
са артерий (рис. 40).
Повреждающее действие атерогенных липопротеинов на сосудистую стенку проявляется, прежде все-
го, набуханием и разрыхлением гликокаликса. Он становится оптически менее плотным, его связь с по-
верхностью эндотелия становится неоднородной и
рыхлой. Эта реакция протекает однотипно вдоль всего эндотелиального слоя.
Следующим этапом является полное исчезнове-
ние гликокаликса с поверхности эндотелия и прилипание в этих участках к эндотелиальным клеткам
фибрина и тромбоцитов с высвобождением из пос-
ледних большого количества биологически активных веществ. Поступление при этом в кровоток тромбо-
цитарного аденозинтрифосфата ведет к локальному
|
|
|
|
Гиперлипидемия |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Атеросклероти- |
|
|
|
Прямое повреждение кардиомиоцитов |
|||||
|
|
|
|||||||
ческое |
|
|
|
|
|
|
|
||
|
|
|
Гемореология и система гемостаза |
||||||
поражение |
|
|
|
|
|||||
|
|
|
|
|
|
|
|||
сосудов |
|
|
|
|
Кислород-транспортная функция крови |
||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Изменения системной и регионарной гемодинамики, микроциркуляции и транскапиллярной диффузии
Ишемия, дистрофия, некроз, склероз
Клинические проявления
Ðèñ. 40. Механизмы участия гиперлипидемии в патогенезе атеросклероза
и активному притоку тромбоцитов к месту повреж-
дения, усилению агрегации тромбоцитов, а тромбоцитарные агрегаты, как установлено, сами способны
приводить к повреждению сосудистой стенки, к воз-
никновению и росту пристеночного тромба [50, 61, 79].
Участие тромбоцитов в атерогенезе описывается несколькими возможными механизмами (рис. 41).
–Активный захват липидов крови с последующим быстрым образованием тромбоцитарных агрега-
тов и появлением в связи с этим выраженных внутрисосудистых микроциркуляторных нарушений.
–Превращение в атеросклеротическую бляшку пристеночного тромба, образующегося при любом – механическом, токсическом, иммунном, воспалительном – повреждении эндотелия артерий.
–Повреждающее сосудистый эндотелий действие тромбоцитарных агрегатов.
–Создание благоприятных условий для отложения липидов в сосудистой стенке вследствие повыше-
ния ее проницаемости под влиянием биологически активных веществ (гистамина, серотонина, адреналина, тромбоксана и др.), выделяющихся из тромбоцитов.
Âсравнительно недавних исследованиях установ-
лено, что атеросклероз по многим признакам подобен хроническому воспалительному процессу [80, 81].
Тлеющему воспалению в атеросклеротической бляш-
ке могут, в частности, способствовать окисленные липопротеины. К другим факторам, поддерживающим
этот процесс, относятся возбудители инфекции (ви-
русы, хламидии) и аутоантигены, например, белки теплового шока. Активированные Т-клетки секрети-
Тромбоциты
|
|
|
|
Образование |
|
|
|
|
Фагоцитоз и |
|
|
|
|
Повреждение |
|||
|
|
пристеночного |
|
|||||
транспорт жиров |
|
|
|
|
эндотелия |
|||
|
|
|
|
тромба на месте |
|
|
||
|
|
|
|
поврежденного |
|
артерии |
||
|
|
|
|
|
|
тромбоцитарным |
||
|
|
|
|
эндотелия |
|
|||
|
|
|
|
|
|
и агрегантами |
||
|
|
|
|
артерии |
|
|||
Вниутрисосудистая |
|
|||||||
|
|
|
|
|
|
|
||
агрегация |
|
|
|
|
|
|
|
|
тромбоцитов |
|
|
Эволюция и |
|
Усиление |
|||
|
|
|
|
пристеночное |
|
сосудистой |
||
|
|
|
|
|
|
|||
|
|
|
|
утолщение |
|
проницаемости |
||
|
|
|
|
|
|
|
|
под влиянием |
|
|
|
|
|
|
|
|
биологически |
Нарушение |
|
|
|
|
|
активных |
||
микроциркуляции |
|
|
Инфильтрация |
|
веществ, |
|||
|
|
|
|
жирами |
|
|
выделяемых из |
|
|
|
|
||||||
|
|
|
|
|
|
|
тромбоцитов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Атеросклеротическая |
|
|
|
|
|
|
|
|
бляшка |
|
|
|
|
Ðèñ. 41. Механизмы участия тромбоцитов в патогенезе атеросклероза

60 |
Глава 1. ФИЗИОЛОГИЯ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ. ПАТОФИЗИОЛОГИЯ КОРОНАРНОЙ НЕДОСТАТОЧНОСТИ... |
руют в бляшки гамма-интерферон, который наруша-
ет синтез коллагена, а гладкомышечные клетки и активированные макрофаги высвобождают ферменты,
ослабляющие соединительнотканную основу атеро-
склеротической бляшки, способствуя ее разрыву и, в конечном итоге, образованию тромба. Эти данные
служат основой для клинических исследований про-
филактической терапии противоспалительными средствами.
По мнению В.Н. Титова, функциональное едине-
ние реакции воспаления и синдрома атеросклероза снимает с повестки дня вопрос: что в атеросклерозе
первично – липидная инфильтрация или воспаление.
Детальный анализ приводит нас к дуалистической точке зрения, согласно которой инфильтрация липи-
дами может предшествовать воспалению и являться
следствием воспаления [81].
И все же, несмотря на разнообразие гипотез и теорий, окончательный вопрос о том, быть или не быть
атеросклерозу, определяется взаимоотношениями атерогенных липопротеинов с артериальной стенкой.
При этом способствовать развитию дислипопротеи-
немии или нарушению эндотелиального покрова может великое число внешних и внутренних факторов,
и в каждом конкретном случае может наблюдаться
различное их сочетание, но основу патогенетического звена атеросклероза составляет накопление холес-
терина в стенке артерии.
Факторы риска атеросклероза и ИБС
Под термином «фактор риска» понимают определенные индивидуальные характеристики и особенно-
сти образа жизни, повышающие вероятность разви-
тия того или иного заболевания.
Многочисленные эпидемиологические, клини- ческие и экспериментальные исследования позволи-
ли выделить факторы риска атеросклероза и ИБС, которые можно разделить на две группы: факторы, ко-
торые практически невозможно изменить, и факто-
ры, подающиеся влиянию.
Факторами риска, которые изменить невозможно, являются пол, возраст и наследственность. Из-
вестно, что мужчины болеют ИБС чаще, чем женщины. С возрастом риск заболеть ИБС увеличивается и
у мужчин, и у женщин. Лица, чьи ближайшие род-
ственники страдали в молодом возрасте ИБС, особенно, если они перенесли инфаркт миокарда в возрасте
до 50 лет, имеют неблагоприятную наследственность
и повышенный риск заболевания ИБС.
Среди факторов риска, которые можно изменить, наибольшее значение придают гиперхолестеринемии
(или дислипидемии), курению и артериальной гипертензии. Эти факторы риска называют основными, так
как имеется достаточно научных данных, позволяю-
щих считать, что между ними и ИБС прослеживается причинная связь [82]. Самостоятельное влияние дру-
гих факторов – сахарного диабета, ожирения, подаг-
ры, гиподинамии – на развитие ИБС менее доказано.
Дислипопротеинемии (ДЛП) атерогенного типа в
виде повышения содержания в крови холестерина, ЛПНП и/или снижения уровня ЛПВП являются ос-
новными факторами риска атеросклероза (табл. 4).
Для оценки соотношения атерогенных и антиатерогенных липопротеинов предложены различные рас-
четные коэффициенты. Атерогенные свойства липо-
протеинов крови обратно коррелируют с отношением: общий холестерин / холестерин ЛПВП, которое в
норме должно быть ниже 5. Более высокая величина
этого отношения свидетельствует о повышенном риске и является основанием для коррекции ДЛП даже
при легкой гиперхолестеринемии [72, 83].
Наряду с нарушениями обмена и состава липидной части липопротеинов, важную роль в развитии
ДЛП и, возможно, в атерогенезе играют белковые
компоненты липопротеинов. Апопротеины (или, просто, апо-), как известно, определяют способность
липопротеинов связывать и транспортировать липи-
ды [64, 71, 72]. Показано, что у здоровых лиц отношение апо-AI к апо-В больше единицы, и изменение
этого соотношения является более чувствительным
показателем атерогенных сдвигов липопротеинов [84].
Курение, представляющее собой независимый
фактор, действует синергично с другими факторами риска атеросклероза. Доказано, что никотин и окись
углерода, содержащиеся в табачном дыме, повыша-
ют проницаемость эндотелия артерий для липидов, вызывают спазм коронарных и периферических ар-
терий и, наконец, увеличивая адгезию тромбоцитов,
способствуют тромбообразованию [71, 82, 85].
Артериальная гипертензия относится к числу веду-
|
|
|
|
Таблица 4 |
|
|
|
Атерогенные дислипопротеинемии |
|
|
|
|
|
|
Показатели |
Значение |
|||
|
|
|
|
|
Гиперхолестеринемия |
|
|
||
Общий ХС |
|
>200 ìã/äë, |
5,2 ммоль/л |
|
ÕÑ ËÏÍÏ |
|
>160 ìã/äë, |
4 ммоль/л |
|
|
|
|
|
|
Гипертриглицеридемия |
>200 ìã/äë, |
2,3 ммоль/л |
||
|
|
|
|
|
Гипоальфахолестеринемия |
>39 ìã/äë, |
1 ммоль/л |
||
(ХСЛПВП) |
|
|
|
|
|
|
|
|
|
Соотношение |
|
|
||
Общий ХС |
|
>5 |
|
|
|
ÕÑ-ËÏÂÏ |
|
|
|
|
|
|
|
|
Примечание: перевод значений холестерина (ХС) и триглицеридов (ТГ), вы-
раженных в мг/дл и ммоль/л: |
|
ХС ммоль/л = ХС мг/дл : 38,7; |
ТГ ммоль/л = ТГ мг/дл : 88,5; |
ХС мг/дл = ХС ммоль/л х 38,7; |
ТГ мг/дл = ТГ ммоль/л х 88,5. |
