
3 курс / Патологическая физиология / ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ 2
.pdf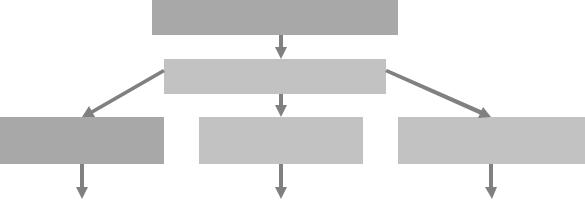
|
|
|
Дефектные эритроциты |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Макрофаги (фагоцитоз) |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пролиферация мак- |
|
|
Непрямой |
|
|
Эритропоэтин |
|
рофагов |
|
|
билирубин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Спленомегалия |
|
|
Желтуха |
|
|
Усиление эритропоэза |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 2. Патогенез нарушений в организме, возникающий вследствие внутриклеточного гемолиза эритроцитов
Классификация гемолитических анемий:
1.По происхождению:
1)Приобретенные:
Иммунные (изоиммунные (ГБН), гетероиммунные, аутоиммунные).
Токсические.
Инфекционные.
Приобретенные мембранопатии (пароксизмальная ночная гемоглобинурия – болезнь Маркиафавы-Микели).
Анемии, обусловленные механическим повреждением эритроцитов.
2)Наследственно обусловленные:
Мембранопатии:
микросфероцитоз (анемия Минковского-Шоффара),
овалоцитоз,
стоматоцитоз,
акантоцитоз.
Ферментопатии:
дефицит ферментов пентозного цикла (глюкозо-6-фосфатдегидрогеназы),
дефицит ферментов гликолиза (пируваткиназы),
дефицит ферментов цикла глутатиона,
дефицит ферментов утилизации АТФ.
Гемоглобинопатии:
качественные (серповидноклеточная анемия),
количественные (α-талассемия, β-талассемия).
2.По причинам гемолиза:
1)анемии, обусловленные экзоэритроцитарными факторами (экстракорпускулярные);
2)анемии, обусловленные эндоэритроцитарными факторами (эндокорпускулярные).
3.По механизмам гемолиза:
1)анемии с внутрисосудистым гемолизом,
2)анемии с внутриклеточным гемолизом.
4.По клиническому течению:
1)острые,
2)хронические.
Основные клинические синдромы гемолитических анемий:
1.Гипоксия. Обусловлена анемией и проявляется резкой слабостью, неприятными ощущениями в области сердца, сердцебиением, одышкой.
51

2.Гемолитическая желтуха.
3.Усиленное образование жёлчных камней, особенно билирубиновых. Объясняется значительным увеличением содержания билирубина в жёлчи и увеличением её вязкости.
4.Гемоглобинурия. Развивается при внутрисосудистом гемолизе. Гемоглобин, который освобождается из разрушенных эритроцитов, связывается белком плазмы крови гаптоглобином. 100 мл плазмы крови содержит столько гаптоглобина, что он может связать 125 мг Hb. Если концентрация Hb в плазме выше 125 мг%, то несвязанный Hb проходит через почечный фильтр и появляется в моче.
5.Спленомегалия. Характерна для внутриклеточного гемолиза эритроцитов. В основе – повышение функциональной активности макрофагов, их активная пролиферация. Спленомегалия часто сопровождается увеличением печени (пролиферация макрофагов).
6.Гемосидероз – отложение гемосидерина в макрофагах. Гемосидерин – это частично денатурированный и депротеинизированный ферритин, т.е. белок, содержащий много железа в негемовой форме (содержание железа в гемосидерине 25-30%).
7.Нарушения микроциркуляции. Часто возникают при интенсивном внутрисосудистом гемолизе и обусловлены развитием ДВС-синдрома.
8.Лихорадка. Развивается в результате резкой активации фагоцитарной функции макрофагов, вследствие чего они выделяют интерлейкин-1.
Периферическая кровь:
Уменьшение количества эритроцитов и концентрации Hb, хотя при внутрисосудистом гемолизе его содержание может не уменьшаться за счёт Hb, находящегося в плазме крови.
ЦП в норме или несколько повышен (в связи с внеэритроцитарным Hb).
Увеличение регенераторных форм эритроцитов (ретикулоцитов, полихроматофилов, нормоцитов).
Красный костный мозг:
Лейкоэритроцитарный индекс 2:1, 1:1, 1:2 (в норме 3:1) – усиленная регенерация клеток красного ростка крови.
Установлено, что здоровый красный КМ может компенсировать 6-8-кратное увеличение темпов разрушения эритроцитов без развития заметной анемии.
Приобретённые гемолитические анемии
Приобретённые гемолитические анемии или анемии от внешних воздействий:
1)токсических веществ (токсическая),
2)инфекционных агентов,
3)иммунных комплексов, в том числе при резус-несовместимости (иммунная),
4)механической травмы (механическая),
5)при гиперспленизме,
6)при приобретённых мембранопатиях (пароксизмальная ночная гемоглобинурия).
Гемолитическая болезнь новорожденных. Возникает в результате гемолиза эритро-
цитов плода и новорожденного, вызванного антителами матери. Наиболее часто встречаются два варианта ГБН – резус (Rh)-конфликт и АВ0-конфликт.
Рис. 3. Механизм развития ГБН при резус (Rh)-конфликте
52
Резус-конфликт развивается в случае Rh-отрицательной матери, беременной Rhположительным плодом. АВ0-конфликт чаще всего возникает в ситуациях, когда мать имеет группу крови 0(I), плод – А(II) или В(III).
Гемолиз эритроцитов внутрисосудистый.
Наследственные гемолитические анемии
Наследственная анемия – когда гемолиз эритроцитов связан с генетическими нарушениями активности ферментов, синтеза гемоглобина или структуры мембран. Поэтому различают: 1) энзимопатии (ферментопатии); 2) гемоглобинопатии; 3) мембранопатии.
Энзимопатии
Энзимопатии обусловлены генетическим дефицитом в эритроцитах глюкозо-6-фосфат- дегидрогеназы, фосфоглицератмутазы, пируваткиназы и др. ферментов. При дефиците глю-козо-6- фосфатдегидрогеназы (Г-6-ФДГ) нарушается пентозофосфатный цикл и не восстанавливается глютатион, вследствие чего повышается проницаемость мембраны эритроцитов для натрия, набухание и внутрисосудистый гемолиз при воздействии лекарств-окислителей (хинин, сульфаниламиды, ацетилсалициловая кислота), а также при употреблении в пищу конских бобов – Vicium favum (поэтому эта анемия называется фавизм). Она наследуется доминантно, сцепленно с X- хромосомой.
Гемоглобинопатии
К гемоглобинопатиям относятся серповидноклеточная анемия и талассемия.
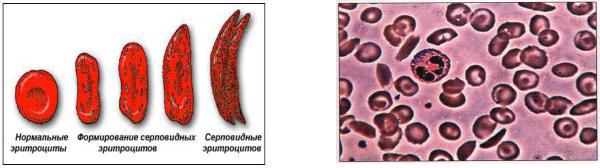
Серповидноклеточная анемия наследуется с неполным доминированием. Вследствие мутации гена, регулирующего синтез нормального гемоглобина (HbA) взрослого человека, синтезируется HbS, в β-цепи которого глютаминовая кислота заменена валином. При гипоксии, ацидозе низкорастворимый восстановленный HbS выпадает в кристаллы, которые деформируют эритроциты (серповидность). Наблюдается массовый распад этих эритроцитов (внутриклеточный гемолиз).
Рис. 4. Формирование серповидных |
Рис. 5. Препарат крови больного с |
эритроцитов |
серповидноклеточной анемией |
Талассемия (болезнь Кули, мишеневидноклеточная гемолитическая анемия, средиземноморская болезнь) характеризуется наследственным нарушением синтеза α- и β-цепочек молекулы Hb. Соответственно различают α- и β-талассемию.
При α-талассемии полностью выключается синтез α-цепей и происходит избыточный синтез β-цепей. Т.е. не могут образовываться все нормальные гемоглобины (А1, А2, и F), синтезируется HbH (тетрамер β-4), который откладывается в виде базофильной пунктации в эритроцитах. У новорожденных, для которых в норме характерен HbF – α2γ2, избыточно образуются γ-цепи, т.е. синтезируется тетрамер γ-4 (гемоглобин Bart). Наследуется аутосомно-доминантно.
При β-талассемии нарушается синтез β-цепей гемоглобина, поэтому не образуется HbA, (в норме у взрослых он преобладает – 96-99%) и компенсаторно избыточно образуется HbF (α2γ2) и HbA2 (α2δ2). Наследуется доминантно.
Клинически бывает: большая (у детей-гомозигот), малая (у детей-гетерозигот).
Характерны мишеневидные эритроциты в периферической крови (центральное расположение гемоглобина), продолжительность их жизни уменьшена до 30 дней, они подвергаются внутриклеточному гемолизу.
53
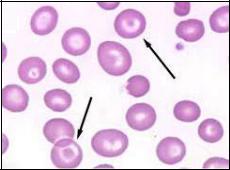
Рис. 6. Препарат крови больного талассемией.
Стрелками указаны мишеневидные эритроциты.
Мембранопатии
Мембранопатии, обусловленные дефектом белковых и липидных компонентов мембран.
Микросфероцитарная гемолитическая анемия (болезнь Минковского-Шоффара).
Наследуется по аутосомно-доминантному типу. Наблюдается наследственный дефект белков мембраны (дефицит в мембране эритроцитов кальций-зависимой АТФ-азы, холестерина,
фосфолипидов ?), что ведет к повышению проницаемости мембраны для натрия и воды, набуханию эритроцитов, превращению их в сфероциты и гемолизу (внутриклеточному). В последующем размеры эритроцита уменьшаются при прохождении (пассаже) через синусоиды селезенки, его мембрана «обтесывается» с поверхности, а эритроцит уменьшается в размерах (микроцитоз), сохраняя сферическую форму. Продолжительность жизни микросфероцитов 8-14 дней (вместо 120).
Может быть деформация черепа, полидактилия, высокое, «готическое», нёбо. Эти изменения обусловлены расширением плацдарма кроветворения, который перемещается в период роста с плоских костей на трубчатые. Кожные покровы и видимые слизистые в разной степени желтушны, что зависит от фазы болезни: гемолитический криз или ремиссия. Увеличена селезенка, иногда и печень; нередки холелитиаз и приступы желчной колики.
Характерна нормохромная анемия, микросфероцитоз. Концентрация Hb вне гемолитического криза сохраняется на уровне 90-100 г/л, а во время криза снижается до 40-50 г/л. Количество ретикулоцитов увеличено как в период ремиссии, так и (особенно) после гемолитического криза - 10-15 и 50-60% соответственно. Тромбоциты в норме, лейкоцитоз в период криза, иногда наблюдается ядерный сдвиг до юных форм; СОЭ увеличена. Осмотическая резистентность (стойкость) эритроцитов понижена: их гемолиз начинается уже в 0,78% растворе натрия хлорида. Содержание свободного билирубина в сыворотке крови увеличено (но не всегда!). Может присоединиться механическая желтуха, обусловленная образованием пигментных желчных камней в желчных протоках; в этих случаях увеличивается содержание обеих фракций билирубина; в моче повышается содержание уробилиногена, а в кале – стеркобилина. Гемолитический криз сопровождается активацией эритропоэза: в пунктате костного мозга выраженная нормобластическая реакция. Описывают отдельные случаи апластического гемолитического криза, когда отсутствует ответная активация эритропоэза, в костном мозге количество клеток эритроидного ростка уменьшено. Чаще такое состояние наблюдается на фоне развившейся инфекции.
54
ЗАНЯТИЕ №3
Тема: ЛЕЙКОЦИТОЗЫ. ЛЕЙКОПЕНИИ. ЛЕЙКОЗЫ
Актуальность темы. Представление о количестве лейкоцитов, соотношении их отдельных форм в периферической крови, а также особенностях их качественных изменений имеет огромное диагностическое значение. Прежде всего, это касается симптоматических изменений лейкоцитарного состава периферической крови, изучение которого является неотъемлемой частью лабораторных исследований при любой патологии. Учет этих показателей в динамике развития заболевания и его лечения очень часто играет важную роль в определении эффективности лечения и прогноза заболевания. Таким образом, знания причин, механизмов возникновения и развития симптоматических изменений лейкоцитарного состава крови, их особенностей при разных патологических процессах и заболеваниях необходимы врачу любой специальности.
Будучи разновидностью гемобластозов, лейкозы представляют собой группу заболеваний системы крови опухолевого характера и потому являются в настоящее время, как и злокачественные опухоли другой локализации, одной из наиболее опасных форм патологии человека. Несмотря на то, что за последние десятилетия медицинская наука внесла значительный вклад в решение вопросов этиологии, патогенеза, диагностики и лечения лейкозов, они дают большой процент смертности, в особенности в детском и молодом возрасте.
Начало лейкозов может сопровождаться такими изменениями в организме, по поводу которых больные могут обратиться к врачу любого профиля. Поэтому знание симптомов этих заболеваний, механизмов их развития, особенностей гематологической картины при разных их формах необходимо каждому врачу.
Общая цель – уметь разобраться в основных количественных и качественных изменениях лейкоцитарного состава крови в условиях патологии, знать возможные причины и механизмы их возникновения и развития, интерпретировать изменения этих данных в диагностическом и прогностическом аспектах различных видов патологии. Уметь дать характеристику лейкозам как разновидности гемобластозов, классифицировать их, объяснять механизмы нарушения кроветворения, количественные и качественные изменения в составе периферической крови, дать характеристику лейкозов при разных формах этого заболевания. Уметь правильно интерпретировать современные основные представления об этиологии и патогенезе лейкозов.
Для этого необходимо уметь (конкретные цели):
1.Различать с общепатологических позиций симптоматические изменения лейкоцитарного состава периферической крови при системных формах ее патологии.
2.Дать характеристику формам изменений лейкоцитарного состава крови симптоматического характера, объяснить их причины, механизм развития и дать классификацию.
3.Оценить данные изменений количества лейкоцитов и лейкоцитарной формулы при различных патологических процессах и заболеваниях, уметь обосновать их диагностическое и прогностическое значение.
4.Охарактеризовать лейкоз как системное заболевание кроветворной системы.
5.Дать современную классификацию лейкозов по гистогенетическому принципу, течению и картине периферической крови.
6.Охарактеризовать основные методики гематологических исследований, использующихся при диагностике лейкозов.
7.Решать вопрос о возможности лейкоза по данным гемограмм.
8.Разобраться в картине изменения периферической крови при лейкозе и распознать разные формы лейкозов.
9.Назвать основные цитохимические показатели, используемые для дифференциальной диагностики лейкозов и дать по ним характеристику основных форм лейкозов.
10.Объяснять механизмы изменений эритроцитарного и тромбоцитарного состава крови при лейкозах.
11.Объяснять механизмы нарушений функций органов и систем при лейкозах.
55
Необходимые для реализации целей обучения базисные знания-навыки. Уметь:
1.Знать основные этапы лейкопоэза и иметь представление о нормальной лейкоцитарной формуле (каф. гистологии, каф. нормальной физиологии).
2.Производить подсчет количества лейкоцитов и знать границы нормальных колебаний этого показателя в крови у человека (каф. нормальной физиологии).
3.Приготовить и окрасить по Романовскому-Гимза мазок крови, знать и распознавать (при его микроскопии) разные формы лейкоцитов, уметь их подсчитывать и рассчитывать абсолютное число каждого вида лейкоцитов (каф. нормальной физиологии).
4.Охарактеризовать основные этапы гемопоэза (каф. нормальной физиологии).
5.Распознавать при микроскопии мазка крови форменные элементы гранулоцитарного, лимфоцитарного, моноцитарного и эритроцитарного рядов (каф. нормальной физиологии).
ВОПРОСЫ К ЗАНЯТИЮ
1.Лейкоцитоз. Механизмы возникновения, классификация.
2.Физиологический лейкоцитоз.
3.Патологический лейкоцитоз. Причины и механизмы развития.
4.Реактивный и перераспределительный лейкоцитоз. Причины и механизмы развития.
5.Варианты лейкоцитоза в зависимости от вида лейкоцитов.
6.Лейкоцитарная формула. Относительный и абсолютный лейкоцитоз и лейкопения.
7.Ядерный сдвиг нейтрофильных лейкоцитов. Виды, причины, их прогностическое значение.
8.Лейкемоидные реакции, их причины и гематологическая характеристика.
9.Лейкопения, принципы классификации.
10.Патогенез основных клинических проявлений лейкопений.
11.Лейкопении вследствие сокращения времени пребывания лейкоцитов в периферической крови и перераспределительные лейкопении. Причины и механизмы развития.
12.Лейкопении вследствие нарушения поступления лейкоцитов из красного КМ в кровь. Причины, механизмы развития.
13.Агранулоцитоз. Причины и механизмы развития.
14.Лейкоз. Этиология и патогенез.
15.Современная классификация лейкозов.
16.Острый лейкоз. Клинические проявления. Патогенез основных клинических синдромов.
17.Хронический лейкоз. Клинические проявления.
18.Стадии острого и хронического лейкоза. Принципы диагностики и лечения.
19.Изменения в гемограмме и миелограмме при лейкозах.
56

ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ ПОДГОТОВКИ К ЗАНЯТИЮ
ЛЕЙКОЦИТОЗЫ. ЛЕЙКОПЕНИИ
Лейкоциты – это клетки крови, отличающиеся сложной структурной организацией, богатым набором ферментов и высокой специализацией.
В норме и при большинстве патологических состояний в периферической крови можно обнаружить пять видов лейкоцитов: нейтрофилы, эозинофилы и базофилы, относящиеся к так называемым гранулоцитам, а также моноциты и лимфоциты (рис. 1).
А |
|
Б |
|
В |
|
|
|
|
|
|
|
|
|
|
Г |
Д |
Рис.1. Лейкоциты в микропрепаратах крови. А – нейтрофил, Б – эозинофил, В – базофил, Г – моноцит, Д – лимфоцит.
Общее количество лейкоцитов в крови взрослого человека в состоянии покоя и натощак составляет 4-9×109/л или 4-9 Г/л (по международной системе единиц (СИ) Г – гига = 109).
Патологические изменения лейкоцитов проявляются:
1)нарушением их образования (лейкопоэза) в кроветворной ткани,
2)количественными изменениями,
3)качественными изменениями.
Главным звеном в патогенезе нарушений при патологии лейкоцитов является изменение реактивности организма, в том числе иммунологической и аллергической, что связано с функциональными особенностями лейкоцитов – их участием в процессах фагоцитоза, антителообразования, инактивации биологически активных веществ (гистамина, серотонина, брадикинина). Патологические изменения лейкоцитов могут сопровождаться трофическими нарушениями тканей, местными микроциркуляторными расстройствами. Это обусловлено тем, что одна из функций лейкоцитов заключается в снабжении регенерирующих тканей питательными веществами и стимуляторами деления клеток. Гранулоциты участвуют в развитии сосудистых нарушений как переносчики вазоактивных веществ (базофилы и эозинофилы) или же влияют на их синтез и высвобождение из тучных клеток (нейтрофилы).
1. НАРУШЕНИЕ ЛЕЙКОПОЭЗА
Выделяют следующие нарушения лейкопоэза: 1) усиление или угнетение образования лейкоцитов в гемопоэтической ткани; 2) нарушение созревания лейкоцитов в кроветворных органах; 3) продукция патологически измененных лейкоцитов.
Причины нарушения лейкопоэза
1. Действие экзогенных факторов:
57

физических (ионизирующее излучение, ультрафиолетовые лучи),
химических,
биологических (бактерии, вирусы, простейшие).
2.Действие эндогенных факторов: генетические нарушения образования и дифференцировки лейкоцитов.
Причины усиления лейкопоэза:
1.Нарушение регуляции образования лейкоцитов:
повышение выработки гуморальных стимуляторов лейкопоэза (колониестимулирующие факторы, КСФ);
уменьшение продукции ингибиторов лейкопоэза (кейлоны, простагландины Е, лактоферрин, изоферритин).
В результате усиливается пролиферация лейкопоэтинчувствительных клеток костного мозга с ускорением их последующей дифференцировки в зрелые лейкоциты.
2.Действие канцерогенных факторов (вызывают мутацию генов, ответственных за размножение и дифференцировку кроветворных клеток II-IV классов, что характерно для лейкоза).
Причины угнетения лейкопоэза:
1.Нарушение регуляции образования лейкоцитов (уменьшение выработки КСФ, увеличение продукции ингибиторов лейкопоэза);
2.Дефицит пластических факторов.
3.Наследственное или приобретённое поражение клеток-предшественников и стромальных клеток;
4.Генерализованное поражение всей лейкопоэтической ткани (наследственная нейтропения, ионизирующее излучение, лейкозные инфильтраты, лекарственная аллергия).
2. НАРУШЕНИЕ СОЗРЕВАНИЯ ЛЕЙКОЦИТОВ
Причины:
1.Мутации (при лейкозах).
2.Действие экзо- и эндогенных факторов (гнойная и вирусная инфекции, интоксикации, лекарственные аллергены).
3.Изменение проницаемости костномозгового барьера (действие глюкокортикоидов).
3. ПРОДУКЦИЯ ПАТОЛОГИЧЕСКИ ИЗМЕНЕННЫХ ЛЕЙКОЦИТОВ
Причины:
1.Опухолевая трансформация лейкопоэтической ткани (при лейкозе, генетически обусловленных нарушениях структуры (пельгеровская аномалия лейкоцитов) и обмена веществ в лейкоцитах).
2.Неэффективный лейкопоэз с укорочением продолжительности жизни лейкоцитов.
Изменения лейкоцитов: качественные (см. выше), количественные.
Количественные изменения лейкоцитов
К ним относятся увеличение (лейкоцитоз) или уменьшение (лейкопения) по сравнению с нормой количества лейкоцитов.
Лейкоцитоз
Лейкоцитоз – это увеличение общего количества лейкоцитов свыше 9∙109/л.
Лейкоцитоз не имеет самостоятельного значения. Он является всего лишь симптомом, сопровождающим развитие многих заболеваний.
58
Механизмы возникновения лейкоцитоза:
1.Усиление лейкопоэза в кроветворных органах.
2.Ускорение выхода лейкоцитов из костного мозга в кровь (вследствие повышения проницаемости костномозгового барьера).
3.Перераспределение лейкоцитов в результате:
их мобилизации из пристеночного (краевого, маргинального) пула в циркулирующий (введение адреналина, эмоциональное напряжение, действие эндотоксинов),
перераспределения крови (шок, коллапс),
повышенной миграции лейкоцитов в очаг воспаления.
Лейкоцитоз часто сочетается с нарушением созревания клеток лейкоцитарного ряда в костном мозге и продукцией патологически измененных лейкоцитов.
Классификация лейкоцитозов:
1.В зависимости от причин развития выделяют физиологические и патологические лейкоцитозы.
2.Лейкоцитоз может быть абсолютным и относительным. Для абсолютного лейкоцитоза характерно увеличение абсолютного количества лейкоцитов в единице объёма крови. Об относительном лейкоцитозе речь идёт в том случае, когда возрастает относительное содержание отдельных форм лейкоцитов в периферической крови.
3.По механизму развития лейкоцитоз бывает: а) реактивным; б) перераспределительным; в) опухолевого происхождения.
4.В зависимости от вида лейкоцитов, содержание которых в крови увеличено, выделяют: а) нейтрофильный лейкоцитоз (нейтрофилёз); б) эозинофильный лейкоцитоз (эозинофилия); в) базофильный лейкоцитоз (базофилия); г) лимфоцитарный лейкоцитоз (лимфоцитоз); д) моноцитарный лейкоцитоз (моноцитоз).
Физиологический лейкоцитоз
Для физиологического лейкоцитоза в большинстве случаев характерно умеренное и относительно кратковременное повышение числа лейкоцитов до 10∙109/л – 12∙109/л, которое через 2-3 часа возвращается к норме. Относительно длительное повышение общего числа лейкоцитов наблюдается у беременных и пациентов, принимающих гормональные препараты (кортикостероиды, АКТГ).
Разновидности физиологического лейкоцитоза:
а) лейкоцитоз новорожденных (количество лейкоцитов в первые 2-е суток составляет 1520∙109/л);
б) алиментарный (пищеварительный) – развивается через 2-3 часа после приема пи-щи; в) миогенный – при мышечном напряжении; г) эмоциональный – вследствие психического возбуждения;
д) лейкоцитоз беременных (с 5-6 месяцев беременности) и рожениц (ко 2-й неделе после родов).
Пищеварительный и миогенный лейкоцитоз – кратковременный, связан с рефлекторным перераспределением крови в сосудистом русле и выходом депонированной крови; а лейкоцитоз новорожденных и беременных – более длительный и обусловлен повышенной функцией миелоидного ростка костного мозга.
Лейкоцитарная формула может также изменяться в зависимости от ряда физиологических условий: характера питания, длительности совершаемой работы и др. Например, углеводы вызывают повышение в крови количества лимфоцитов. Мышечная работа сначала приводит к относительному
59
повышению количества лимфоцитов, переходящему затем в понижение, увеличению нейтрофилов и уменьшению эозинофилов.
Патологический лейкоцитоз:
Причины патологического лейкоцитоза:
1.Острые инфекции (за исключением брюшного и сыпного тифов, паратифов, гриппа, кори и некоторых других вирусных инфекций).
2.Любые острые и хронические (в стадии обострения) воспалительные заболевания, особенно гнойное воспаление.
3.Заболевания, сопровождающиеся распадом тканей (некрозом) (инфаркт миокарда, инсульт, панкреонекроз, инфаркт кишечника, почек, селезенки, обширные ожоги и т. д.) и/или выраженной интоксикацией (уремия, диабетический кетоацидоз и др.).
4.Патологические состояния, для которых характерна выраженная гипоксемия (например, значительные острые кровопотери и др.).
5.Действие токсических веществ (угарный газ, ртуть, дигиталис, хинидин, производные бензола, свинец и др.) или некоторых физических факторов (ионизирующее излучение).
6.Злокачественные новообразования.
7.Острые и хронические лейкозы, сопровождающиеся выраженной пролиферацией одного из ростков кроветворения.
8.Полицитемия.
9.Заболевания, сопровождающиеся иммунными реакциями (коллагенозы, сывороточная болезнь, острый гломерулонефрит и др.).
Механизм этих лейкоцитозов объясняется повышением лейкопоэтической функции костного мозга. Лейкоцитоз в большинстве случаев отражает удовлетворительную реактивность системы костномозгового кроветворения в ответ на действие внешних и внутренних стимуляторов лейкопоэза, хотя следует учитывать и возможность сосудистых реакций, перераспределение кровотока, изменения проницаемости эндотелия, а также пролиферацию ростков кроветворения при лейкозах.
Наиболее выраженный лейкоцитоз встречается при 1) хронических и острых лейкозах и 2) гнойных заболеваниях внутренних органов (абсцесс, гангрена и т. п.). Лейкоцитоз не характерен для брюшного тифа, паратифа, некоторых стадий сыпного тифа, а также для многих вирусных инфекций (грипп, корь, паротит, вирусный гепатит и др.), при которых увеличение количества лейкоцитов в периферической крови свидетельствует о развитии бактериальных и других осложнений. Исключение составляют вирусные заболевания дыхательных путей, оспа и некоторые другие.
Реактивный лейкоцитоз
Реактивный лейкоцитоз возникает как реакция красного КМ на патогенные воздействия. Закономерно развивается при инфекционных заболеваниях, воспалении, действии низких доз токсических веществ.
Механизмы лежащие в основе развития реактивного лейкоцитоза:
1.Усиление пролиферации и созревания лейкоцитов в красном КМ (связано с увеличением образования эритропоэтинов или уменьшением содержания ингибиторов лейкопоэза).
2.Увеличение перехода резервных лейкоцитов из красного КМ в кровь (этому способствуют интерлейкин-1 и бактериальные токсины, повышающие проницаемость стенки кровеносных сосудов красного КМ).
Среди лейкопоэтинов наиболее изученным в настоящее время является колониестимулирующий фактор – вещество, секретируемое активированными макрофагами и стимулирующее образование гранулоцитов в красном КМ.
На роль ингибиторов лейкопоэза претендуют высокомолекулярный ингибитор сыворотки крови – липопротеин, кейлоны и лактоферрин.
60
