
- •Министерство образования российской федерации
- •Функциональная организация иммунной системы
- •1. 1. Основные понятия
- •1.2. Клетки иммунной системы
- •1.3. Молекулы иммунной системы
- •1.4. Иммунные ответы
- •1. T-клеточный ответ с образованием т-клеток воспаления;
- •2. Т-клеточный ответ с образование цитоткосических т-клеток;
- •3. Простой в-клеточный (гуморальный) ответ с синтезом IgM;
- •4. Развёрнутый в-клеточный (гуморальный) ответ
- •Костимулирующие молекулы при иммунном ответе
- •1.4.3. Регуляция иммунных процессов
- •Taблица 4 регуляторные субпопуляции т-лимфоцитов
- •2. Иммунный статус человека
- •2.1. Уровни оценки иммунного статуса
- •2.3. Клиническая оценка иммунограммы Основные правила интерпретации иммунограммы:
- •2.4. Требования к взятию крови для иммунологических исследований
- •2.5. Изменения иммунного статуса при инфекционно-воспалительных процессах
- •3.1. Основные этапы развития иммунной системы плода
- •3.2. Критические периоды функционирования иммунной системы на постнатальном этапе развития
- •Первичные иммунодефицитные состояния (пид).
- •4.1.1. Рабочая классификация первичных иммунодефицитов.
- •4.2.1. Клинико-иммунологическая характеристика вариантов пид
- •Хроническая грануломатозная болезнь
- •4.1.3. Подходы к терапии первичных иммунодефицитов.
- •4.1.4. Общие принципы лечения первичных иммунодефицитов.
- •4.2 Вторичные иммунодефицитные состояния (вид)
- •4.2.1. Этиология вторичных иммунодефицитов.
- •4.2.2. Классификация вторичных иммунодефицитов.
- •Основные правила интерпретации иммунограммы:
- •Инструментальные методы: осуществляется согласно стандартам диагностики и лечения основного заболевания и сопутствующей патологии.
- •Консультации специалистов: проводятся согласно стандартам диагностики и лечения основного заболевания и сопутствующей патологии.
- •4.2.4. Основные алгоритмы нарушений в иммунной системе при вид.
- •1. Вич-инфекция и спид.
- •2. Veb- инфекция.
- •4.2.5. Принципы реабилитации вид.
- •5. Иммунотропная терапия
- •5.1. Классификации иммунотропных препаратов.
- •Препараты, преимущественно оказывающие действие на нейтрофильно- макрофагальную фагоцитарную активность, показатели врожденного иммунитета.
- •5.2. Основные группы иммунотропных препаратов, нашедших применение в клинической практике.
- •5.2.1. Препараты преимущественного действия на т-систему.
- •5.2.2. Препараты, преимущественно воздействующие на пролиферацию и дифференцировку в-лимфоцитов.
- •Миелопид
- •5.2.4. Препараты, преимущественно воздействующие на показатели врожденного иммунитета (макрофагально-нейтрофильный фагоцитоз, цитотоксичность, интерферонопродукцию). Полиоксидоний
- •5.3.Основы заместительной терапии.
- •5.4. Экстракорпоральные методы иммунокоррекциии
- •5.6.Общие рекомендации при назначении иммунотропных препаратов.
- •6. Аллергические заболевания
- •6.2. Патогенез аллергических заболеваний.
- •6.3. Систематизация экзогенных аллергенов
- •1) Аллергены неинфекционного происхождения:
- •2) Аллергены инфекционного происхождения:
- •6.4. Этапы приготовления препаратов аллергенов:
- •6.5. Стандартизация аллергенов
- •6.6. Лечебные аллергены
- •6.7. Подходы к диагностике аллергических заболеваний
- •7. Аллергический ринит.
- •7.1. Классификация ринитов.
- •7.2. Эпидемиология и этиология ринитов.
- •7.3. Симптоматика аллергического ринита.
- •7.4. Патогенез аллергического ринита.
- •Медиаторы аллергических реакций 1 типа
- •7.5. Диагностика аллергического ринита.
- •7.5.1. Оценка степени тяжести заболевания и дифференциальная диагностика.
- •7.6. Лечение аллергическоо ринита.
- •6.1 Элиминация причинно-значимого аллергена.
- •7.6.2. Аллергенспецифичская иммунотерапия (асит).
- •7.6. 4 Ступенчатая схема лечения круглогодичного ринита.
- •2. Легкая форма с непостоянными клиническими проявлениями:
- •7.6.5. Профилактика аллергического ринита.
- •8. Поллинозы.
- •Основные нозологические формы и синдромы пыльцевой аллергии
- •8.3. Критерии диагностики поллинозов.
- •8.4. Ступенчатая схема лечения поллинозов
- •9. Бронхиальная астма
- •9.1. Классификация бронхиальной астмы:
- •Степень тяжести определяется по следующим показателям:
- •9.2. Иммунопатогенез экзогенной (атопической) бронхиальной астмы
- •9.3. Диагностика бронхиальной астмы
- •10. Системные заболевания легких
- •Принято классифицировать эаа по степени выраженности воспаления на:
- •11. Пищевая аллергия.
- •11.1. Классификация и характеристика пищевых аллергенов.
- •11.2. Продукты питания, вызывающие аллергию
- •11.3. Клинические проявления пищевой аллергии
- •11.4. Псевдоаллергические реакции.
- •11.5. Лечение пищевой аллергии.
- •11.6. Атопический дерматит.
- •11.6.1. Классификация атопического дерматита:
- •11.6.2. Принципы терапии атопического дерматита
- •12. Лекарственная аллергия
- •12.1. Современная классификация осложнений медикаментозного лечения
- •12.2. Этиология лекарственной аллергии
- •12.3. Механизмы развития лекарственной аллергии
- •1. Немедленные аллергические реакции.
- •2. Цитотоксические иммунопатологические реакции.
- •3. Иммунокомплексные иммунопатологические реакции.
- •Тяжелые формы лекарственной аллергии с везикобуллезным синдромом
- •12.4. Острая токсико-аллергическая реакця на медикаменты (отар)
- •Клиническая характеристика отар на медикаменты
- •12.5. Классификация проявлений лекарственной аллергии
- •12.6. Перекрестные реакции на лекарства
- •Перекрестные аллергенные свойства лекарственных препаратов
- •12.7. Диагностика лекарственных аллергий
- •11.8. Лечение лекарственной аллергии
- •12.9. Лекарственный анафилактический шок (лафш)
- •11.10. Профилактика лекарственной аллергии
- •13. Аутоимунные заболевания
- •12.1. Систематизация аутоиммунных заболеваний
- •13.2. Иммунопатогенез аутоиммунных заболеваний
- •13.3. Иммунодиагностика аутоиммунных заболеваний
- •13.3. Основные принципы терапии аутоиммунных заболеваний
- •12.5. Аутоиммунный тиреоидит
- •13.6. Ревматоидный артрит
- •14. Клиническая иммунология опухолевого роста
- •14.1. Иммунная система и опухолевый рост.
- •13.2. Механизмы онкогенеза.
- •14.3. Свойства опухолевых клеток
- •14.4. Механизмы противоопухолевого иммунитета.
- •14.5. Механизмы “ускользания” опухолей из-под контроля иммунной системы:
- •14.6. Изменения в иммунном статусе опухоленосителей на разных стадиях опухолевого роста.
- •Наиболее информативные опухолевые маркеры злокачественных новообразований основных локализаций
- •13.8. Современные подходы к иммунотерапии опухолей
- •6. Перечислите основные мероприятия, использующиеся поэтапно при развитии анафилактического шока.
Костимулирующие молекулы при иммунном ответе
|
Клетка |
Молекула |
Функция |
|
Антигенпредставляющие клетки Т-хелпер 1
Т-хелпер 2 В-лимфоцит |
B7.1, B7.2
CD28 CTLA-4 (CD152) OX40L CD40
CD22 |
Лиганды для CD28,CTLA-4
Активационный сигнал Ингибирующий сигнал Активационный сигнал Активационный сигнал на переключение синтеза различных классов антител Ингибирующий сигнал |
Активация клеток (activation) является результатом сигнальной трансдукции, которая осуществляется серией сложных внутриклеточных реакций. После распознавания первоначально наблюдается активация связанных с корецепторами и молекулами CD3 (на Т-клетках) или CD79 (на В-клетках) тирозинкиназ нескольких семейств (Lck, Fyn, Blk, Btk, Lyn, Zap70, Syk и др.), затем через посредничество адаптерных белков включаются сигнальные пути. Один из них связан с активацией фосфолипазы С, образованием инозитолтрифосфата и диацилглицерола, активацией протеинкиназы С и мобилизацией внутриклеточного Ca2+, с транскрипцией гена IL2. Данный цитокин является ключевым ростовым фактором для лимфоцитов при иммунном ответе. Второй сигнальный путь связан с обменом арахидоновой кислоты и приводит к транскрипции генов структурных белков, необходимых для осуществления митозов клеток.
Клональная экспансия (clonal expansion) лимфоцитов представляет собой их бурную пролиферацию, которая протекает в периферических органах иммунной системы. Пролиферирующие В-лимфоциты образуют вторичные фолликулы в лимфатических узлах (центробластная стадия), при этом размножение клеток регулируется рядом цитокинов: IL2, IL4, IL5, IL6, IL10, IL13, IL14, IFN, TNF и др. В последующем центробласты начинают превращаться в центроциты, которые мигрируют на периферию фолликулов (центроцитарная стадия). В этот момент клетки вступают в период соматических гипермутаций, который является своеобразным способом селекции нужной специфичности BCR. Происходит позитивный отбор клеток с высокоспецифичным BCR и негативный отбор В-лимфоцитов с низкоспецифичным рецептором. В процессе созревания (maturation) В-клетки претерпевают морфологические изменения (иммунобласт, затем лимфоплазмоидная клетка и, наконец, плазмоцит) и мигрируют в костный мозг и MALT для синтеза антител различных классов. Синтез ранних антител IgM наблюдается уже к концу первых суток клинического инфекционного эпизода, а высокоспецифических IgG - на 5-7 сутки.
Клональная экспансия и созревание Т-клеток протекает в паракортикальных зонах лимфатических узлов и периартериолярных пространствах селезёнки. Распознавшие антиген клетки вступают в пролиферацию и превращаются в лимфобласты. Клоны CD8+ T-клеток нарастают быстро, а клоны CD4+ Т-лимфоцитов - более медленно. В целом, клональная экспансия и диференцировка регулируются разными цитокинами (IL2, IL7, IL9, IL12, IL15, IFN, TNF и др.) и адгезивными молекулами. В процессе дифференцировки значительно изменяется фенотип Т-лимфоцитов, но, в отличие от В-лимфоцитов, они не меняются морфологически.
Характерным клиническим эквивалентом стадий клональной экспансии и дифференцировки является увеличение периферических лимфатических узлов, миндалин, видимых лимфатических фолликулов и селезёнки. Можно наблюдать эти симптомы при респираторной, урогенитальной или значительной системной инфекциях.
По окончанию иммунного ответа наряду с эффекторными клетками формируются Т- и В-клетки памяти. В отличие от небольших сроков жизни, характерных для эффекторных лимфоцитов, клетки памяти остаются жизнеспособными в течение длительного времени (пожизненно). Существуют CD4+ и CD8+ T-клетки памяти, В-клетки памяти и долгоживущие плазматические клетки. В отличие от наивных Т-лимфоцитов Т-клетки памяти характеризуются фенотипом CD45RO+, CD44hi, быстрым HLA-независимым циклом и способностью секретировать большие количества цитокинов. Долгоживущие плазматические клетки обеспечивают дополнительный механизм поддержания синтеза иммуноглобулинов без дополнительной антигенной стимуляции в течение 1,5 лет.
В
Рис.3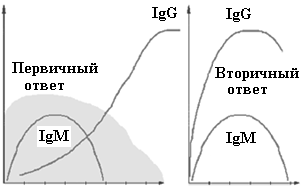
1.4.2. Эффекторные реакции
Физические барьеры (кожа, слизистые оболочки с их мерцательным эпителием, секреты) являются первой линией защиты, часто очень эффективной. Многие патогены могут быть уничтожены с помощью лизоцима, бактерицидных жирных кислот, -дефензина, кислотности желудочного сока и др. Печень представляет собой метаболический барьер для патогенов за счёт моноксигеназной системы(цитохром Р450).
У здоровых людей в сыворотке крови постоянно присутствуют натуральные антитела, представляющие собой IgM, которые направлены против антигенов условно-патогенной флоры. Существуют также каталитические антитела (abzymes), обладающие протеиназной и нуклеазной активностью.
Система естественной цитотоксичности (NK-клетки и интерфероны) обеспечивает экстренную защиту против вирусов и других внутриклеточных патогенов без воспалительной реакции.NK-клетки подвергаютапоптозу(apoptosis) любую клетку в организме, если она не экспрессирует на своей поверхностиHLAI, поэтому мишенями для них являются собственные клетки, инфицированные вирусами, опухолевые, деградирующие и повреждённые клетки. РаспознавHLAIна какой-либо встретившейся клетке,NK-клетка, напротив, получает ингибирующий сигнал и не индуцирует апоптоз этой клетки.
При попадании патогенов в ткань быстро развивается неспецифическое воспаление (nonspecific inflammation). Этот процесс включает острофазную реакцию белков сыворотки крови,активацию комплементапо альтернативному пути инеспецифический фагоцитознейтрофилами и макрофагами. Такое воспаление является острым, не зависит от присутствия антител и сопровождается активацией эндотелия.
Если патогену удаётся миновать врождённый эшелон защиты, на него развивается адаптивный иммунный ответ, следствием которого является включение специфических эффекторных механизмов, направленных на деструкцию данного патогена (см. Табл. 3). Следует иметь в виду, что иммунное воспаление типа IV (по Gell и Coombs) c иммунологической точки зрения является нормальной эффекторной реакцией на внутриклеточно расположенные патогены. Однако нерегулируемое иммунное воспаление с широким распространением на собственные ткани является безусловным патологическим явлением.
Тaблица 3
TИПЫ СПЕЦИФИЧЕСКИХ ЭФФЕКТОРНЫХ МЕХАНИЗМОВ
|
|
|
1. Связывание антигена в иммунные комплексы и его: a) простая нейтрализация; б) деградация в связи с активацией комплемента по классическому пути; в) опсонизация антителами IgM/IgG и последующий фагоцитоз
|
1. Апоптоз клеток-мишеней, индуцированный CD8+ цитотоксическими Т-клетками
|
|
2. Aнтитело-зависимая клеточная цитотоксичность (AЗКЦ), например, при отторжении трансплантата |
2. Деградация антигена путём индуцированного CD4+ T-эффекторами иммунного воспаления (ГЗТ) с активацией макрофагов и других клеток |
