
- •Основные законы фазового равновесия бинарных систем
- •Введение
- •Диаграммы фазового равновесия бинарных систем
- •Основное уравнение фазового равновесия жидкостьпар
- •Законы Коновалова
- •Законы Вревского
- •Для точки азеотропа из третьего закона Коновалова (уравнение (17)) выразим отношение вторых производных потенциала:
- •С учетом (31) уравнение (30) имеет вид:
- •Задания к практическим занятиям
- •По курсу «Физико-химические основы процессов разделения»
- •Задание 1. Обработка и анализ экспериментальных
- •Данных по парожидкостному равновесию бинарных систем
- •Задание 2. Законы Коновалова
- •Задание 3. Законы Вревского
- •Коэффициенты зависимостей давлений насыщенных паров компонентов от температуры [11]
- •Основная литература
- •Дополнительная литература
- •Условные обозначения
- •Индексы
- •Содержание
- •117571 Москва, пр. Вернадского 86.
Министерство образования Российской Федерации
Московская государственная академия
тонкой химической технологии
им. М. В. Ломоносова
Учебно-научный центр «Наукоемкие химические технологии
органических и неорганических веществ и материалов»
Кафедра химии и технологии
основного органического синтеза
Фролкова А. К., Раева В. М., Серафимов Л. А.
Основные законы фазового равновесия бинарных систем
Методическое пособие
Москва, 2000
ББК
Фролкова А. К., Раева В. М., Серафимов Л. А. Основные законы фазового равновесия бинарных систем - М.: МИТХТ, 2000, 25 с.
Методическое пособие к курсу «Физико-химические основы процессов разделения» предназначено для студентов 4-го курса, проходящих обучение в бакалавриате по направлению 550800 «Химическая технология и биотехнология».
Утверждено Библиотечно – издательской комиссией МИТХТ
в качестве
ББК
МИТХТ им. М. В. Ломоносова, 2000
Введение
Первым этапом при разработке принципиальных технологических схем разделения (ТСР) многокомпонентных смесей в промышленности основного органического синтеза является анализ физикохимических особенностей поведения систем, в том числе и при варьировании внешних условий (температур, давлений). Эти особенности определяют возможность разделения смесей на практически чистые компоненты или фракции заданного состава.
Основным массообменным процессом в производствах основного органического синтеза сегодня является ректификация. Движущая сила данного процесса различие равновесных составов паровой и жидкой фаз. При наличии в разделяемой смеси азеотропов принципиально невозможно выделение при ректификации индивидуальных веществ. Если система зеотропна, но характеризуется незначительной относительной летучестью компонентов, то ее разделение требует значительных энергозатрат. В этих случаях применяют специальные приемы, ориентированные на принцип перераспределения полей концентраций между областями разделения1. В частности, приемы, базирующиеся на варьировании давления в колоннах, сочетании ректификации с расслаиванием, использовании селективных растворителей и др.14.
В курсе «Физико-химические основы процессов разделения» объектами изучения на первом этапе будут наиболее простые бинарные смеси. Методически это объясняется низкой размерностью задачи, возможностью наглядного представления результатов, наличием больших массивов экспериментальных данных для анализа и сравнения поведения систем различных классов и при различных условиях, достаточно простой математической моделью фазового равновесия. Экспериментальные данные бинарных систем непосредственно используются для моделирования равновесий жидкость-пар и жидкость-жидкость в многокомпонентных смесях и расчета процесса ректификации. Знание особенностей поведения бинарных растворов необходимо для выбора адекватной математической модели фазового равновесия, для выбора приема разделении бинарных составляющих многокомпонентной смеси в двухколонных комплексах, расположенных на концах схемы.
Диаграммы фазового равновесия бинарных систем
Состояние двухфазной бинарной системы жидкостьпар определяется двумя независимыми переменными. Парожидкостное равновесие (ПЖР) обычно изучают при постоянном давлении (изобарические условия) или постоянной температуре (изотермические условия). На рис. 1-3 схематически представлены основные типы диаграмм равновесия жидкостьпар бинарных систем. При изучении гомогенных систем (рис. 1) в качестве параметров состояния обычно выбирают температуру, давление и концентрацию одного из компонентов (обычно компонент 1 имеет меньшую температуру кипения). Данные системы являются двухфазными, т. е. состоят из двух фаз: жидкой и паровой.
При ограниченной взаимной растворимости компонентов бинарная система характеризуется наличием областей с тремя равновесными фазами: две жидкие и одна паровая (рис.3). Такая трехфазная система имеет только одну степень свободы, т. е. состояние системы определяется заданием одного из параметров температуры, давления или состава равновесной фазы.
По характеру отклонения от идеального поведения бинарные смеси подразделяются на системы с положительными, отрицательными и смешанными отклонениями 57.
Идеальные системы описываются законом Рауля:
![]() (1)
(1)
Отклонения от
идеальности учитываются введением
соответствующих коэффициентов: активности
(![]() )
для жидкой фазы и летучести (
)
для жидкой фазы и летучести (![]() )
для паровой фазы. Поведение паровой
фазы обычно принимают идеальным (
)
для паровой фазы. Поведение паровой
фазы обычно принимают идеальным (![]() ),
тогда уравнение (1) для реальных систем
имеет вид:
),
тогда уравнение (1) для реальных систем
имеет вид:
![]() (2)
(2)
Для положительных
отклонений
![]() ,
для отрицательных -
,
для отрицательных -![]() ,
для смешанных отклонений
,
для смешанных отклонений![]() имеет
разные знаки.
имеет
разные знаки.
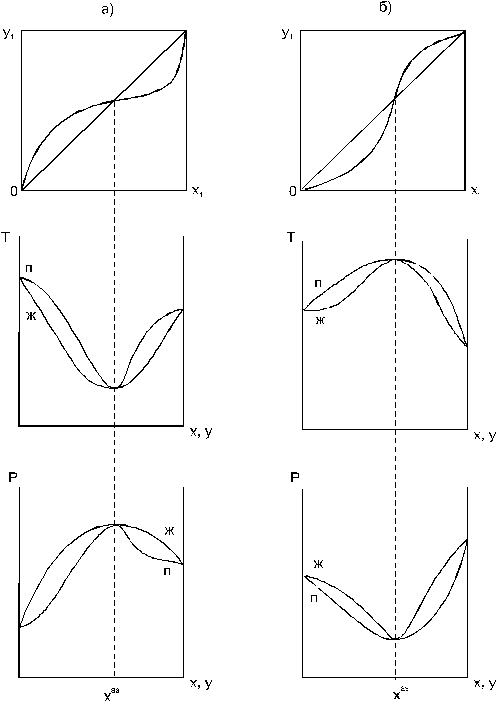
Рис. 1. Диаграммы фазового равновесия жидкостьпар
гомогенных азеотропных систем:
а - положительный азеотроп, б - отрицательный азеотроп.

Рис. 2. Диаграммы фазового равновесия жидкостьпар
зеотропной гомогенной системы.
Бинарные системы можно разделить также на зеотропные (рис. 2, 3а) и азеотропные (рис. 1, 3б-г). Гетероазеотропные системы имеют азеотроп в области сосуществования двух равновесных жидких фаз, который реализуется только при положительных отклонениях от идеального поведения.
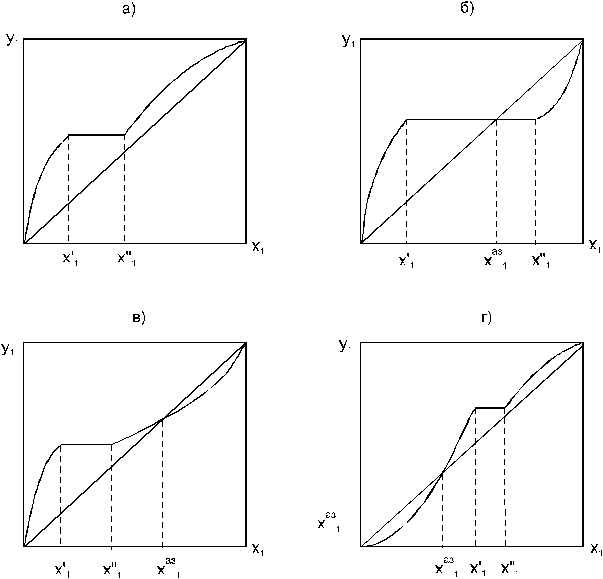
Рис. 3. Диаграммы фазового равновесия бинарных расслаивающихся систем:
а) зеотропная, б) гетероазеотропная, в) с гомогенным азеотропом,
г) со смешанными отклонениями от идеального поведения (расслаивание и отрицательный азеотроп).
Азеотроп
характеризуется равенством составов
паровой и жидкой фаз и наличием экстремума
по температуре (в изобарических условиях)
или давлению (в изотермических условиях),
что вытекает, как будет показано далее,
из первого закона Коновалова. В точке
азеотропа наблюдается равенство единице
коэффициента распределения компонентов
![]() и коэффициента относительной летучести
и коэффициента относительной летучести![]() :
:
![]() (3)
(3)
![]() (4)
(4)
Соотношения (3)-(4) используют для определения параметров азеотропной точки при интерполяции экспериментальных данных по ПЖР.
Результаты обширных исследований азеотропии в бинарных системах представлены в монографии 4-???и справочной литературе810, а также регулярно публикуются в оригинальных научных статьях. В настоящее время открыто явление биазеотропии, когда в бинарной системе присутствуют два азеотропа […], но такие системы в данном курсе подробно не рассматриваются.
