
Свидунович_Материаловедение_для ХТОМ
.pdfМАТЕРИАЛОВЕДЕНИЕ
для студентов специальности
1-48 01 02 Химическая технология органических веществ, материалов и изделий
Лектор |
|
д.т.н., профессор |
Н.А. Свидунович |

СТРОЕНИЕ И СВОЙСТВА МАТЕРИАЛОВ
КРИСТАЛЛИЧЕСКИЕ И АМОРФНЫЕ ТЕЛА
В природе существуют две разновидности твердых тел, различающиеся по своим свойствам, — кристаллические и аморфные.
Кристаллические тела остаются твердыми, т.е. сохраняют приданную им форму до вполне определенной температуры, при которой они переходят в жидкое состояние. При охлаждении процесс идет в обратном направлении. Так, у чистых металлов переход из одного состояния в другое протекает (рис.
1.1) при определенной температуре плавления. |
|
|
|
|
|
|
Аморфные |
тела |
при |
нагреве |
|
|
размягчаются в |
большом |
температурном |
||
|
интервале, становятся вязкими, а затем |
||||
|
переходят в жидкое состояние. При |
||||
|
охлаждении процесс идет в обратном |
||||
|
направлении. |
|
|
|
|
|
Кристаллическое |
состояние |
твердого |
||
тела |
более стабильно, чем аморфное. |
|
|||
|
Аморфные тела в отличие от жидкостей |
||||
|
имеют пониженную |
подвижность |
частиц. |
||
Аморфное состояние можно зафиксировать во многих органических и неорганических веществах ускоренным охлаждением из жидкого состояния. Однако при повторном нагреве, длительной выдержке 20...25° С, а в некоторых случаях при деформации нестабильность аморфного твердого тела проявляется в частичном или полном переходе в кристаллическое состояние.
Примерами такого перехода могут служить помутнение неорганических стекол при нагреве, частичная кристаллизация плавленого янтаря при нагреве, а также резины при растяжении, сопровождающаяся упрочнением.
Кристаллические тела характеризуются упорядоченным расположением в пространстве частиц, из которых они составлены (ионов, атомов, молекул).
Свойства кристаллов зависят от электронного строения атомов и характера взаимодействия их в кристалле, от пространственного расположения частиц, химического состава. Все эти детали строения кристаллов описывает понятие «структура».
В зависимости от размеров структурных составляющих и применяемых методов их выявления используют следующие понятия: тонкая структура, микро- и макроструктура.
Тонкая структура описывает расположение частиц в кристалле и электронов в атоме; изучают ее дифракционными методами (рентгенография, электронография, нейтронография). Анализируя дифракционную картину, получаемую при взаимодействии атомов кристалла с короткими волнами ( λ = 10-10. . . 10-12 м) рентгеновских лучей (или волн электронов, нейтронов),
можно получить обширную информацию о строении кристаллов. Большинство материалов состоит из мелких кристалликов (зерен).
Наблюдать такие мелкие структурные составляющие — микроструктуру можно с помощью оптического (до 10-7 м) или электронного (до 2 • 1 0 — 10 м) микроскопа.
Микроскопические методы дают возможность определить размеры и форму кристаллов, наличие различных по своей природе кристаллов, их распределение и относительные объемные количества, форму инородных включений и микропустот, ориентирование кристаллов, наличие специальных кристаллографических признаков (двойникование, линии скольжения
идр.). Это далеко не полное перечисление характеризует обширность тех сведений, которые можно получить при помощи микроскопа.
Изучая строение кристаллов — макроструктуру — невооруженным глазом или при небольших увеличениях с помощью лупы, можно выявить характер излома, усадочные раковины, поры, размеры и форму крупных кристаллов. Используя специально приготовленные образцы (шлифованные
итравленые), обнаруживают трещины, химическую неоднородность, волокнистость.
Исследование макроструктуры, несмотря на свою простоту, является очень ценным методом изучения материалов.
ЭЛЕМЕНТЫ КРИСТАЛЛОГРАФИИ
КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
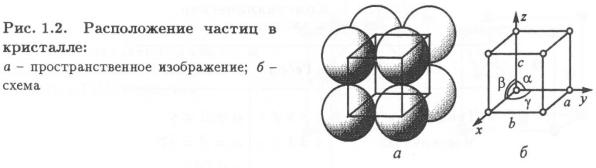
В кристалле частицы (ионы, атомы, молекулы), из которых построен кристалл, сближены до соприкосновения и располагаются различно, но закономерно по разным направлениям (рис.1.2,а). Для упрощения пространственное изображение заменяют схемами (рис. 1.2,б), отмечая точками центры тяжести частиц. Кристаллы различаются симметрией расположения частиц.
Если в кристалле провести три направления х, у, z, не лежащих в одной плоскости, то расстояния между частицами, расположенными по этим направлениям, в общем случае неодинаковы и соответственно равны а, b, с.
Плоскости, параллельные координатным плоскостям, находящиеся на
расстоянии а, b, с разбивают кристалл на множество параллелепипедов, равных и параллельно ориентированных. Наименьший параллелепипед называют элементарной ячейкой. Последовательное перемещение его образует пространственную кристаллическую решетку. Вершины параллелепипеда называют узлами пространственной решетки. С этими узлами совпадают центры тяжести частиц, из которых построен кристалл.
Для описания элементарной ячейки кристаллической решетки используют шесть величин: три отрезка, равные расстояниям а, b, с до ближайших частиц по осям координат, и три угла а, β, γ между этими отрезками.
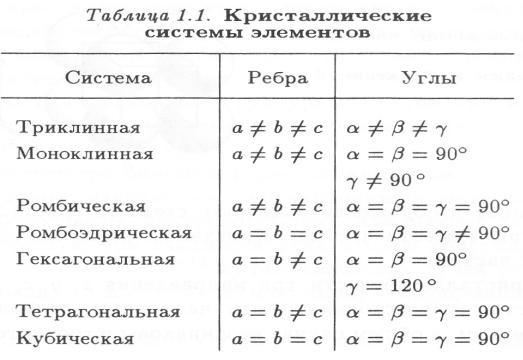
Соотношения между этими величинами определяются симметрией, согласно которой все кристаллы подразделяют на семь систем (табл. 1.1). Размер элементарной ячейки кристаллической решетки оценивают отрезки a, b, с. Их называют периодами решетки.
В большинстве случаев решетки имеют сложное строение, так как частицы находятся не только в узлах, но и на гранях или в центре решетки (рис. 1.3). О степени сложности судят по числу частиц, приходящихся на одну элементарную ячейку. В простой пространственной решетке (см. рис. 1.3, а) всегда на одну ячейку приходится одна частица. В каждой ячейке имеется восемь вершин, но каждая частица в вершине относится, в свою очередь, к восьми ячейкам. Таким образом, от узла на долю каждой ячейки приходится 1/8 объема, а всего узлов в ячейке восемь, следовательно, на ячейку приходится одна частица.

В сложной пространственной решетке на одну ячейку всегда приходится больше одной частицы. На объемно-центрированную ячейку (см. рис. 1.3,в) имеются четыре частицы: одна от вершины и три от шести центрированных плоскостей, так как частица, находящаяся в центре плоскости, относится одновременно к двум ячейкам.
Система, период и число частиц, приходящихся на элементарную ячейку, полностью определяют расположение частиц в кристалле. Дополнительными характеристиками кристаллической решетки являются координационное число и коэффициент компактности.
Число ближайших равноудаленных частиц определяет координационное число К. Например, в решетке объемно-центрированного куба (ОЦК) для каждого атома число таких соседей будет равно восьми (К8). Для простой кубической решетки координационное число будет 6 (Кб), для гранецентрированной кубической решетки (ГЦК) — 12 ( К12).
Отношение объема всех частиц, приходящихся на одну элементарную ячейку, ко всему объему элементарной ячейки определяет коэффициент компактности. Для простой кубической решетки его значение равно 0,52, для ОЦК — 0,68 и для ГЦК — 0,74.
Оставшееся пространство образуют поры, которые подразделяют на октаэдрические и тетраэдрические. На рис. 1.4 центры этих пор показаны маленькими точками на ГЦК решетке. Радиус октаэдрической поры составляет 0,41, а тетраэдрической поры — лишь 0,22 радиуса частицы.
Для многих металлов характерна плотная упаковка частиц. Если частицы изобразить в виде шаров, а для большинства частиц это справедливо, так как они обладают шаровой симметрией, то при упаковке
получаются структуры, показанные на рис. 1.5.
Рис. 1.5. Плотная упаковка атомов в
кристаллах
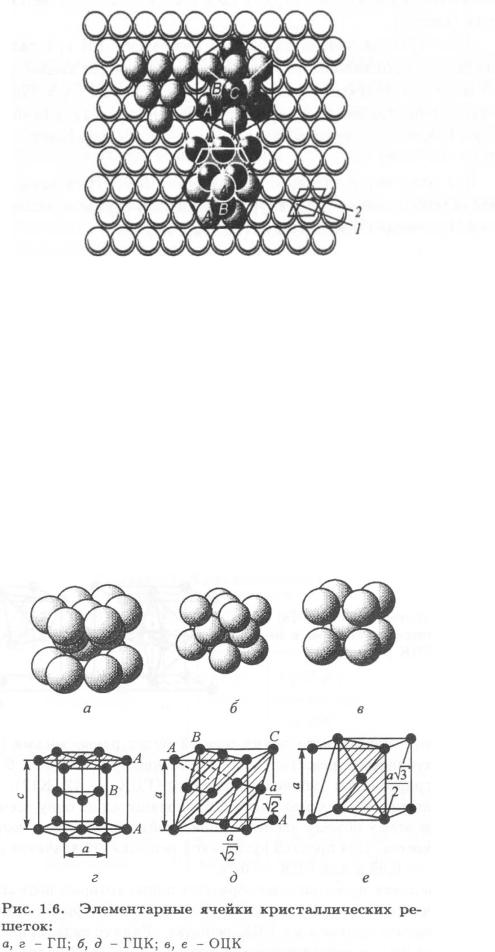
На первый слой шаров, обозначенных А, в лунки 1 накладывается второй слой шаров, обозначенных В. Для следующего слоя шаров возможны два варианта: если шары укладываются над первым слоем, то решетка получается гексагональная плотноупакованная (ГП) (внизу); если третий слой шаров С укладывается на второй над лунками 2 и только четвертый слой повторяет первый слой шаров А, то получается ГЦК решетка (вверху).
Шестигранная призма на рис. 1.6 изображает ГП кристаллическую решетку. Однако элементарной ячейкой здесь является элемент, выделенный жирными линиями. В нем а = b ≠ с ; а = β = 90°; γ = 120°. Исходя из чисто геометрических соображений, можно определить отношение периодов с/а, если частицы обладают сферической симметрией. Оно равно 1,633.
При отклонении частиц от сферической симметрии возможно образование гексагональных структур с отношением периодов, отличающихся от 1,633, а также ОЦК структур (см. рис. 1.6).
КРИСТАЛЛОГРАФИЧЕСКИЕ ИНДЕКСЫ
По параллельным направлениям свойства одинаковы, поэтому достаточно указать для всего семейства параллельных прямых одно направление, проходящее через начало координат. Это дает возможность задать направление прямой только одной точкой, так как другой всегда является начало координат. Такой точкой является узел кристаллической решетки, занимаемый частицей. Координаты этого узла выражают целыми числами и,
v , |
w в единицах отрезков а, b, с, заключают в квадратные скобки [и, v , w ] |
и |
называют индексами направления. Отрицательное значение индекса |
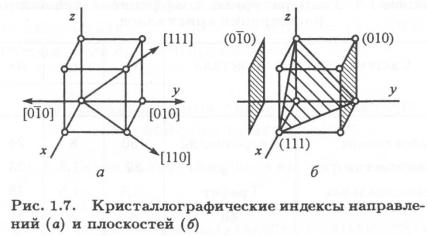
обозначают знаком «минус» над ним (рис. 1.7, а).
Положение плоскости в пространстве определяется отрезками, отсекаемыми плоскостью по координатным осям. Эти отрезки выражают целыми числами т, п, р в единицах отрезков а, b, с. Принято за индексы плоскостей брать обратные отрезки: h = 1/т; к = 1/n; l = 1/р. Три числа h, к, l , заключенные в круглые скобки, называют индексами плоскости (рис. 1.7, 6). Если плоскость отсекает по осям отрицательные отрезки, то это отмечают знаком «минус» над соответствующим индексом.
АНИЗОТРОПИЯ
Анизотропия— это зависимость свойств кристалла от направления, возникающая в результате упорядоченного расположения атомов (ионов, молекул) в пространстве. Свойства кристаллов определяются взаимодействием атомов. В кристалле расстояния между атомами в различных кристаллографических направлениях различны, а поэтому различны и свойства.
Анизотропия присуща многим свойствам кристаллов. Наиболее сильно она проявляется в кристаллах со структурами, обладающими малой симметрией (табл. 1.2).
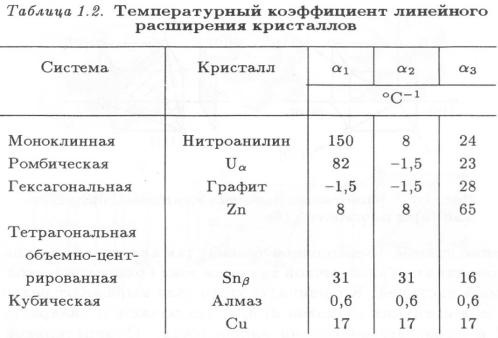
Из приведенных значений температурных коэффициентов линейного расширения в кристаллах по трем координатным осям можно заключить, что анизотропия резко проявляется у моноклинных и ромбических кристаллов и практически незаметна у кубических.
Анизотропия свойств проявляется при использовании монокристаллов, полученных искусственным путем. В природных условиях кристаллические тела — поликристаллы, т.е. состоят из множества мелких различно ориентированных кристаллов. В этом случае анизотропии нет, так как среднестатистическое расстояние между атомами по всем направлениям оказывается примерно одинаковым. В связи с этим поликристаллические тела считают мнимоизотропными. В процессе обработки давлением поликристалла кристаллографические плоскости одного индекса в различных зернах могут ориентироваться параллельно. Такие поликристаллы называют текстурованными и они, подобно монокристаллам, анизотропны.
Ниже приведены значения модуля упругости для моно- и поликристаллов трех металлов, ГПа:
|
Монокристалл* |
Поликристалл |
Сu (ГЦК) ............................. |
68/104 |
121 |
Fe (ОЦК) ............................. |
135/290 |
214 |
Zn (ГП) ............................... |
35/126 |
100 |
* В числителе - минимальное значение, в знаменателе - максимальное. Видно, что значения свойств поликристаллов занимают промежуточ-
ные положения в интервалах значений для монокристаллов.
Прочность и пластичность монокристалла меди изменяются в зависимости от направления (<σв = 350 ... 180 МПа; δ = 10 ... 50 %). Для поликристаллической меди <σв = 250 МПа и δ = 40 %.
ФАЗОВЫЙ СОСТАВ СПЛАВОВ
Термин «сплав» в настоящее время имеет более широкое значение, чем во время его появления. Если раньше промышленные материалы, содержащие несколько элементов, получали преимущественно путем сплавления, то сейчас для этого используют различные технологические способы: порошковую металлургию (прессование твердых частиц и их последующее спекание при высоких температурах), диффузионный метод (проникновение одного вещества в другое твердое вещество при высоких температурах), плазменное напыление, кристаллизацию из паров в вакууме, электролиз и т.д. Преимущественное использование в промышленности находят сплавы металлов с металлами или неметаллами. В сплавах элементы могут поразному взаимодействовать между собой, образуя различные по химическому составу, типу связи и строению кристаллические фазы. Фазой называется однородная, отделенная поверхностью раздела часть металла или сплава, имеющая одинаковые состав, строение и свойства. В зависимости от атомно-кристаллической структуры различают твердые растворы и промежуточные фазы. Твердыми растворами называются кристаллы, в которых сохраняется тип кристаллической решетки элемента-растворителя. В промежуточных фазах образуется новый тип кристаллической решетки, отличающийся от решеток элементов, его образующих.
Таким образом, помимо классификации кристаллов по видам связи используют классификацию по типам кристаллической решетки, которая позволяет прогнозировать характер изменения свойств сплава в зависимости от химического состава.
ТВЕРДЫЕ РАСТВОРЫ
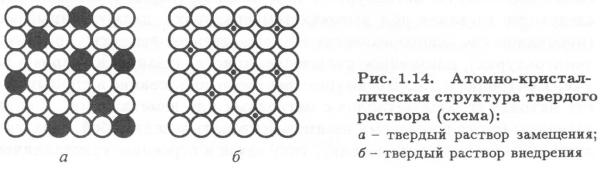
Твердые растворы являются кристаллическими фазами переменного состава. Атомы растворенного элемента В размещаются в кристаллической решетке растворителя — элемента А, замещая атомы в узлах решетки или внедряясь между узлами. В первом случае кристаллы называют твердыми растворами замещения, во втором — твердыми растворами внедрения (рис. 1.14). Количество замещенных атомов, так же как и количество внедренных, может изменяться в широких пределах, что и приводит к переменной растворимости твердых растворов.
Твердые растворы обозначаются буквами греческого алфавита: а, β, γ и т.д. или А(В), где А — растворитель, В — растворенный элемент.

Твердые растворы замещения. Замещение атомов растворителя А атомами растворенного элемента В возможно, если атомные радиусы отличаются не более, чем на 15 %. Это условие называют размерный фактор. В твердых растворах атомы растворенного вещества, как правило, распределяются в решетке растворителя статистически. Вокруг атома растворенного вещества возникают местные искажения пространственной решетки, которые приводят к изменению свойств и среднего периода решетки. Растворение элементов с меньшим атомным радиусом, чем атомный радиус растворителя, вызывает уменьшение среднего периода решетки, а с большим — его увеличение.
Образование твердых растворов всегда сопровождается увеличением электрического сопротивления и уменьшением температурного коэффициента электрического сопротивления; твердые растворы обычно менеепластичны (исключение составляют твердые растворы на основе меди) и всегда более твердые и прочные, чем чистые металлы.
Растворимость элементов в твердом состоянии уменьшается при увеличении различия в атомных радиусах сплавленных элементов и их валентности.
При образовании твердых растворов замещения возможна и неограниченная растворимость элементов в твердом состоянии, т.е. когда при любом количественном соотношении сплавляемых элементов все разнородные атомы размещаются в узлах общей пространственной решетки.
Неограниченная растворимость наблюдается при соблюдении размерного фактора и если элементы имеют одинаковый тип кристаллической решетки. Неограниченная растворимость в твердом состоянии наблюдается в сплавах Cu-Au, Cu-Ni, Ge-Si. В полиморфных металлах встречается неограниченная растворимость в пределах одной модификации пространственной решетки. Например, Feα дает неограниченный ряд твердых растворов с хромом (ОЦК решетки), a Feγ — неограниченный ряд твердых растворов с никелем (ГЦК решетки).
Многие твердые растворы замещения при относительно невысоких температурах способны находиться в упорядоченном состоянии, т.е. вместо статистического распределения разносортных атомов в узлах пространственной решетки атомы одного и другого металла размещаются в совершенно определенном порядке. Такие твердые растворы называются упорядоченными1.
Переход из неупорядоченного в упорядоченное состояние происходит при определенной температуре или в определенном интервале температур. Температура, при которой твердый раствор полностью разупорядочивается, называется точкой Курнакова и обозначается θк. Упорядочение происходит обычно только при медленном охлаждении твердого раствора из температурной области выше θк.
Упорядоченные твердые растворы встречаются в системах с значи-
1 Используется также термин «сверхструктура».
