
Вариант1
.pdfХимия Вариант 1
Вариант 1
1.Основные понятия
1.Получить дигидроксид никеля (основной), доказать его кислотно-основные свойства. Уравнения реакций написать в молекулярной и в сокращенной ионной форме.
2.Подобрать коэффициенты в следующих окислительно-восстановительных реакциях методом электронно-ионного баланса:
MnO2 + KNO3 + KOH → K2MnO4 + KNO2 + H2O
K2Cr2O7 + KI + H2SO4 → K2SO4 + Cr2(SO4)3 + I2 + H2O
3.Получить из хлорида алюминия основную соль, назвать ее. Перевести ее в нормальную соль. Уравнения реакций написать в молекулярной и в сокращенной ионной форме.
2.Количественные расчеты
1.Какой объем 40% раствора ортофосфорной кислоты H3PO4 (ρ=1.25г/см3) необходим для приготовления 400 мл 0.25 М раствора?
2.Какой объем 0.01 Н раствора нитрата серебра AgNO3 потребуется для полного осаждения бромид иона в виде AgBr из 10 мл 10% раствора бромистоводородной кислоты НBr (ρ=1.073 г/см3)?
3.Термодинамика
1.Определить энтальпию образования окиси алюминия (Al2O3), если известно, что при сгорании 1г алюминия в кислороде выделилось 31,03 кДж теплоты.
2.Возможно ли восстановление оксида висмута оксидом углерода при Т = 800 К по
реакции (энтальпии образования ( Hof) и энтропии (So) веществ известны):
|
Bi2O3 + |
3CO |
= |
2Bi + |
3CO2 |
Hof кДж/моль |
-570,70 |
-110,53 |
|
0 |
-393,51 |
So Дж/моль*К |
151,49 197,55 |
56,9 |
|
213,66 |
|
3. Перечислить термодинамические параметры состояния химической системы.
4.Кинетика
1.Как изменится скорость реакции 2А+В → А2В, если при постоянной температуре увеличить концентрацию вещества А в 5 раз, а В в 10 раз. Кинетический порядок реакции по веществу В равен 1, по А – 1.
2.Константа скорости реакции АВ→А+В при 620о С равна 0.72 с-1, а при 600о С - 0.08с-1. Определите температурный коэффициент и константу скорости реакции при 610о С.
3.Кинетические параметры реакции.
5.Равновесие
Химия Вариант 1
1.Какая из перечисленных солей подвергается гидролизу: NaNO3, KCN, KCl, Na2SO4? Рассчитать рН раствора, если концентрация этой соли равна 0.5 моль/л, а константа диссоциации основания равна Ка = 4.9·10-10.
2.Определите рН 2 М раствора азотной кислоты (НNO3), считая, что степень диссоциации кислоты α=0.5.
3.Равновесие реакции Н2 +I2 = 2HI установилось при следующих концентрациях: [H2]=0.5моль/л; [I2]=0.1моль/л; [HI]=1.8моль/л. Определите константу химического равновесия и исходные концентрации иода и водорода. В начальный момент времени
[HI]=0.
4.Рассчитать растворимость сульфата бария (ВaSO4) в г/л, ПР = 1.8·10-10. Как изменится концентрация ионов бария в растворе, если в него добавить Н2SO4 до концентрации 1
моль/л (α=1)?
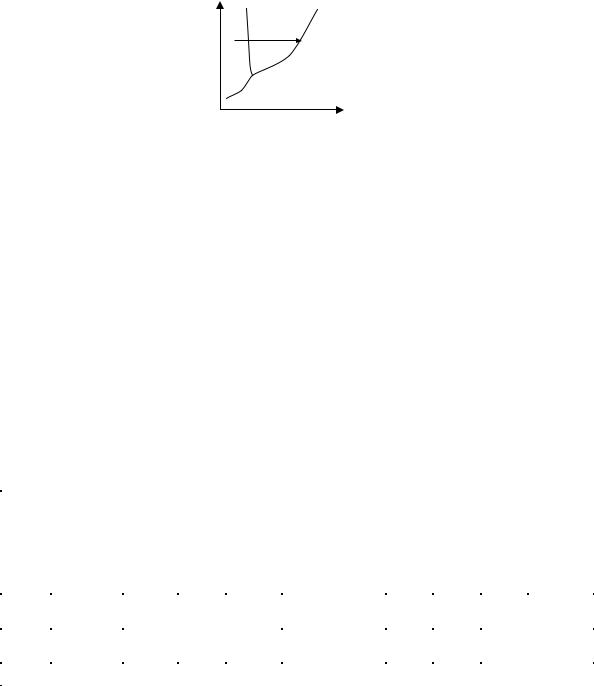
5.Описать переход 1→ 2
1.
2
6.Электрохимия
1.Какие процессы протекают при электрохимической коррозии хромированного железного изделия в водном растворе с рН<7 при нарушении покрытия?
2.Какие коррозионные процессы протекают при хранении изделий из кадмия и свинца во влажной атмосфере, если они соприкасаются друг с другом?
3.Составить гальванический элемент, в котором медь является анодом. Написать уравнения реакций, протекающих на электродах, и вычислить ЭДС в стандартных условиях и при концентрации ионов меди у анода равной 0.001 моль/л.
4.Составить гальванический элемент с серебряным катодом. Написать уравнения реакций, протекающих на электродах при работе этого элемента. Вычислить ЭДС, если концентрация ионов металла у катода равна 0.1 моль/л, а у анода 0.001 моль/л
5.При электролизе водного раствора нитрата калия (KNO3) с инертными электродами на катоде выделилось 2 г вещества. Какое это вещество? Какой продукт, и в каком количестве выделился на аноде?
6.При электролизе водного раствора соли сульфата MeSO4 в течение 12 минут с током 5А на катоде выделилось 2,0966 г этого металла. Определить металл, вычислив его атомную массу. Какой продукт, и в каком количестве выделится на инертном аноде?
|
Осн. |
|
Терм. |
Кин. |
Равн. |
Кол.Х |
ВМС |
Эл.х |
Корр |
Ато |
Хим. |
Хим |
|
понятия |
|
|
|
|
|
|
. |
м |
св. |
.Ан. |
|
ДЗ |
1 |
2 |
3 |
4 |
5 |
- |
- |
6 |
6 |
? |
7, SnCl2 |
- |
|
|
|
|
|
|
|
|
|
|
|
He2 |
|
Лаб. |
1 |
|
- |
2 |
- |
- |
- |
3 |
4 |
- |
- |
? |
|
|
|
|
|
|
|
|
|
|
|
|
|
Конс. |
- |
|
+ |
+ |
+ |
+ |
+ |
- |
- |
+ |
+ |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
Тест |
- |
|
- |
- |
- |
+ |
+ |
- |
- |
+ |
|
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
Тема |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
