
Лекции по ФХ 2 семестр / лекция 7 адс и катализ
.docx
АДСОРБЦИЯ
Адсорбция
—
это самопроизвольное концентрирования
вещества на поверхности раздела фаз.
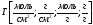
Вещество, на котором происходит адсорбция, называется адсорбентом. Вещество, которое адсорбируется, называется адсорбатом или адсорбтивом.
|
Адсорбция |
|
|
Физическая |
Химическая (хемосорбция) |
|
1. Сила взаимодействия между адсорбентом и адсорбатом слабая физическая или силы Ван-дер-Ваальса. |
1. Химическая связь |
|
2. Обратимая адсорбция адс.↔десорция |
2. Процесс необратим |
|
3. С увеличением температуры возрастает скорость десорбции |
|
ОСОБЕННОСТИ АДСОРБЦИИ НА ТВЕРДОМ КАТАЛИЗАТОРЕ.
ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕОРИИ ЛЕНГМЮРА
1. На поверхности адсорбента имеются активные адсорбционные центры, т.е. участки, на которых происходит адсорбция.
2. Все адсорбционные центры одинаковы.
3. На каждом адсорбционном центре может адсорбируется только одна молекула адсорбата.
4. Адсорбционные молекулы не взаимодействуют друг с другом.
5. Адсорбционные молекулы находятся в динамическом равновесии с молекулами адсорбата, находящимся в среде, из которой происходит поглощение.
При описании адсорбции используют величину θ
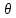 — степень
заполнения поверхности
— степень
заполнения поверхности
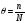 ;
где n
—
число
занятых центров; N
—
общее
число центров.
;
где n
—
число
занятых центров; N
—
общее
число центров.
Скорость адсорбции равна : wадс.=К1С(1- θ)
Скорость десорбции описывается уравнением: wдес.=К2θ
Предположим динамическое равновесие wадс.= wдес.
К1С(1- θ) = К2θ; К1С-К1С θ = К2θ;
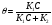 разделим
на К2;
разделим
на К2;
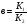
w=КӨ — скорость процесса, лимитируемая адсорбцией.
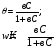
АНАЛИЗ УРАВНЕНИЯ
1.
Если С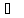 1,
то скорость процесса равна:
1,
то скорость процесса равна:
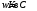 —
кинетическое
уравнение 1 порядка (n=1).
—
кинетическое
уравнение 1 порядка (n=1).
2.
Если С
 1,
то скорость процесса равна:
1,
то скорость процесса равна:

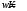 — кинетическое
уравнение 0 порядка (n=0).
— кинетическое
уравнение 0 порядка (n=0).
3. Если Сср, то n= от 0 до 1.
В 1 и 2 случаях используют уравнения Ленгмюра:
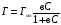 — уравнение
Ленгмюра
— уравнение
Ленгмюра
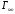 —
адсорбция
насыщения
—
адсорбция
насыщения
Адсорбция насыщения — это процесс полного адсорбирования на всех адсорбционных центрах.

Адсорбция в средних областях концентраций описывается уравнением Фрейндлиха:
 ,
,
где β и n — константы, описывающие данный процесс.
Задача решения уравнения Фрейндлиха сводится к нахождению постоянных β и n. Для этого уравнения логарифмируют и строят график в координатах "lgГ — lgC".
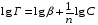

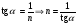 .
.
КАТАЛИЗ
Катализ — явление изменения скорости реакции под действием веществ, называемых катализатором.
Катализатор — вещество, учавствующее в реакции и изменяющее её скорость, но остающееся неизменным после того, как химическая реакция заканчивается.
Катализатор, замедляющий реакцию, называется ингибитором. Биологические катализаторы белковой природы называются ферментами.
|
Катализ |
|
|
Положительный |
Отрицательный |
|
Увеличение скорости реакции |
Уменьшение скорости реакции |
|
Связан с уменьшением ∆H ⃰ |
Связан с уменьшением ∆S ⃰ |
По теории активированного комплекса:
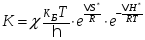
ОСОБЕННОСТИ КАТАЛИЗА
1. Катализатор образует с одним или несколькими реагирующими веществами переходное состояние с гораздо меньшим значением энергии активации, чем значение энергии активации комплекса, образованного исходными веществами, т.е. реакция протекает по иному механизму с другими значениями энергии активации.
Взаимодействие с катализатором может протекать по следующим механизмам: слитному и раздельному.
Для реакции: А+В→АВ ⃰ → АВ,
где АВ ⃰ — активированный комплекс, представим раздельный механизм.
а) Раздельный механизм.
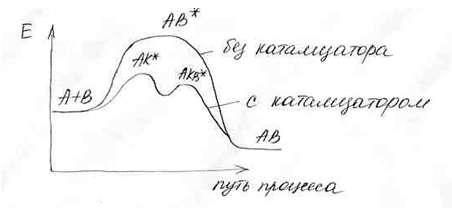
А + К → АК ⃰
АК ⃰ + В → АКВ ⃰
АКВ ⃰ → АВ + К
С катализатором протекает реакция по более энергетически выгодному пути.
б) Слитный механизм.
А+В+К→ АВК ⃰ →АВ+К
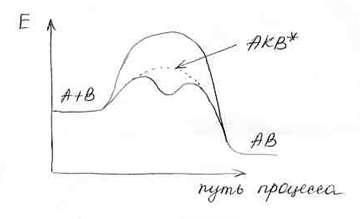
В этом случае также каталитический процесс является более энергетически выгодным.
Действие катализаторов можно оценить величиной, которая называется степенью компенсации æ "каппа" (это понятие ввел Боресков).
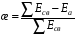 ,
,
где
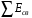 -
сумма энергий связи всех участников
реакции4
-
сумма энергий связи всех участников
реакции4
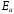 -
энергия активации.
-
энергия активации.
Чем меньше значение энергии активации, тем больше значение æ.
Степень компенсации для:
- некаталитической реакции ≈ 0,5;
- каталитических реакций ≈ 0,8;
- цепных, радикальных реакций — (0,95-0,98).
Скорость любого некаталитического процесса меньше скорости любого каталитического процесса.
СН3СНО(уксусный
альдегид) → СН4
+ СО;
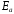 =191,1
кДж/моль
=191,1
кДж/моль
cat — J2 1) СН3СНО + J2 → СН3 J + HJ + СО;
2)
СН3
J
+ HJ
→ СН4
+
J2;
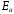 =136,5
кДж/моль
=136,5
кДж/моль
Скорость второй стадии в 10000раз больше скорости первой.
2. Катализаторы обладают свойствами селективного, т.е. катализатор может ускорять какой - либо один из идущих процессов.
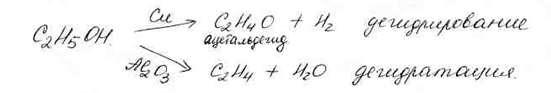
3. Каталитической активностью обладают даже малое количества катализатора (этим они отличаются от исходных веществ).
4. На действие катализаторов влияют различные добавки. Их классифицируют на:
а) усаливающие, или промоторы;
б)ослабляющие, или каталитические яды.
5. Катализаторы не влияют на состояние термодинамического равновесия, они лишь ускоряют момент достижения этого равновесия.
Если ∆G > 0, то с помощью катализатора процесс заставить идти быстрее невозможно.
6. Скорость процесса зависит от количества каталтзатора.
7. По фазовому состоянию катализ делится на следующие типы:
- гомогенный, когда все вещества и катализаторы находятся в одной фазе;
- гетерогенный, когда исходные вещества и катализаторы находятся а разных фазах;
- микрогетерогенный, который в свою очередь, делятся на ферментативный и гельиммобилизованный.
КИНЕТИКА ГОМОГЕННОГО КАТАЛИЗА

По характеру взаимодействия с катализатором все вещества делятся на две группы:
- вещества Аррениуса, которые находятся в термодинамическом равновесии с катализатором;
- вещества Вант-Гоффа, которые не образуют равновесного состояния с катализатором.
ВЫВОД И АНАЛИЗ КИНЕТИЧЕСКИХ УРАВНЕНИЙ С УЧАСТИЕМ ВЕЩЕСТВ АРРЕНИУСА И ВАНТ-ГОФФА
1. Вещества Аррениуса.
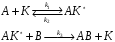

w1=к1СА(СК-САК ⃰ ), где СК - суммарная концентрация катализатора.
w2=к2САК ⃰
т.к. считается, что промежуточное соединение находится а равновесии с исходными веществами, то w1 = w2.
к1САСК - к1САСАК ⃰ - к2 САК ⃰ =0
Выражаем концентрацию промежуточного соединения.
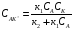
Рассчитаем суммарную скорость реакции.
Основное уравнение для веществ Аррениуса.
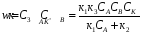
Анализ уравнения:
1)
если к1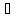 к2,
то
величиной к2
в
знаменателе пренебрегаем и
к2,
то
величиной к2
в
знаменателе пренебрегаем и
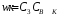
Порядок по катализатору не входит в выражение общего порядка реакции — n=1;
2)
если к1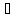 к2,
то имеем
к2,
то имеем
 ,
n=2;
,
n=2;
2. Вещества Вант-Гоффа.
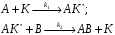
Используя
метод стационарных концентраций
Боденштейна, выводим кинетическое
уравнение:
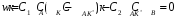
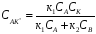 ;
;
 .
.
АНАЛИЗ УРАВНЕНИЯ
1)
если к1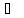 к2,
то
к2,
то
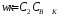 ,
n=1
по веществу В.
,
n=1
по веществу В.
2)
если к1 к2,
то имеем
к2,
то имеем
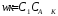 ,
n=1
по веществу А.
,
n=1
по веществу А.
