
- •Специальные технологии художественной обработки материалов. Часть 2 (Технология изготовления художественных изделий обработкой давлением)
- •Оглавление
- •Введение
- •Лекция 1. Из истории обработки металлов давлением
- •1.1. Ковка металлов в древности
- •1.2. Кованые изделия средневековья
- •1.3. Изделия конца хviii - начала хх веков
- •Лекция 2. Элементы теории напряжений и деформаций
- •2.1. Связь между деформацией и напряжением
- •2.2. Плоское напряжённое состояние и плоская деформация
- •2.3. Главные напряжения и их основные схемы
- •2.4. Взаимосвязь обобщенного напряжения и обобщенной деформации. Испытание металлов на растяжение
- •Заключение
- •3.2. Типы дефектов кристаллического строения и их основные свойства
- •3.3. Структурообразования при пластической деформации металлов
- •3.4. Причины деформационного упрочнения
- •Упрочнение от взаимодействия дислокаций
- •Взаимодействие дислокаций с примесями
- •Упрочняющее действие межзеренных и межфазных границ
- •3.5. Разрушение металлов при пластической деформации
- •3.6. Пластичность металлов. Влияние напряжённого состояния
- •Заключение
- •4.2. Взаимосвязь предела текучести и пластичности металла
- •4.3. Термическое разупрочнение деформированного металла
- •4.4. Движущие силы и кинетика термического разупрочнения
- •4.5. Сопротивление деформации металлов. Релаксация напряжений
- •4.6. Охлаждение деформированного металла. Фазовые превращения
- •Заключение
- •Вопросы для самоконтроля:
- •Лекция 5. Основные виды пластической деформации
- •5.1. Сжатие
- •5.2. Вытяжка
- •5.3. Прошивка
- •5.4. Закручивание
- •5.5. Листовая штамповка
- •5.6. Прокатка
- •5.7. Волочение
- •5.8. Гибка
- •Вопросы для самоконтроля:
- •Лекция 6. Средства нагрева металлов
- •6.1. Источники нагрева
- •6.2. Пламенные нагревательные устройства
- •6.3.Электрические нагревательные устройства
- •Вопросы для самоконтроля:
- •Лекция 7. Технологические процессы художественной деформации, ч. 1
- •7.1. Художественная ковка Основные положения
- •Кузнечные инструменты
- •Основные операции ручной ковки
- •7.2. Выколотка (дефовка)
- •7.3. Чеканка
- •Инструменты и приспособления
- •Технология чеканки
- •Вопросы для самоконтроля:
- •Лекция 8. Технологические процессы художественной деформации, ч. 2
- •8.1. Тиснение (басма)
- •8.2. Металлопластика
- •8.3. Насечка (тауширование)
- •Вопросы для самоконтроля:
- •Лекция 9. Технологические процессы художественной деформации, ч. 3
- •9.1. Филигрань (скань)
- •9.2. Гравирование Общие положения
- •Инструменты и приспособления
- •Плоскостное гравирование
- •Обронное гравирование
- •9.3. Изготовление сусального золота
- •9.4. Листовая штамповка
- •9.5. Ручное резание
- •Вопросы для самоконтроля:
- •Список литературы
- •Специальные технологии художественной обработки материалов. Часть 2 (Технология изготовления художественных изделий обработкой давлением)
Заключение
В этой лекции мы рассмотрели величины, характеризующие напряженное и деформированное состояние металла, получили уравнения, характеризующие взаимосвязь напряжений и деформаций. Познакомились с основными схемами деформации и сформулировали условия пластичности, которые определяют уровень внешних напряжений, выше которого начинается пластическая деформация, позволяющая менять форму и свойства металлов.
Вопросы для самоконтроля:
1. Подавляющее большинство процессов прессования , ковки выколотки горячей и листовой штамповки основаны на операции ?
2. Закон Гук , как связь между деформацией и напряжением
3. Что такое модуль упругости металла (Е ?
4. Каков физический смысл модуля Сдвига (G) ?
5. Какие напряжения называются главными ?
ЛЕКЦИЯ 3. ФИЗИЧЕСКИЕ ПРЕДСТАВЛЕНИЯ
О МЕХАНИЗМАХ ПЛАСТИЧЕСКОЙ ДЕФОРМАЦИИ
И СВОЙСТВАХ МЕТАЛЛОВ
3.1. ТЕОРЕТИЧЕСКАЯ ПРОЧНОСТЬ ИДЕАЛЬНЫХ КРИСТАЛЛОВ
Рис.
3.1. Трехмерная сетка, образованная
системами параллельных линий –
аналог
кристаллической решетки

Будем рассматривать простую кубическую, гранецентрированную кубическую (ГЦК), объемно центрированную кубическую (ОЦК) и гексагональную плотноупакованную (ГПУ) кристаллические решетки (рис. 3.2). Эти типы решеток самые распространенные среди металлов: ГЦК – алюминий, медь, серебро, золото, никель, платина и др.; ОЦК – железо (при температурах ниже 911 °С), хром, вольфрам, молибден и др.; ГПУ – бериллий, титан, кобальт, цирконий, цинк, олово, рений и др. Некоторые металлы при изменении температуры изменяют тип кристаллической решетки; подобное превращение называется полиморфным и имеет определенную температуру Тп.п. Полиморфное превращение сопровождается изменением энергии металла: либо поглощением, либо выделением теплоты в окружающую среду. Примерами подобных металлов являются железо, титан, кобальт и др.
Как известно, металлами называют кристаллические тела, имеющие на каждый атом кристалла один или несколько подвижных (свободных) электронов. Эти электроны объединяются в энергетическую зону (зону проводимости), средняя энергия электронов в которой меньше, чем энергия тех же электронов в изолированных друг от друга атомах. Разность энергий электронов проводимости в атоме и кристалле и является энергией металлической связи в кристаллической решетке.
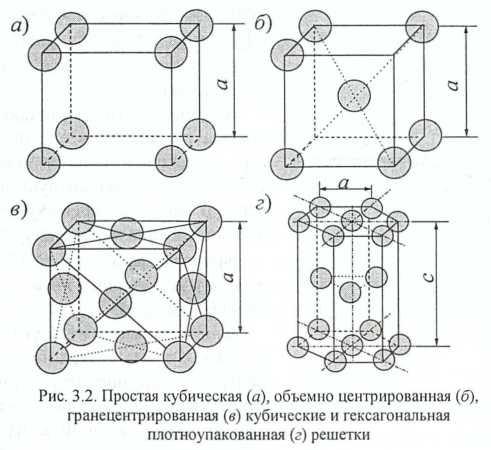
Рис. 3.2. Простая кубическая (а), объемно центрированная (б),
гранецентрированная (в), кубические и гексагональная
плотноупакованная (г) решетки
Считается, что взаимодействие атомов (ионов) в кристаллической решетке парное, т. е. энергия взаимодействия всех атомов в кристалле есть сумма энергий взаимодействия всех пар атомов:
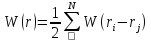 (3.1)
(3.1)
где W(r) – сумма взаимодействия всех пар; ri, и rj – координаты i-го и j-го атомов; W(ri – rj) – энергия их взаимодействия; N – число пар.
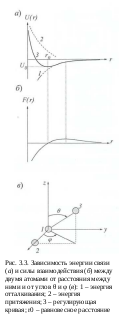
Если два иона в пространстве расположены на расстоянии r, то при их сближении они начинают притягиваться, причем энергия этого взаимодействия достигает минимума при r = r0 (рис. 3.3). Равновесное положение r0, около которого происходят тепловые колебания, находится из условия:
 (3.2)
(3.2)
где F(r) - сила.
Энергия в этом положении W(r0) называется энергией связи. Эта величина характеризует работу А, которую необходимо затратить, чтобы оторвать атомы друг от друга и удалить на такое расстояние, на котором их взаимодействие не ощущается, А+W(r0) = 0. Очевидно, что для стабильности кристалла необходимо условие А > 0, т. е. W(r0) < 0, и кристаллическое состояние атомов энергетически выгодно.
Энергия притяжения, например, в системе ион-электрон, которая является первопричиной металлической связи, ощущается при всех значениях r. Энергия отталкивания (кривая 2 на рис. 3.3) связана обычно с деформацией электронных оболочек ионов и ощущается лишь на малых радиусах взаимодействия r ≤ dат (dат – диаметр атома).
Атомные связи различаются в основном по характеру сил притяжения. Как известно, выделяют ионную, металлическую, ковалентную и молекулярную (ван-дер-ваальсову) связи. Эти взаимодействия характеризуются:
радиусом действия R (R >> r0 – дальнодействуюшие, R ≈ r0 – короткодействующие);
зависимостью от углов: если W = W(r), то взаимодействия называют центральными, поскольку они не зависят от углов, под которыми взаимодействуют ионы; если W=W(r, θ, φ) – нецентральными взаимодействиями, энергия которых зависит от углов θ и φ (см. рис. 3.3,6); энергией связи: W0 > 1 эВ – сильная связь; W0 < 1 эВ – слабая связь; W0 ≈ 1 эВ – связь промежуточной силы.
На сегодняшний день наивысшую прочность имеют очень тонкие нитевидные кристаллы, получаемые конденсацией из пересыщенных растворов, газовой или плазменной фаз, – для их разрушения необходимо приложить напряжения до 10 ГПа, т. е. по прочности они приближаются к теоретической прочности τ°.
Так в чем же причина огромной разницы между прочностями идеального кристалла и реальных металлов? Ответ на этот вопрос дали исследования, которые начали проводить в 30-х гг. XX столетия, когда были высказаны гипотезы о роли дефектов кристаллического строения в формировании прочностных свойств металлов и механизмах пластической деформации. О каких дефектах шла речь?
