
- •Диазосоединения с ковалентной связью
- •Ароматические азосоединения
- •Строение азосоединений
- •1. Реакция диазотирования
- •Механизм реакции диазотирования
- •2) Замещение диазогруппы на иод
- •3) Замещение диазогруппы на другие атомы или группы атомов
- •Механизм реакции
- •4) Получение фторпроизводных ароматических углеводородов
- •5) Получение металлорганических соединений (реакция Несмеянова)
- •6) Реакция Меервейна
- •8) Замещение диазогруппы на водород
- •2. Реакции диазосоединений без выделения азота
- •1) Восстановление солей диазония
- •2. Окисление диазосоединений
- •4. Взаимодействие с аминами
1. Реакция диазотирования
Реакция диазотирования первичных ароматических аминов азотистой кислотой открыта П. Гриссом в 1858 г.
Реакция протекает в присутствии нитрита натрия (или калия) и минеральной кислоты (азотистая кислота неустойчива). Так как реакция диазотирования является экзотермической, а диазосоединения легко разлагаются при нагревании, поэтому реакцию проводят при температуре 0-50С.
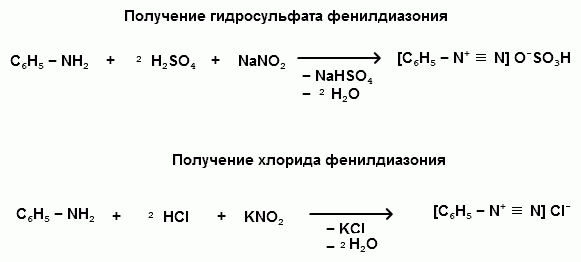
Соли диазония представляют собой твердые вещества. В индивидуальном виде их выделяют крайне редко, поскольку в твердом виде они очень взрывоопасны. Поэтому, после проведения реакции диазотирования полученный раствор соли арилдиазония используют в дальнейших превращениях для получения самых разных ароматических соединений.
Соли арилдиазония при подщелачивании превращаются в арилдиазогидроксиды, а затем в арилдиазотаты натрия. При подкислении протекает обратная реакция:
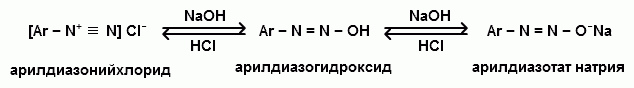
В реакции с алифатическими аминами не удается получить соль диазония, поскольку по мере образования она тут же превращается в спирт.
Механизм реакции диазотирования

Химические свойства
Многочисленные реакции, в которые вступают соли диазония можно разделить на две большие группы:
1) реакции, идущие с выделением азота;
2) реакции. Идущие без выдения азота.
1. Реакции солей диазония с выделением азота
Эти реакции широко используются для получения ароматических соединений различных классов. При этом диазогруппа замещается различными атомами и группами атомов (У):
![]()
В основе этих превращений лежит легкость отщепления диазогруппы и большая стабильность молекулы выделяющегося азота.
В зависимости от
условий реакций и характера реагирующих
веществ замещение может протекать по
гомолитическому или гетеролитическому
механизм
1) Замещение диазогруппы на гидрокси-группу (алкокси-группу)
Образование фенолов
При кипячении кислых растворов солей диазония выделяется азот и образуются фенолы:
Лучше всего применять для этой цели соли серной кислоты, так как с другими кислотами могут происходить побочные явления.
![]()
Замещение диазогруппы протекает по механизму SN1.
На первой стадии происходит гетеролитическое расщепление связи C-N, выделяется азот и образуется арил-катион.
На второй стадии арил-катион взаимодействует с водой с образованием фенола:

Образование эфиров фенолов
Аналогично, по гетеролитическому механизму, в водном растворе спирта диазогруппа замещается на алкокси-группу с образованием простых эфиров:
![]()
2) Замещение диазогруппы на иод
При нагревании солей диазония с иодидом калия диазогруппа замещается иодом:
![]()
Из всех галогенов иод обладает самой низкой реакционной способностью в реакциях электрофильного замещения, поэтому замещение диазогруппы на иод является одним из основных методов получения иодпроизводных ароматического ряда.
Реакция протекает по радикальному механизму, что обусловлено легкой окисляемостью аниона иода:

