
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Карбоновые кислоты
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот
- •Функциональные производные карбоновых кислот

Карбоновые кислоты

Карбоновые кислоты
Карбоновыми кислотами называются соединения, содержащие карбоксильную группу —СООН
O
R C OH
Карбоновые кислоты
Некоторые термины, относящиеся к карбоновым кислотам
O |
|
|
O |
|
|
|
O |
|
O |
||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R - C |
- |
OH |
R - C - O - H |
R - C - O - H |
R - C - O - H |
||||||||||||
|
|
|
|
|
|
|
|
|
|
àöè ëüí û é àòî ì |
àöè ëüí û é àòî ì |
||||||
àöè ëüí àÿ |
àöè ëî ê ñè - |
|
|
||||||||||||||
|
|
ê è ñëî ðî äà |
|||||||||||||||
ãðóï ï à |
|
|
|
ãðóï ï à |
|
|
углеро да |
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
Карбоновые кислоты
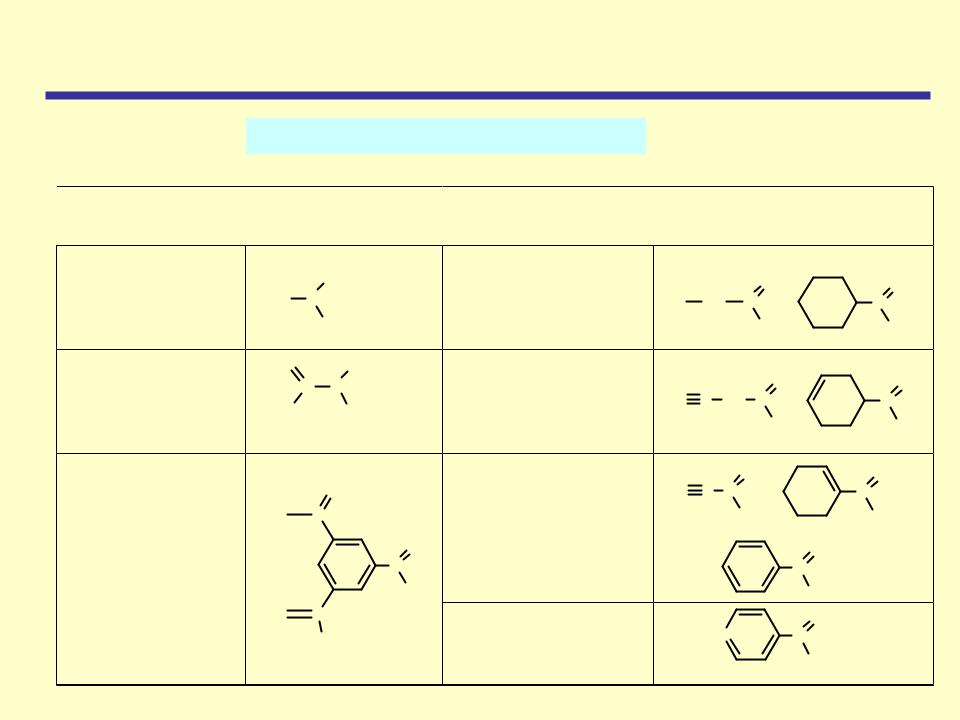
Классификация карбоновых кислот
 По количеству карбоксильных групп:
По количеству карбоксильных групп:
Монокарбоновые
O H C
OH
Дикарбоновые O O C C 
HO OH
O
HO C
 По типу радикала:
По типу радикала:
Насыщенные (нециклические и циклические)
Ненасыщенные (нециклические и циклические)
Сопряженные
ненасыщенные
Поликарбоновые |
O |
Ароматические |
|
C |
|
|
OH |
|
O C |
|
Гетероциклические |
OH |
|
|
|
|
O |
O |
H3C CH2 |
C |
C |
|
|
|
OH |
OH |
HC |
|
O |
O |
C CH2 C |
C |
||
|
|
OH |
OH |
HC |
C C |
O |
O |
|
C |
||
|
|
OH |
OH |
|
|
C |
O |
|
|
|
|
|
|
|
OH |
|
N |
C |
O |
|
|
||
|
|
|
OH |

Карбоновые кислоты

Карбоновые кислоты

Карбоновые кислоты
Строение и физические свойства |
|
||||||
124О |
.O.. |
0,1202 нм |
H '' |
.O.. |
|
||
H |
C 125О |
|
C |
|
C |
sp2 |
|
0,1097 нм |
.. |
111О |
H3C |
|
|
||
|
O |
H |
|
H |
|
.. |
|
0,1343 нм .. |
|
|
|
|
|||
|
|
|
|
.. |
' |
||
|
0,0972 нм |
|
|
'' |
O |
H |
|
|
|
|
|
|
|||
|
|
|
|
|
|
||
Карбоксильная группа представляет собой сочетание карбонильной и гидроксильной групп. Карбоксильный атом углерода находится в sp2-гибридном состоянии и связан с другими атомами -связями. Они лежат в одной плоскости под
углом 120о друг к другу. Остающаяся р-орбиталь атома углерода перекрывается с р-орбиталью атома кислорода, при этом образуется -связь.
Карбоновые кислоты
Строение и физические свойства
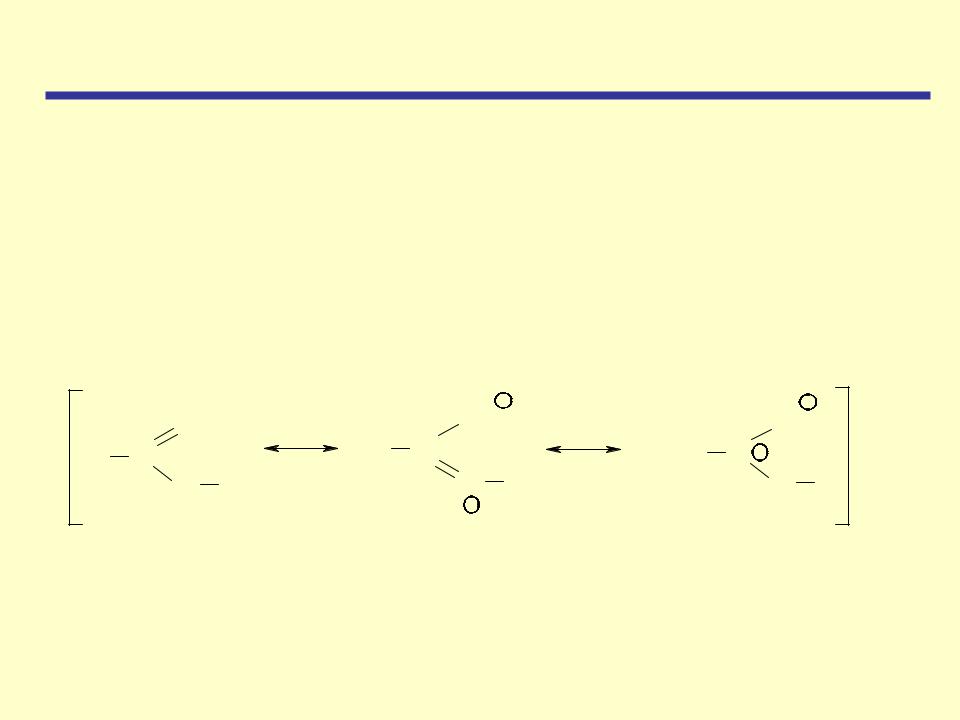
Одна из неподеленных электронных пар атома кислорода гидроксильной группы образует единую -электронную систему с-электронами двойной связи С=О. Делокализация электронной
плотности в карбоксильной группе показана на примере мурвьиной кислоты
.. |
|
.. |
: |
- |
.. - |
O: |
|
Î |
|
Î |
|
Í Ñ .. |
Í Ñ |
.. |
|
|
..: |
O |
|
Í |
Í Ñ + .. |
||
Î Í |
|
|
Î Í |
||
.. |
|
+ |
|
|
.. |

Карбоновые кислоты
Строение и физические свойства
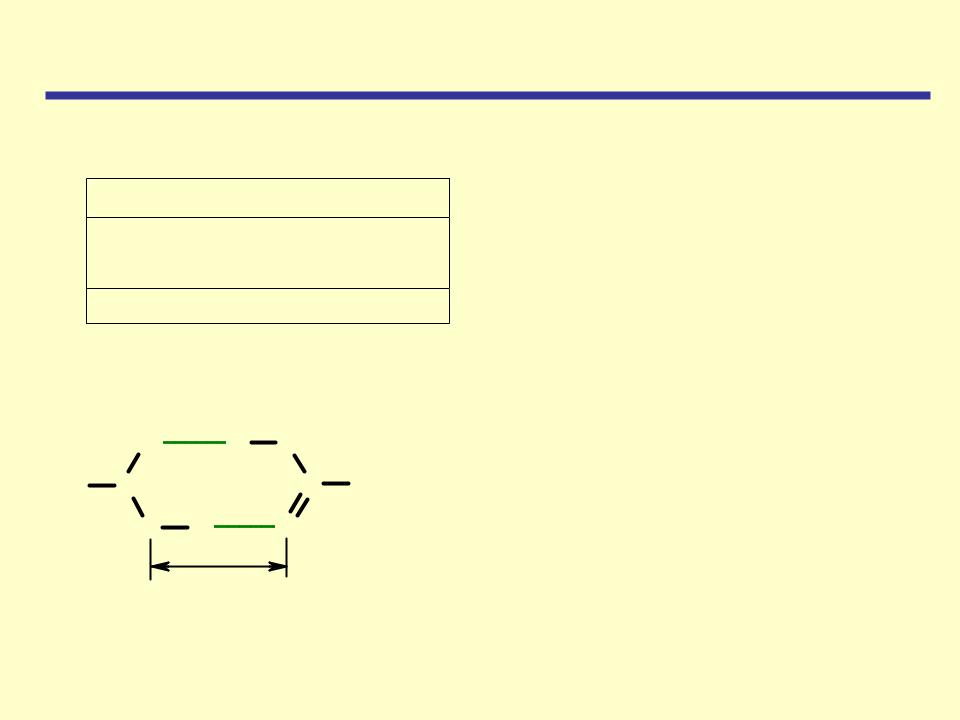
Вещество |
lOH, нм |
lСO, нм |
Кислота |
0,131 |
0,125 |
Спирт |
0,144 |
|
Альдегид |
|
0,122 |
В результате такого распределения электронной плотности атом углерода карбоксильной группы менее склонен к реакциям с нуклеофильными реагентами, чем углерод карбонильной группы альдегидов и кетонов
Карбоновые кислоты
Строение и физические свойства
Вещество |
Ткип, ОС |
Формальдегид |
-21,0 |
Метанол |
64,5 |
Муравьиная кислота |
101,0 |
OH O
R C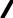 C R
C R
O H O
0,267 нм
Карбоновые кислоты полярны и подобно спиртам могут образовывать водородные связи друг с другом и с другими соединениями. Поэтому алифатические кислоты по растворимости похожи на спирты: кислоты С1-С4
смешиваются с водой, растворимость валериановой кислоты незначительна, а высшие кислоты практически не растворимы в воде. Ароматические карбоновые кислоты – твердые соединения, плохо растворимые в воде
