
- •МЕТОДЫ
- •МЕТОД ЦЕРИМЕТРИИ
- •1. Вариант обратного титрования А) Парацетамол (после кислотного гидролиза) – основан
- •Продолжение
- •МЕТОД БРОМАТОМАТРИИ
- •Б) Ароматические первичные аминопроизводные ЛВ окисляются бромом на первой стадии метода при стоянии
- •2. Вариант обратного титрования (реакции Se) А) ЛВ фенолов (фенол, резорцин, синестрол и
- •МЕТОД ЙОДАТОМЕТРИИ
- •МЕТОД ЙОДОМЕТРИИ
- •2. Вариант обратного титрования А) Альдегидопроизводные ЛВ, окисление в щелочной
- •В) Вариант обратного титрования для органических оснований: первичных –норадреналин, вторичных – эфедрин и
- •Д) Алифатические серосодержащие аминокислоты (цистеин, метионин), окисление по R-SH или R-S-R1
- •3. Вариант косвенного титрования
- •МЕТОД ЙОДХЛОРМЕТРИИ 1. Вариант обратного титрования
- •МЕТОД НИТРИТОМЕТРИИ (окислительно-восстановительного титрования)
- •2. Вариант нитрозирования (пример – один препарат
- •3. Вариант косвенного титрования - амидов после кислотного гидролиза (образуется ароматический первичный амин
- •4. Вариант косвенного титрования ароматических нитропроизводных после восстановления Ar-NO2 до R-NH2
- •МЕТОД КОМПЛЕКСОНОМЕТРИИ 1. Вариант прямого титрования
- •Б) Висмута нитрат основной, после растворения в азотной кислоте (металлиндикатор – пирокатехиновый фиолетовый,
- •2. Вариант обратного титрования солей 3-х валентных металлов (титров. р-ры: эдетат натрия и
- •МЕТОД КЪЕЛЬДАЛЯ
- •1.Вариант метода Къельдаля - основан на щелочном гидролизе амидов с образованием летучих веществ
- •МЕТОД МЕРКУРИМЕТРИИ (осадительного титрования)
- •Б) Орг. ЛВ – соли HГаL кислот и органических
МЕТОДЫ
КОЛИЧЕСТВЕННОГО АНАЛИЗА ЛВ
И ВАРИАНТЫ методов
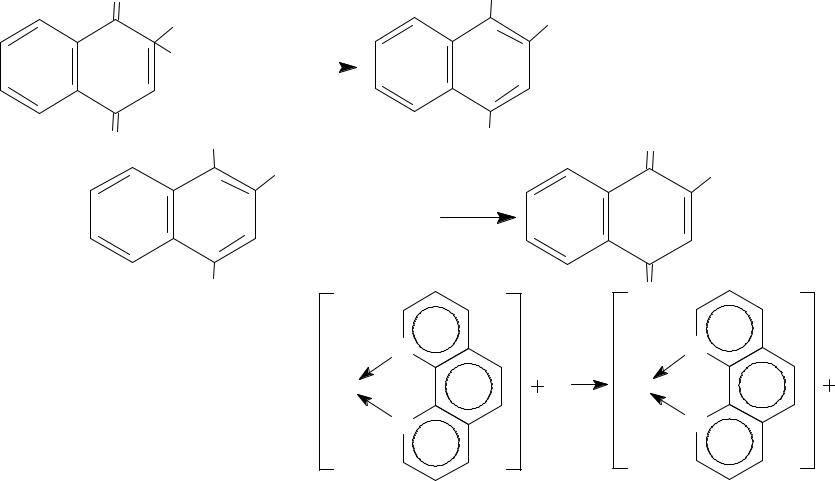
МЕТОД ЦЕРИМЕТРИИ
(метод окислительно-восстановительного титрования)
1. Вариант прямого титрования |
|
|
|
|
||||
А) Викасол (после гидролиза и восстановления) |
|
|
|
|||||
O |
CH3 |
|
OH |
CH3 |
|
|
|
|
|
Zn,HCl |
|
|
|
|
|
||
|
SO3Na |
|
+SO2 +NaCI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
OH |
CH3 |
OH |
O |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
+ 2Ce(SO4)2 |
|
+Ce |
(SO ) +H |
SO |
4 |
|
|
|
|
|
2 |
4 3 |
2 |
|
|
OH
Индикатор
ортофенантролин
Э=1/2Моль
|
|
2+ |
O |
|
3+ |
|
N |
4 + |
|
N |
3+ |
|
|
|
|
||
Fe |
|
Се |
Fe |
|
Cе |
|
N |
|
|
N |
|
красный |
синий |
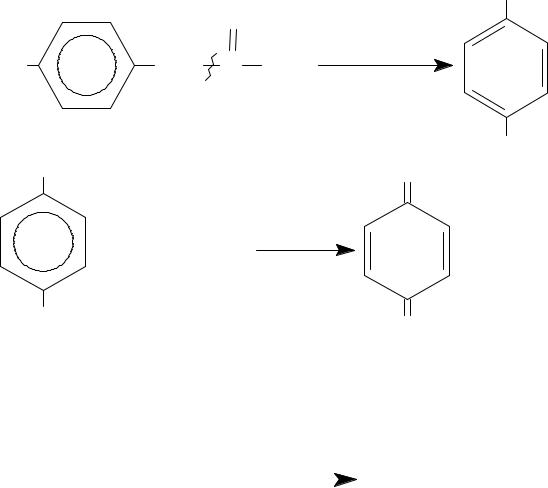
1. Вариант обратного титрования А) Парацетамол (после кислотного гидролиза) – основан
на окислении пара-аминофенола церия (IV) сульфатом до
пара-хинонимина (- 2Н = - 2е) |
NH2 |
|
||||
|
O |
СH3 to,НОН,H+ |
|
|
||
HO |
NH С |
+ CH3 COOH |
||||
|
NH2 |
|
|
NH |
OH |
|
|
|
|
|
|
||
|
+4 |
|
|
|
+3 |
|
|
+ 2Ce(SO4)2 |
|
|
|
+ H SO |
|
|
(-2H |
+ |
) |
+ Ce2(SO4)3 |
||
|
|
|
|
2 4 |
||
|
OH |
(-2e) |
O |
|
|
|
|
|
|
|
|
||
Избыток церия сульфата определяют йодометрически
2Ce(SO4)2 + 2KI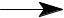 I2 + Ce2(SO4)3 + K2SO4
I2 + Ce2(SO4)3 + K2SO4
I2 + 2Na2S2O3 |
|
2NaI + Na2S4O6 |
Э = ½ Моль |
|

Продолжение |
|
|
|
|
|
|
|
|
|
|||
Б) Раствор формальдегида (вариант обратного |
|
|
|
|||||||||
титрования), основан на окислении формальдегида до |
|
|||||||||||
Муравьиной (метановой) кислоты |
Э = ½ Моль |
|||||||||||
O |
|
+ H2O |
|
|
|
O |
|
|
|
|
||
|
|
|
|
|
|
|
+Ce (SO ) +H |
SO |
4 |
|||
|
|
|
|
|
|
|
||||||
C |
+ 2Ce(SO4)2 |
|
H |
|
C |
2 |
4 3 |
2 |
|
|||
|
|
|
|
|
|
|
||||||
H |
H |
|
|
|
|
OH |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
избыток церия сульфата титруют раствором соли Мора до желтого окрашивания (изб. капля титранта)
2Ce(SO4)2 + 2FeSO4∙(NH4)2SO4∙6H2O→Ce2(SO4)3 + +Fe2(SO4)3+ 2(NH4)2SO4 +6H2O
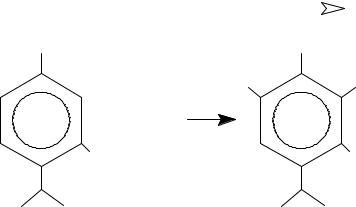
МЕТОД БРОМАТОМАТРИИ
(окислительно-восстановительного титрования)
1. Вариант прямого титрования (реакция Se)
А) Тимол (производное фенолов), индикатор метилоранж (окисляясь бромом в точке экв., обесцвечивается) Э=1/4 Моль
1Моль Br2 = 2 эквивалентам, т.к. Br2 +2e = 2Br¯
KBrO3+5KBr+3H2SO4  3Br2+3K2SO4+3H2O
3Br2+3K2SO4+3H2O
Br |
Br |
+ 2Br2 |
+ 2HBr |
OH |
OH |
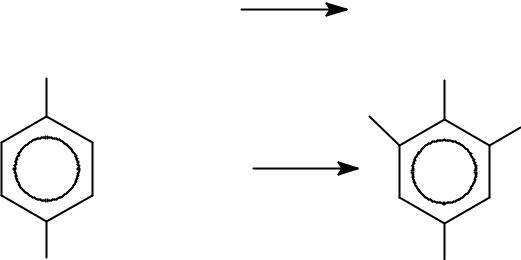
Б) Ароматические первичные аминопроизводные ЛВ окисляются бромом на первой стадии метода при стоянии с бромат-бромидной смесью и получается завышенный результат -новокаин и др. ЛВ ПАБК, Э=1/4 Моль
-сульфаниламиды (норсульфазол, стрептоцид и др.) Э=1/4Моль
KBrO3 + 5KBr + 6 HCl |
|
|
3Br2 + 6 KCl + 3H2O |
NH2 |
|
Br |
NH2 |
|
|
Br |
|
|
M .O |
|
|
+ 2Br2 |
|
+ 2HBr |
|
|
|
R R
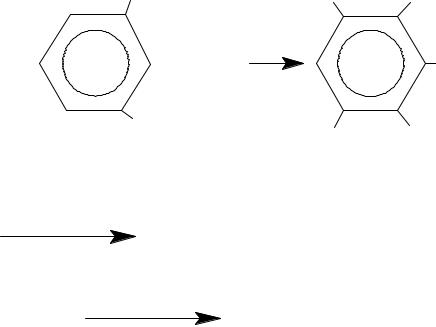
2. Вариант обратного титрования (реакции Se) А) ЛВ фенолов (фенол, резорцин, синестрол и др.)
KBrO3+5KBr+3H2SO4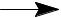 3Br2+3K2SO4+3H2O
3Br2+3K2SO4+3H2O
Резорцин |
OH |
Br |
OH |
|
|
|
|
Э=1/6 Моль |
+ 3Br2 |
Br + 3HBr |
|
|
|||
|
OH |
Br |
OH |
Избыток брома определяется йодометрическим методом |
|||
Br + 2KI |
I2 + 2KBr |
|
|
2 |
|
|
|
I2 + 2Na2S2O3 |
|
2NaI +Na2S4O6 |
|
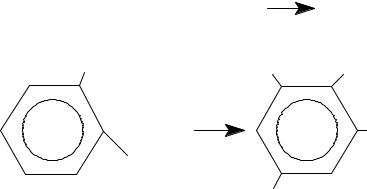
Б) Салициловая кислота и ее Na соль, бромирование идет с декарбоксилированием, Э=1/6 Моль
KBrO3+5KBr+3H2SO4 |
3Br2+3K2SO4+3H2O |
|
Натрия салицилат OH |
Br |
OH |
+ 3Br2 |
|
Br +2HBr + CO2 + NaBr |
COONA |
Br |
|
|
|
|
Br2 + 2KI  I2 + 2KBr
I2 + 2KBr
I2 + 2Na2S2O3  2NaI +Na2S4O6
2NaI +Na2S4O6
В) Амиды и эфиры салиц. к-ты - салициламид и метил- салицилат (Э=1/4 Моль, т.к. образуются дибромпроиз- водные, бромирование идет без декарбоксилирования), или после гидролиза по салициловой кислоте (см. Б)

МЕТОД ЙОДАТОМЕТРИИ
(окислительно-восстановительного титрования)
1.Вариант прямого титрования А) Лактоны полиоксикислот- аскорбиновая кислота
|
|
OH OH |
|
|
O |
|
O |
||||||||||
|
|
|
|
|
3 |
||||||||||||
3 |
|
|
|
+ KIO3 |
|
|
|
|
|
|
|
|
|
|
+KI + 3H2O |
||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
OH |
|
H |
|
|
|
|
||||||||
|
|
|
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|||||||||||||||
CH2OH |
|
|
CH2OH |
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||
В точке эквивалентности (крахмал с I2 дает синее окраш.)
KIO3 +5KI + 6HCI → 3I2 + 6KCI +3H2O Э =1/2 Моль
Примеров варианта обратного титрования на 3курсе -
нет

МЕТОД ЙОДОМЕТРИИ
(окислительно-восстановительного титрования)
1. Вариант прямого титрования А) Тиосульфат натрия (Э =1Моль)
2 экв.
2Na2S2O3 +I2  2NaI + Na2S4O6
2NaI + Na2S4O6
Б) Кислота аскорбиновая, инд. крахмал (Э =1/2 Моль)
|
|
OH OH |
|
|
|
O |
|
O |
|
|
|||||||
|
|
|
I2 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
O |
+2HI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H |
O |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
O |
|||||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
OH |
|
|
H |
|
|
|
|
|
|||||||
|
|
|
|
|
|
OH |
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
||||||||||||||
CH2OH |
|
|
|
CH2OH |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
