
- •Раздел 1. Теоретические основы органической химии. Углеводороды. Методы исследования органических соединений.
- •Раздел 2. Галогенопроизводные, гидроксипроизводные углеводородов. Амины, диазо- и азосоединения. Альдегиды и кетоны.
- •Раздел 3. Карбоновые кислоты. Гетерофункциональные органические соединения. Аминокислоты, пептиды, белки. Углеводы.
- •Раздел 4. Гетероциклические соединения. Липиды.
I. Тесты
Раздел 1. Теоретические основы органической химии. Углеводороды. Методы исследования органических соединений.
КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА, ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1. Предмет органической химии составляет:
А) Изучение состава органических соединений.
В) Изучение физических свойств органических соединений.
С) Изучение состава, свойств, законов, химических превращений, способов получения, применения органических соединений.
D) Изучение способов получения органических соединений.
Е) Изучение химических свойств органических соединений.
2. Группа соединений, которой цепи атомов углерода может быть неразветвленной или разветвленной относятся к:
А) Алифатическому ряду.
В) Карбоциклическому ряду.
С) Гетероциклическому ряду.
D) Стероидному ряду.
Е) Терпеноидному ряду.
3. Функциональная группа альдегидов:
А) – ОН
В) – СО –
С) – СНО
D) – СООН
Е) – СОО –
4. Изомеры – это:
А) Вещества, имеющие одинаковый количественный и качественный состав, но различное строение.
В) Вещества, имеющие одинаковое строение, но различный количественный и качественный состав.
С) Вещества, имеющие сходное строение, образующие гомологический ряд.
D) Вещества, имеющие в составе несколько одинаковых функциональных групп.
Е) Вещества, имеющие в составе различные функциональные группы.
5. Соединение, в котором один из атомов углерода находится в sp – гибридном состоянии является:
А) Бутан.
В) Метилацетилен.
С) Ацетальдегид.
D) Ацетон.
Е) Пропилен.
6. Бензол, нафталин, фенантрен – это:
А) Спирты.
В) Арены.
С) Кетоны.
D) Кислоты.
Е) Тиолы.
7. Пропанол, этанол, бутанол – это:
А) Изомеры.
В) Радикалы.
С) Гомологи.
D) Функциональные группы.
Е) Характеристическая группа.
8. Пентан и неопентан – это:
А) Изомеры.
В) Радикалы.
С) Гомологи.
D) Функциональные группы.
Е) Характеристическая группа.
9. Гетерофункциональное соединение:
А) Этанол.
В) Глицерин.
С) Фенол.
D) Этаноламин.
Е) Этиленгликоль.
10. Радикал СН2 = СН – называется:
А) Аллил.
В) Фенил.
С) Бензил.
D) Метил.
Е) Винил.
11. Функциональная группа соединения:

А) Метокси.
В) Гидроксил.
С) Карбонил.
D) Карбоксил.
Е) Амино.
12. Автором теории химического строения органических соединений является:
А) Лебедев.
В) Кекуле.
С) Марковников.
D) Бутлеров.
Е) Зинин.
13. Хлорангидрид карбоновой кислоты:
А) СІСН2СООН.
В) СІ3ССООН.
С) С4Н9СООН.
D) С4Н9СONH2.
Е) С4Н9СOСІ.
14. Гетерофункциональными называются:
А) Соединения, содержащие в молекулах 2 одинаковые функциональные группы.
В) Соединения, содержащие в молекулах 3 одинаковые функциональные группы.
С) Соединения, содержащие в молекулах 4 одинаковые функциональные группы.
D) Соединения, содержащие в молекулах различные функциональные группы.
Е) Соединения, содержащие в молекулах 1 функциональную группу.
15. Коламин СН2NН2 – СН2ОН по номенклатуре ИЮПАК называется:
А) 2-аминоэтаналь.
В) 2-аминоэтанол.
С) 2-метилпропаналь.
D) 2-аминопропаналь.
Е) 2-аминопропановая кислота.
16. Радикал С6Н5 – СН2 – называется:
А) Аллил.
В) Фенил.
С) Бензил.
D) Метил.
Е) Винил.
17. Называется по международной номенклатуре:
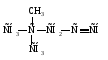
А) 4,4 - диметилпентин-2.
В) 2,2 - диметилпентин-4.
С) изобутилацетилен.
D) 4,4-диметилпентин-1.
Е) Трет.бутилацетилен.
18. Акролеин СН2=СН–СНО по заместительной номенклатуре ИЮПАК называется:
А) Пропаналь.
В) Пропиналь.
С) Пропеналь.
D) Пропионовый альдегид.
Е) Пропанон.
19. Определите класс соединения:
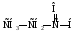
А) Сложный эфир.
В) Кислота.
С) Кетон.
D) Альдегид.
Е) Простой эфир.
20. Называется по рациональной номенклатуре:

А) Изопропилпентан.
В) 3 – этилпентан.
С) Триэтилметан.
D) Метилэтилпропан.
Е) Метилэтилпропилметан.
21. Радикал С6Н5 – называется:
А) Аллил.
В) Фенил.
С) Бензил.
D) Метил.
Е) Винил.
22. Альдегиды и кетоны содержат в своем составе функциональную:
А) Аминогруппу.
В) Нитрогруппу.
С) Карбоксильную группу.
D) Карбонильную группу.
Е) Гидроксильную группу.
23. Функциональная группа карбоновых кислот:
А) – ОН
В) – СО –
С) – СНО
D) – СООН
Е) – СОО –
24. Радикал:
А) Дивинил.
В) Нафталин.
С) Этан.
D) Бензил.
Е) Фенол.
25. Гомологи:
А) Этан, этен, этин.
В) Пропанол-1, пропанол-2.
С) Метанол, этанол, пропанол.
D) Хлор, бром, йод, фтор.
Е) Пропаналь, пропанон-2.
26. Количество первичных атомов углерода в н. пентане:
А) 1
В) 2
С) 3
D) 4
Е) 5
27. Дивинил СН2 = СН – СН = СН2 по номенклатуре ИЮПАК называется:
А) Бутен-2
В) Бутадиен-2,3
С) Бутен-1
D) Бутадиен-1,3
Е) Бутадиен-1,4
28. Углеводородный радикал:

А) Этил.
В) Фенил.
С) Аллил.
D) Винил.
Е) Этинил.
29. Определите класс соединения:
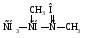
А) Альдегид.
В) Кислота.
С) Сложный эфир.
D) Кетон.
Е) Простой эфир.
30. Этиленоксид, пирролидин, тиофен относятся к углеводородам:
А) Ациклическим.
В) Карбоциклическим.
С) Алифатическим.
D) Алициклическим.
Е) Гетероциклическим.
31. Радикал СН2 = СН – СН2 – называется:
А) Аллил.
В) Фенил.
С) Бензил.
D) Метил.
Е) Винил.
32. Частицы метил, этил, винил – это:
А) Изомеры.
В) Радикалы.
С) Гомологи.
D) Функциональные группы.
Е) Характеристическая группа.
33. Полифункциональное соединение:
А) Этанол.
В) Коламин.
С) Глицерин.
D) Анилин.
Е) Фенол.
34. Функциональная группа – карбоксил:
А) – С ≡ N
В) – СООН
С) – ОН
D) – СНО
Е) – NН2
35. Глицин (аминоуксусная кислота) имеет формулу:
А) СН3 – СН(NН2) – СООН
В) NН2 – СН2 – СН2 – ОН
С) NН2 – СН2 – СН2 – СООН
D) СН3 – СНОН – СН2 – NН2
Е) NН2 – СН2 – СООН
36. Углеводородный радикал:

А) Пропил.
В) Изобутил.
С) Изопропил.
D) Аллил.
Е) Винил.
37. Называется по международной номенклатуре:
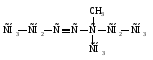
А) 5,5 - диметилгептин –3
В) 3,3 - диметилгептин– 4
С) 5,5 - диметилгептен– 3
D) Этилизобутилацетилен
Е) 3,3 - диметилгексин– 4.
38. Определите класс соединения:
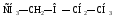
А) Сложный эфир.
В) Простой эфир.
С) Кетон.
D) Альдегид.
Е) Спирт.
39. Называется по рациональной номенклатуре:
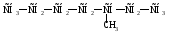
А) Метилэтилбутилметан.
В) Этилизобутилметан.
С) Пропилизобутилметан.
D) Изопропилбутилметан.
Е) Метилэтилпропилметан.
40. Структурными изомерами являются:
А) Пропанол и пропаналь.
В) Пропен и пропан.
С) Пропен и пропин.
D) Пропанол и метоксиэтан.
E) Пропан и 2-метилпропан.
41. Наиболее старшая группа:
А) – С ≡ N
В) – СООН
С) – ОН
D) – СНО
Е) – NН2
42. Изопрен СН2 = С(СН3) – СН = СН2 по номенклатуре ИЮПАК называется:
А) 2-метилбутадиен-1,3.
В) 2-аминоэтанол.
С) 2-метилпропаналь.
D) 3-метилбутадиен-1,3.
Е) 2-гидроксипропановая кислота.
43. Ковалентная рх - рх связь осуществляется между атомами:
А) Н – Н
В) Н – С ≡
С) = С – С =
D) ≡ С – Nа
Е) Н – Сl
44. Водородные связи не образует:
A) Метанол.
B) Метиламин.
C) Фенол.
D) Метантиол.
E) Уксусная кислота.
45. Типы гибридизации валентных АО углерода:
А) s2р3 , sр2, sр3
В) sр, s2р, sр2
С) sр3, sр2, sр
D) s2р, s2р4, sр4
Е) s2р6, sр, sр3
46. Свободные атомы или частицы с неспаренным электроном:
А) Электрофилы.
В) Реагенты.
С) Субстраты.
D) Нуклеофилы.
Е) Радикалы.
47. Называется по международной номенклатуре:

А) 2,5-диметилгексан.
В) 3-метил -5- этилпентан.
С) 3,5 – диметилгексан.
D) Диизобутилметан.
Е) 2,4 – диметилгексан.
48. Углеводородный радикал:
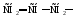
А) Аллил.
В) Винил.
С) Фенил.
D) Пропил.
Е) Изопропил.
49. Одноатомный вторичный спирт:
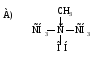


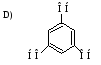
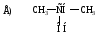
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ
1. Передача электронного влияния заместителя по системе π – связей называется :
А) Индуктивным эффектом.
В) Мезомерным эффектом.
С) Поляризуемостью.
D) Ароматичностью.
Е) Кислотностью.
2. Электронные эффекты метильной группы в толуоле:
А) + M, – I
B) – M, + I
C) – M, – I
D) + M, + I
E) + I
3. Мерой прочности химической связи является:
А) Полярность молекулы.
В) Энергия связи.
С) Ковалентность связи.
D) Электроотрицательность элементов.
Е) Длина связи.
4. Соединение, в котором имеется π,π – сопряженная система:
А) Уксусная кислота.
В) Этанол.
С) н-бутан.
D) Бензол.
Е) Циклопропан.
5. Индуктивный эффект всегда направлен в сторону:
А) Заместителей.
В) Углеродной цепи.
С) Более электроотрицательного атома.
D) Наиболее длинной углеродной цепи.
Е) -связи.
6. Электронные эффекты нитро группы в нитробензоле:
А) + I, – М
В) – I, – М
С) – I
D) – I, + М
Е) + I, + М.
7. Электронные эффекты альдегидной группы в бензальдегиде:
А) + M, – I
B) – M, + I
C) – M, – I
D) + M, + I
E) + I
8. Передача электронного влияния заместителей по системе σ – связей называется:
А) Индуктивным эффектом.
В) Мезомерным эффектом.
С) Поляризуемостью.
D) Ароматичностью.
Е) Основность.
9. Электронные эффекты карбоксильной группы в уксусной кислоте:
А) + M, – I
B) – M, + I
C) – M, – I
D) + M, + I
E) – I
10. Соединение, в котором имеется р,π – сопряженная система:
А) Бутадиен-1,3.
В) Изопрен.
С) Толуол.
D) Бензол.
Е) Винилхлорид.
11. Соединение, в котором имеется сопряженная двойная связь:
А) СН2 = СН – СН = СН2
В) СН2 = С = СН – СН = СН2
С) СН2 = СН – СН2 – СН = СН2
D) СН2 = С = СН2
Е) СН2 = СН – СН2 – СН2 – СН = СН2
12. Только положительный индуктивный эффект (+J) проявляет заместитель:
А) – ОН
В) – СН3
С) – COOH
D) – NH2
Е) – Вr
13. Мезомерный эффект возникает при передаче влияния заместителей:
А) По -связям углеродной цепи.
В) По - и -связям углеродной цепи.
С) По системе -связи.
D) По -связям сопряженной системы.
Е) По -связям замкнутого цикла.
14. Электронные эффекты брома в бромбензоле:
А) + M, – I
B) – M, + I
C) – M, – I
D) + M, + I
E) + I
15. Электроноакцепторные заместители:
А) – СООН
В) – CI
С) – C2H5
D) – CHO
Е) – СН3
16. В молекуле СH2 = СНNО2 нитрогруппа оказывает влиние:
А) +М
В) –М
С) +J, +М
D) +J, +М
Е) –І, –М
17. Заместитель проявляет электроноакцепторные свойства:
A) В феноле.
B) В йодбензоле.
C) В анилине.
D) В этилбензоле.
E) В метилфениловом эфире.
18. Электронные эффекты гидроксильной группы в феноле:
А) + M, – I
B) – M, + I
C) – M, – I
D) + M, + I
E) + I
ПРОСТРАНСТВЕННАЯ ИЗОМЕРИЯ
1. Конфигурация стереомера по конфигурационному стандарту:
А) Относительная конфигурация.
В) Абсолютная конфигурация.
С) Конформация.
D) Хиральность.
Е) Таутомерия.
2. В молекуле (СН3)2СНСН2СН(NH2)СООН встречается изомерия:
А) Таутомерия.
В) Цис-транс изомерия.
С) Диастереомерия.
D) Энантиомерия.
Е) Е, -изомерия.
3. Энантиомеры отличаются друг от друга:
А) Химическими свойствами.
В) Температурой плавления.
С) Температурой кипения.
D) Плотностью.
Е) Знаком оптической активности.
4. Е, -изомерия существует для:
А) 1-бром-1,2-дихлорпентена-1
В) 1,1- дихлорпентена-1
С) 1,1-дибромпентена-1
D) 1,1-дийиодпентена-1
Е) Пентена-1
5. Для изображения конформационных изомеров за минимальный отсчет поворота принимают угловой градус:
А) 180о
В) 360о
С) 90о
D) 60о
Е) 30о
6. Для хлоряблочной (2-гидрокси-3-хлорбутандионовой) кислоты существует:
А) 2 стереоизомера.
В) 3 стереоизомера.
С) 4 стереоизомера.
D) 6 стереоизомеров.
Е) 8 стереоизомеров.
7. Оптически активное соединение:
А) 2-аминопропановая кислота.
В) Пропановая кислота.
С) Пропантриол-1,2,3.
D) 2-аминоэтановая кислота.
Е) Этаналь.
8. Укажите соединение, существующее в виде антиподов:
А) Гидрохинон.
В) α-аминомасляная кислота.
С) Уксусная кислота.
D) Этандиол-1,2
Е) 2-метилпропаналь.
9. π – Диастереомерия характерна для:
А) Алканов.
В) Алкенов.
С) Спиртов.
D) Аренов.
Е) Циклоалканов.
10. Число ассиметрических атомов углерода в фруктозе:
А) 1
В) 2
С) 3
D) 4
Е) 5
11. В молекуле СН3СН(NH2)СООН встречается изомерия:
А) Таутомерия.
В) Энантиомерия.
С) Диастереомерия.
D) Цис-транс изомерия.
Е) Е, -изомерия.
12. -Диастереомеры образует:
А) 2,3-дигидроксипропановая кислота.
В) 2-гидроксибутановая кислота.
С) 2,3-дигидроксибутандиовая кислота.
D) Молочная кислота.
Е) 2-гидроксибутандиовая кислота.
13. Вид изомерии между малеиновой и фумаровой кислотами:
А) Цис-транс изомерия.
В) Энантиомерия.
С) Диастереомерия.
D) Таутомерия.
Е) Структурная изомерия.
14. В виде Е, Z-стереоизомеров существует:
А) 1,2,2-трихлорэтен.
В) 1,1-дихлор-2,2-дифторэтан.
С) 1,2-дифтор-1,2-дихлорэтан.
D) 1,1-дихлорэтен.
Е) 1-бром-2-иод-1,2-дифторэтен.
15. Оптически активное соединение:
А) 2-метилпропаналь.
В) Пропаналь.
С) 2-гидроксипропаналь.
D) Пропанол-2
Е) Пропантриол-1,2,3
16. Стереоизомер с одним хиральным центром:
А) 3-гидроксипропановая кислота.
В) 2-аминоэтанол.
С) Аминоуксусная кислота.
D) 2-гидроксипропановая кислота.
Е) Пропантриол-1,2,3.
17. Цис-транс изомерия не существует для:
А) Бутена-2
В) Гексена-2
С) Гексена-3
D) Пропана.
Е) 1-хлорбутена-2
18. n в формуле N = 2n является:
А) Числом центров хиральности.
В) Числом общего числа атомов С.
С) Числом стереоизомеров.
D) Числом общего числа атомов Н.
Е) Числом функциональных групп.
19. Оптические изомеры:
А) -диастереоизомеры.
В) Энантиомеры.
С) -диастереомеры.
D) Эпимеры.
Е) Рацематы.
20. Порядок расположения атомов в пространстве без учета различий, возникающих вследствие вращения вокруг одинарных связей, называется:
А) Конфигурацией.
В) Конформацией.
С) Таутомерией.
D) Изомерией.
Е) Структурной изомерией.
21. Молекулы, которые относятся к конфигурационным изомерам:
А) Отличаются по положению двойной связи.
В) Отличаются по расположению атомов в пространстве.
С) Не отличаются по расположению атомов в пространстве.
D) Имеют одинаковые пространственное строение.
Е) Отличаются по распределению электронной плотности π-связи.
22. Абсолютной конфигурации стереоизомеров соответствует:
А) Пространственное строение глицеринового альдегида.
В) Е - , Z – система.
С) Цис-транс система.
D) R- , S – система.
Е) D- , L – система.
23. Цис-транс-изомерия относится к изомерии:
А) Конформационной.
В) Структурной.
С) Конфигурационной.
D) Положения.
Е) Функциональных групп.
24. Стереоизомеры – это:
А) Вещества, имеющие одинаковый количественный и качественный состав, но различное строение.
В) Вещества, имеющие одинаковое строение, т.е. с одним и тем же порядком соединения атомов, отличающиеся расположением тех же атомов в пространстве.
С) Вещества, имеющие сходное строение, образующие гомологический ряд.
D) Вещества, имеющие в составе несколько одинаковых функциональных групп.
Е) Вещества, имеющие одинаковое строение, но различный качественный и количественный состав.
25. Соединения, имеющие асимметрический атом углерода:
A) CH3–CH(NH2) –COOH
B) CH3–CH2–CHBr–CH3
C) (CH3)2CH – CH2 – CH(OH) –CH3
D) HOOC–CH2 – CH(OH) – CH2–COOH
E) HOOC–CH2 – CH(OH) – COOH
26. Энантиомеры – это:
А) Стереоизомеры, молекулы которых относятся друг к другу как предмет и совместимое с ним зеркальное изображение.
В) Стереоизомеры, молекулы которых не относятся друг к другу как предмет и несовместимое с ним зеркальное изображение.
С) Изомеры строения.
D) Изомеры функциональных групп.
Е) Изомеры положения.
27. Различные стереоизомеры молекулы, возникающие в результате вращения вокруг одинарных связей, называют:
А) Конфигурацией.
В) Конформациями.
С) Таутомерами.
D) Энантиомерами.
Е) Диастереомерами.
28. Для изображения конформации используют проекционные формулы:
А) Хеуорса.
В) Фишера.
С) Ньюмена.
D) Байера.
Е) Колли-Толленса.
29. Оптически не активная смесь равных количеств энантиомеров называется:
А) Рацематом.
В) Эпимером.
С) Антиподом.
D) Мезоформой.
Е) Диастереоизомером.
30. Энантиомерами являются:
А) D – глюкоза и D – фруктоза.
В) L – фруктоза и L – глюкоза.
С) D – глюкоза и L – фруктоза.
D) D – глюкоза и L – глюкоза.
Е) D – фруктоза и L – манноза.
31. Для изображения конформаций на плоскости используют проекционные формулы:
А) Фишера.
В) Байера.
С) Хеуорса.
D) Вант-Гоффа.
Е) Ньюмена.
32. Рацематом является:
А) Д – винная кислота.
В) L – винная кислота.
С) (Д, L) – винная кислота.
D) Мезовинная кислота.
Е) Д – молочная кислота.
33. Оптически активное соединение:
А) 2-метилпропаналь.
В) Пропаналь.
С) 2-гидроксипропаналь.
D) Пропанол-2.
Е) Пропантриол-1,2,3.
34. В конформациях циклогексана валентные углы приближаются к углу:
А) 120о
В) 180о
С) 109о
D) 90о
Е) 60о
35. Молочная (2-гидроксипропановая) кислота имеет число стереоизомеров:
А) 2
В) 3
С) 4
D) 1
Е) 6
36. Не имеет асимметрического атома углерода:
A) CH3 – CH(OH) –COOH
B) (CH3)2CBr – CH2 – COOH
C) C6H5 – CH(NH2) – COOH
D) CH3 – CH(NH2) –CH2–COOH
E) CH3 – CHCl – COOH
КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1. По теории Бренстеда-Лоури кислотами являются:
А) Акцепторы протона.
В) Доноры электронной пары.
С) Доноры протона.
D) Акцепторы электронной пары.
Е) Доноры катионов.
2. Этиловый спирт относится к:
А) Карбоновым кислотам.
В) SH-кислотам.
С) NH-кислотам.
D) СH-кислотам.
Е) ОH-кислотам.
3. Не является основанием Льюиса:
А) Фуран.
В) Пиридин.
С) Тиофен.
D) Метилциклогексан.
Е) Нафталин.
4. Обладает наибольшей кислотностью:
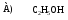



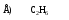
5. Электронодонорные заместители:
А) Стабилизируют анион и увеличивают кислотность соединения.
В) Дестабилизируют анион и уменьшают кислотность соединения.
С) Не влияет на кислотность соединения.
D) Стабилизируют анион и уменьшают кислотность соединения.
Е) Дестабилизируют анион и увеличивают кислотность соединения.
6. Нейтральные молекулы или ионы, способные присоединять протон:
А) Кислоты Бренстеда.
В) Основания Бренстеда.
С) Кислоты Льюиса.
D) Основания Льюиса.
Е) ОН-кислоты.
7. Самое сильное основание в ряду:
А) п-толуидин.
В) Анилин.
С) п-нитроанилин.
D) 2,4,6-тринитроанилин.
Е) 2,4-динитроанилин.
8. Присоединение галогеноводорода к этилену относится к кислотно-основному взаимодействию, где этилен:
А) р-основание.
В) -основание.
С) Кислота Бренстеда.
D) Кислота Льюиса.
Е) СН-кислота.
9. Наибольшими кислотными свойствами обладает:
А) НСООН
В) СН3СООН
С) СН2FСООН
D) СНF2СООН
Е) СF3СООН
10. По теории Бренстеда-Лоури основаниями являются
А) Доноры протона.
В) Доноры электронной пары.
С) Акцепторы электронной пары.
D) Акцепторы катионов.
Е) Акцепторы протона.
11. Наибольшими кислотными свойствами обладает:
А) СН3SН
В) СН3ОН
С) С2Н5NН2
D) СН3 – СН2 – СН3
Е) СН3 – СН = СН – СН3
12. Электроноакцепторные заместители:
А) Повышают основность соединения.
В) Понижают основность соединения.
С) Не влияют на основность соединения.
D) Повышают, затем уменьшают основность соединения.
Е) Уменьшают, затем увеличивают основность соединения.
13. Фенол относится к:
А) Карбоновым кислотам.
В) SH-кислотам.
С) NH-кислотам.
D) СH-кислотам.
Е) ОH-кислотам.
14. Ацетилен относится к:
А) Оксониевым основаниям.
В) SH-кислотам.
С) NH-кислотам.
D) СH-кислотам.
Е) ОH-кислотам.
15. Наибольшую кислотность имеет:
А) Муравьиная кислота.
В) Уксусная кислота.
С) Пропионовая кислота.
D) Бутановая кислота.
Е) Пентановая кислота.
16. Основания Бренстеда:
А) Способны присоединять протон.
В) Имеют гидроксильную группу.
С) Способны отдавать протон.
D) Имеют вакантную орбиталь.
Е) Имеют отрицательный заряд.
17. Наибольшей кислотностью обладает:
А) о-Нитрофенол.
В) Фенол.
С) Пикриновая кислота (2,4,6-тринитрофенол).
D) п-крезол (п -метилфенол).
Е) о-крезол (о-метилфенол).
18. Сильное основание:
А) RСООН
В) RNH2
С) ROR
D) ROH
Е) RSH
19. Наибольшую кислотность имеет:
А) n-Нитроанилин.
В) Анилин.
С) о-Крезол.
D) n-Нитрофенол.
Е) Фенол.
20. По теории Бренстеда-Лоури соединения имеющие протон связанный с кислородом:
А) SH – кислоты.
В) OH – кислоты.
С) NH – кислоты.
D) СН – кислоты.
Е) ОН – основания.
21. Наибольшими основными свойствами обладает:
А) NН3
В) Н2О
С) СН3NН2
D) СН3ОН
Е) СН3SН
22. По теории Бренстеда-Лоури соединения присоединяющие протон за счет электронной пары атома азота:
А) -основания.
В) Сульфониевые основания.
С) Оксониевые основания.
D) Аммониевые основания.
Е) NH-кислоты.
23. По теории Льюиса кислотами являются :
А) Доноры электронной пары.
В) Акцепторы электронной пары.
С) Акцепторы протона.
D) Доноры протона.
Е) Акцепторы катионов.
24. Наибольшую кислотность имеет:
А) СН3 – СООН
В) СН3 – СН2 – СООН
С) СН2СI – СООН
D) СН2СI – СН2 – СООН
Е) СН3 – СН2 – СООН
25. Наибольшую кислотность имеет:
А) Пропионовая кислота.
В) Уксусная кислота.
С) Трихлоруксусная кислота.
D) Монохлоруксусная кислота.
Е) Дихлоруксусная кислота.
26. Кислоты Бренстеда:
А) Способны присоединять протон.
В) Способны присоединять положительные частицы.
С) Способны отдавать протон.
D) Имеют вакантную орбиталь.
Е) Имеют отрицательный заряд.
27. Наиболее сильная кислота:
А) рК = 10,5
В) рК = 7,6
С) рК = 3,8
D) рК = 5,8
Е) рК = 4,9
28. Обладает наибольшей основностью:
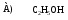


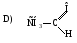

29. Наиболее сильная кислота:
A) Метиламин.
B) Диметиламин.
C) Анилин.
D) Метантиол.
E) Метанол.
30. Наиболее слабое основание:
А) (СН3)3N.
В) NН3.
С) (СН3)2NН.
D) (С6Н5)3N.
Е) СН3NН2.
АЛКАНЫ. ЦИКЛОАЛКАНЫ.
1. Общая формула алканов:
А) СnН2n
В) СnН2n-2
С) СnН2n-6
D) СnН2n+2
Е) СnН2n+1
2. (СН3)2СН – СН(СН3) – СН2 – СН3 называется по международной номенклатуре:
А) 2,3-диметилпентан.
В) 2,2-диметилпентан.
С) 2,2,3-триметилбутан.
D) 2,3-диметилбутан.
Е) 3,3-диметилпентан.
3. При крекинге парафинов образуются:
А) Алканы.
В) Алканы и алкены.
С) Алкены и алкины.
D) Алкины.
Е) Арены.
4. Для алканов характерны реакции :
А) SN
В) S E
С) SR
D) АR
Е) А E
5. Взаимодействие алканов с молекулярным кислородом относится к реакциям:
А) Нуклеофильного замещения.
В) Электрофильного замещения.
С) Радикального присоединения.
D) Электрофильного присоединения.
Е) Радикального замещения.
6. СН4 + Сl2 → СН3Сl + НСl взаимодействие относится к реакциям:
А) АR
В) SN
С) SE
D) SR
Е) АE
7. При бромировании 2-метилпропана в первую очередь образуется:
А) 1,2-дибром-2-метилпропан.
В) 1-бром-2-метилпропан.
С) 2-бром-2-метилпропан.
D) 1,1-дибром-2-метилпропан.
Е) 1,1,1-трибром-2-метилпропан.
8. Изомерия в ряду алканов начинается с:
А) Метана.
В) Бутана.
С) Этана.
D) Пентана.
Е) Гексана.
9. Реакция галогенирования метана идет по механизму:
А) Нуклеофильного присоединения.
В) Радикального замещения.
С) Электрофильного замещения.
D) Элиминирования.
Е) Электрофильного присоединения.
10. Для атома С в состоянии sp – гибридизации характерен валентный угол:
А) 109о
В) 120о
С) 180о
D) 108о
Е) 45о
11. Молекула метана СН4 имеет геометрическую форму:
А) Треугольную.
В) Линейную.
С) Кубическую.
D) Прямоугольную.
Е) Тетраэдрическую.
12. При осущеcтвлении реакции Вюрца происходит:
А) Галогенирование.
В) Гидрирование.
С) Окисление.
D) Удвоение числа атомов углерода.
Е) Нитрование.
13. При нитровании пропана по Коновалову преимущественно образуется:
А) 1-Нитропропан.
В) 2- нитропропан.
С) Нитроэтан.
D) Нитрометан.
Е) Смесь нитросоединений.
14. Циклопропан можно получить из:
А) 1,1-дихлорпропана.
В) 1,4- дихлорбутана.
С) 1,3-дихлорпропана.
D) 2,2-дихлорпропана.
Е) 1,4-дихлорбутана.
15. При взаимодействии циклопропана с бромом образуется:
А) 1,2-дибромпропан.
В) 1,1-дибромпропан.
С) 2,2-дибромпропан.
D) 1,3-дибромпропан.
Е) 1-бромпропан.
16. Соединение СН3 – СН(СН3) – СН2 – СН (СН3) – СН2 – СН3 по номенклатуре ИЮПАК называется:
А) 3 – метил – 5 – этилгексан.
В) 2,5 – метилгептан.
С) 2,4 – диметилпентан.
D) 2,4 – диметилгексан.
Е) 3,5 – диметилгексан.
17. Соединение СН3 – С(СН3)2 – СН2 – СН3 по номенклатуре ИЮПАК называется:
А) 2,3 – диметилбутан.
В) 2,2 – диметилбутан.
С) 2 – метилбутан.
D) 2 – метилпентан.
Е) 2,2,3 – триметилбутан.
18. Соединение СН3 – СН (СН3) – СН2 – СН3 по рациональной номенклатуре называется:
А) Диметилэтилметан.
В) Этилизопропилметан.
С) Метилизопропилметан.
D) Пропилэтилметан.
Е) Метилдиэтилметан.
19. Автор реакции:
СН3
– СН2
– Вr
+ 2Nа
+ Вr
– СН2
– СН3
СН3 –
СН2 –
СН2
– СН3
+ 2NаВr

А) Коновалов.
В) Вюрц.
С) Гофман.
D) Зинин.
Е) Кучеров.
20. В результате гидрирования бутена – 2 образуется:
А) Бутан.
В) Пропан.
С) Бутен – 1.
D) Бутин – 2.
Е) Бутин – 1.
21. Реакция хлорирования метана при УФ – облучении идет по механизму:
А) Нуклеофильного замещения.
В) Радикального замещения.
С) Электрофильного замещения.
D) Нуклеофильного присоединения.
Е) Электрофильного присоединения.
22. Наиболее легко радикальной атаке подвергается:
А) Метил.
В) Первичный углеродный атом.
С) Вторичный углеродный атом.
D) Третичный углеродный атом.
Е) Пропил.
23. Для насыщенных углеводородов характерны реакции:
А) Радикального замещения (SR).
В) Электрофильного присоединения (АЕ).
С) Электрофильного замещания(SE).
D) Нуклеофильного присоединения(AN).
Е) Нуклеофильного замещания(SN).
24. При бромировании изобутана в первую очередь образуется:
А) 1,2-дибром-2-метилпропан.
В) 1-бром-2-метилпропан.
С) 2-бром-2-метилпропан.
D) 1,1-дибром-2-метилпропан.
Е) 1,1,1-трибром-2-метилпропан.
25. Бензилхлорид образуется при реакции:
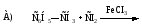
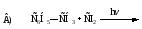

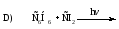
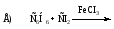
26. В изобутане преимущественно радикальной атаке подвергается атом углерода:
А) Первичный и вторичный.
В) Вторичный и третичный.
С) Третичный и первичный.
D) Первичный.
Е) Третичный.
27. Число структурных изомеров у алкильной группы, имеющей состав С4Н9:
А) 6
В) 2
С) 3
D) 5
Е) 4
28. Реагенты, взаимодействующие с алканами:
1. Cl2(h)
2. HNO3+H2O
3. NaOH
4. Br2 +HOH
5. HOH
А) 1,2
В) 4,5
С) 3,4
D) 3,5
Е) 1,4
29. По реакции Вюрца получают бутан из:
А) Бромметана.
В) 2-бромпропана.
С) Бромэтана.
D) 1-бромпропана.
Е) 2-бромбутана.
30. Из этана в двух стадиях образуется :
А) Пентан.
В) Пропан.
С) Бутан.
D) 2,3-диметилпропан.
Е) Метан.
31. Автор реакции нитрования алканов:
А) Коновалов.
В) Кольбе.
С) Зинин.
D) Вюрц.
Е) Гофман.
32. Механизм реакции взаимодействия метана с хлором при облучении УФ-светом:
А) Нуклеофильное замещение.
B) Электрофильное присоединение.
C) Радикальное присоединение.
D) Радикальное замещение.
E) Электрофильное замещение.
33. Механизм реакции взаимодействия циклогексана с бромом при облучении УФ-светом:
А) Нуклеофильное замещение.
B) Электрофильное присоединение.
C) Радикальное присоединение.
D) Радикальное замещение.
E) Электрофильное замещение.
34. Механизм реакции взаимодействия пропана с бромом при облучении УФ-светом:
А) Нуклеофильное замещение.
B) Электрофильное присоединение.
C) Радикальное присоединение.
D) Радикальное замещение.
E) Электрофильное замещение.
35. Количество третичных атомов углерода в молекуле 2-метилбутана:
A) 1
B) 2
C) 3
D) 4
E) 5
36. Продуктом взаимодействия 2-метилбутана с 1 моль брома является:
A) 2-бром-2-метилбутан.
B) 2, 2-дибром-3-метилбутан.
C) 2-бром-3-метилбутан.
D) 2, 3-дибром-3-метилбутан.
E) 1-бром-3-метилбутан.
АЛКЕНЫ, ДИЕНЫ, АЛКИНЫ
1. Общая формула алкенов:
А) СnН2n+2
В) СnН2n
С) СnН2n -2
D) СnН2n-6
Е) СnН2n-1
2. Характерны для алкенов реакции:
А) АN
В) АR
С) SN
D) АE
Е) SE
3. СН2 = СН2 + НСl → СН3СН2Сl механизм реакции:
А) АE
В) АN
С) АR
D) SE
Е) SN
4. СН3 – СН = СН2 при присоединений НСl образует:
А) 1-хлорпропан.
В) 3-хлорпропен.
С) 1-хлорпропен.
D) 2-хлорпропен.
Е) 2-хлорпропан.
5. Из алкенов под действием водного раствора КМnО4 образуются:
А) Диолы.
В) Одноатомные спирты.
С) Альдегиды.
D) Кетоны.
Е) Диены.
6. При внутримолекулярной дегидратации бутанола-2 образуется:
А) Бутен-1
В) Бутен-2
С) Бутин-2
D) Бутин-1
Е) Бутан.
7. Характерны для алкадиенов реакции:
А) АN
В) E
С) SN
D) SE
Е) АE
8. К алкенам относится:
А) Гексан.
В) Пропилен.
С) Пропан.
D) Циклогексан.
Е) Бензол.
9. Для алкенов наиболее характерны реакции:
А) Радикального замещения.
В) Электрофильного присоединения.
С) Элиминирования.
D) Электрофильного замещения.
Е) Нуклеофильного замещения.
10. В результате присоединения воды к алкенам (реакция гидратации) получается:
А) Алкан.
В) Спирт.
С) Кислота.
D) Алкин.
Е) Альдегид.
11. При присоединении к пропену по правилу Марковникова йодоводородной кислоты получается:
А) 2-йодпропан.
В) 1-йодпропан.
С) 1-йодбутан.
D) 1-йодпропин.
Е) 1-йодбутин.
12. В результате реакции гидратации 2-метилпропена образуется:
А) Пропанол-2.
В) 2-метилпропанол-2.
С) Этанол.
D) Бутанол-1.
Е) Метанол.
13. При взаимодейтсвии воды с карбидом кальция СаС2 образуется:
А) Этилен.
В) Этан.
С) Пропан.
D) Бутан.
Е) Ацетилен.
14. Образуется при гидрировании алкена:
А) Алкан.
В) Алкин.
С) Спирт.
D) Кислота.
Е) Альдегид.
15. Углеводород состава С5Н10, обесцвечивает бромную воду и водный раствор КМпO4, окисляется в уксусную и пропионовую кислоту. Название углеводорода:
А) 1-пентен.
В) 1-пентин.
С) 2-метил-2-бутен.
D) 2-пентен.
Е) 2-метил-1-бутен.
16. При гидратации ацетилена по реакции Кучерова образуется:
А) Этиловый спирт.
В) Этилен.
С) Этан.
D) Ацетальдегид.
Е) Ацетон.
17. При взаимодействии этилена с хлороводородом образуется:
А) Хлорэтан.
В) 1,2-дихлорэтан.
С) 1,1-дихлорэтан.
D) 1,1,2,2-тетрахлорэтан.
Е) Этан.
18. sр Гибридизация характерна для:
А) Алканов.
В) Алкенов.
С) Алкинов.
D) Алкадиенов.
Е) Аренов.
19. Структурные изомеры:
А) Бутен-2 и пентен-2.
В) 2-метилбутан и 2-метилбутен-1.
С) Бутен-1 и бутен-2.
D) Пропен и бутен-1.
Е) Бутен-1 и пентен-1.
20. В результате бромирования этилена образуется:
А) 1,2 – дибромэтен.
В) 1,1 – дибромэтен.
С) 1,1 – дибромэтан
D) 1,2 – дибромэтан
Е) Бромэтан
21. Бутен – 1, бутен – 2 и 2 – метилпропен являются:
А) Гомологами.
В) Радикалами.
С) Карбкатионами.
D) Изомерами.
Е) Эпимерами.
22. Общая формула алкадиенов:
А) CnH2n+2
В) CnH2n-2
С) CnH2n
D) CnH2n-6
Е) C2nH2n+2
23. Диен, обладающий большой термодинамической устойчивостью:
А) Бутадиен – 1,3.
В) Бутадиен – 1,2.
С) Пентадиен – 1,2.
D) Пентадиен – 1,4
Е) Гексадиен – 1,2.
24. Общая формула алкинов:
А) CnH2n+2
В) CnH2n-2
С) CnH2n
D) CnH2n-6
Е) C-2nH2n+2
25. Радикал НС ≡ С –
А) Этил.
В) Винил.
С) Этинил.
D) Пропил.
Е) Аллил.
26. Продукт гидрирования пропина:
А) Пропен.
В) Пропанол – 1.
С) Пропаналь.
D) Ацетон.
Е) Пропанол – 2.
27.
В результате реакции Н3С
– С ≡ СН + 2НСl
образуется: 
А) 1,2 – дихлорпропан.
В) 1,1 – дихлорпропан.
С) 2 – хлорпропан.
D) 2,2 – дихлорпропан.
Е) 1 – хлорпропан.
28. Продукт присоединения воды к ацетилену (реакции Кучерова):
А) Уксусный альдегид.
В) Бутанон – 2.
С) Ацетон.
D) Винилацетилен.
Е) Дивиниловый эфир.
29. В результате реакции озонирования бутена-2 и последующего гидролиза озонида образуется:
А) Трехатомный спирт.
В) Двухатомный спирт.
С) 2 молекулы карбоновой кислоты.
D) 2 молекулы альдегида.
Е) 2 молекулы спирта.
30. Продукт дегидрогалогенирования 2-бромбутана:
А) Бутен-1.
В) Бутан.
С) Этилэтилен.
D) Сим. диметилэтилен.
Е) Триметилэтилен.
31. При гидратации в кислой среде бутена-1 образуется:
А) Бутанол-1.
В) Бутанол-2.
С) 2-метилпропанол-2.
D) 2-метилпропанол-1.
Е) Бутаналь.
32. При внутримолекулярной дегидратации 3-метилбутанола-2 образуется алкен:
А) Изопропилэтилен.
В) Метилэтилэтилен.
С) 3-метилбутен-1.
D) 2-метилбутен-1.
Е) Триметилэтилен.
33. При обработке разбавленным раствором КМnО4 (реакция Вагнера) дает бутандиол-2,3:
А) Пропен.
В) 2-метилпропен.
С) Бутен-1.
D) Бутен-2.
Е) Этилэтилен.
34. Присоединение хлороводорода осуществляется не по правилу Марковникова у вещества:
А) СН2 = СН – СН3
В) СН2 = СН – СI
С) СН2 = СН – СНО
D) СН3 – СН = СН – СН3
Е) СН3 – СН = СН – СНО
35. Для того, чтобы качественно отличить этилен от ацетилена, можно использовать химическую реакцию:
А) Этилена с бромной водой.
В) Ацетилена с бромной водой.
С) Ацетилена с хлоридом меди (1).
D) Этилена с водой.
Е) Этилена с перманганатом калия.
36. Является мономером природного каучука:
А) Метилакрилат.
В) Бутадиен-1,3.
С) Хлоропрен.
D) Изобутилен.
Е) Изопрен.
37. При мягком окислении этилена образуется:
А) Уксусный альдегид.
В) Уксусная кислота.
С) Щавелевая кислота.
D) Этиленгликоль.
Е) Этанол.
38. Соединения, обесцвечивающие бромную воду:
1. алкены, 2. алканы, 3. диены, 4. спирты
А) 2,3
В) 1,2
С) 1,3
D) 3,4
Е) 2,4
39. При гидратации в кислой среде метилпропена образуется спирт:
А) Бутанол-1.
В) Бутанол-2.
С) 2-метилпропанол-2.
D) 2-метилпропанол-1.
Е) Пропанол-2.
40. Ацетилен получают действием воды на:
А) Карбид алюминия.
В) Карбонат кальция.
С) Карбид кальция.
D) Карбид натрия.
Е) Ацетат натрия.
41. Ацетилен как кислота реагирует с:
А) К
В) КОН
С) КСN
D) K2CO3
Е) KNO2
42. Образуется уксусный альдегид по реакции Кучерова при гидратации:
А) Этена.
В) Пропина.
С) 1-бутина.
D) 2-бутина.
Е) Этина.
43. Применяется для качественной реакции на двойную связь:
А) Гидроксид меди (II).
B) Уксусная кислота.
C) Гидроксид натрия.
D) Гидроксид меди (I).
E) Бромная вода.
44. Можно доказать наличие двойной связи с помощью:
A) Раствора щелочи.
B) Раствора хлорного железа.
C) Гидроксида меди.
D) Бромной воды.
E) Аммиачного раствора гидроксида серебра.
45. Образуется в результате реакции:
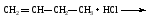
A) 1-хлорбутан.
B) 2-хлорбутан.
C) 1, 2-дихлорбутан.
D) 2, 2-дихлорбутан.
E) 1, 1-дихлорбутан.
46. Механизм реакции:

A) Нуклеофильное замещение.
B) Окисление-восстановление.
C) Электрофильное присоединение.
D) Радикальное присоединение.
E) Нуклеофильное присоединение.
47. Способно взаимодействовать с 1 моль хлороводорода:
A) Бензол.
B) Пропен.
C) Пропан.
D) Циклопентан.
E) Бутан.
48. Используется для отличия этилена от ацетилена:
A) Бромная вода.
B) Раствор перманганата калия.
C) Аммиачный раствор гидроксида серебра.
D) Водород.
E) HCl.
49. Тип реакции ацетилена с гидроксидом меди (1):
A) Присоединение.
B) Замещение.
C) Окисление.
D) Отщепление.
E) Восстановление.
50. Образует бутен-2 при дегидрогалогенировании:
A) CH3 – CH2 – CH2 – CH2 – Br
B) CH3 – CHBr – CH2 – CH3
C) Br – CH2 – CH2 – CH2 – CH2 – Br
D) Br – CH = CH – CH2 – CH3
E) Br – CH2 – CH2 – CH = CH2
51. Механизм реакции бромирования этилена:
A) Нуклеофильное присоединение.
B) Электрофильное присоединение.
C) Нуклеофильное замещение.
D) Электрофильное замещение.
E) Радикальное замещение.
52. При взаимодействии пропина с 2 моль бромоводорода образуется:
A) 1, 2-дибромпропан.
B) 1, 1-дибромпропан.
C) 2, 2-дибромпропан.
D) 2-бромпропен.
E) 1-бромпропен.
53. Механизм реакции взаимодействия пропена с водой в кислой среде:
A) Нуклеофильное присоединение.
B) Электрофильное присоединение.
C) Радикальное присоединение.
D) Электрофильное замещение.
E) Элиминирование.
54. Кумулированный диен:
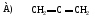
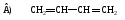
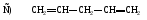
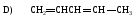

55. Изолированный диен:
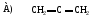
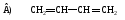
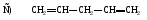

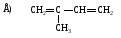
56. Сопряженный диен:
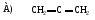


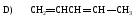
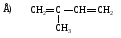
АРЕНЫ
1. По правилу Хюккеля в ароматических соединениях число электронов в π – системе определяет формула:
А) 4n + 2
В) 2n + 4
С) n + 4
D) 4n + 4
Е) 2n + 6
2. Реакции характерные для ароматических соединений:
А) SR
В) АE
С) SE
D) АN
Е) SN
3. При бромировании нитробензола (в присутствии FeBr3) образуется:
А) о – бромнитробензол.
В) п – бромнитробензол.
С) 2,4,6 - трибромнитробензол
D) 3,5 - дибромбензол
Е) м - бромнитробензол
4. При нитровании анилина (в присутствии Н2SO4) образуются:
А) 3,5 – динитроанилин.
В) 2,4,6 – тринитроанилин.
С) 3 – нитроанилин.
D) 2 – нитроанилин.
Е) 4 – нитроанилин.
5. При хлорировании бензола на свету образуется:
А) Дихлорциклогексадиен.
В) Тетрахлорциклогексан.
С) Хлорбензол.
D) Гексахлорциклогексан.
Е) Дихлорбензол.
6. Общая формула простейших аренов:
А) СnН2n+4
В) СnН2n+2
С) СnН2n
D) СnН2n-2
Е) СnН2n-6
7. Легче сульфируется:
А) Бензойная кислота.
В) Метоксибензол.
С) Бензальдегид.
D) Нитробензол.
Е) Бромбензол.
8. Труднее нитруется нитрующей смесью:
А) Бензол.
В) Этилбензол.
С) Ацетофенон.
D) Этоксибензол.
Е) Изопропилбензол.
9. К ароматическим соедниениям не относится:
А) Бензол.
В) Нафталин.
С) Этанол.
D) Ксилол.
Е) Стирол.
10. Для аренов наиболее характерны реакции:
А) Радикального замещения.
В) Электрофильного присоединения.
С) Элиминирования.
D) Электрофильного замещения.
Е) Нуклеофильного присоединения.
11. Электроноакцепторные заместители в ароматическом ядре на реакционную способность электрофильного замещения оказывают влияние:
А) Активизируя бензольное ядро.
В) Дезактивизируя бензольное ядро.
С) Активизируя, затем дезактивируя.
D) Дезактивизируя, затем активируя.
Е) Не оказывают никакого влияния.
12. Электронодонорные заместители в ароматическом ядре на реакционную способность электрофильного замещения оказывают влияние:
А) Активизируя бензольное ядро.
В) Дезактивизируя бензольное ядро.
С) Активизируя, затем дезактивируя.
D) Дезактивизируя, затем активируя.
Е) Не оказывают никакого влияния.
13. При нитровании бензойной кислоты образуется продукт:
А) о-нитробензойная кислота.
В) м-нитробензойная кислота.
С) п-нитробензойная кислота.
D) Смесь орто и пара-нитробензойной кислот.
Е) п-аминобензойная кислота.
14. При алкилировании бензола бромметаном в присутствии катализатора образуется продукт:
А) Бромэтилбензол.
В) Бромбензол.
С) Этилбензол.
D) Толуол.
Е) Фенол.
15. При алкилировании бензола хлорметаном в присутствии катализатора образуется продукт:
А) Хлорэтилбензол.
В) Хлорбензол.
С) Этилбензол.
D) Толуол.
Е) Фенол.
16. Общая формула углеводородов гомологического ряда бензола:
А) CnH2n+2
В) CnH2n-2
С) CnH2n
D) CnH2n-6
Е) C-2nH2n+2
17. Ароматическое соединение:
А) Ацетилен.
В) Циклогексан.
С) Толуол.
D) Циклобутан.
Е) Бутадиен – 1,3.
18. Радикал бензола:
А) Фенил.
В) Бензил.
С) о – Толил.
D) п – Толил.
Е) м – Толил.
19. Радикал C6H5 – CH2 – называется:
А) Фенил.
В) Бензил.
С) Циклогексил.
D) п – Толил.
Е) м – Толил.
20. Многоядерный арен:
А) Ксилол.
В) Стирол.
С) Бензол.
D) Нафталин.
Е) Фенол.
21. Реакция галогенирования бензола проходит при наличии катализатора:
А) Рt
В) FeCl3
С) Pd
D) Ni
Е) H2SO4
22. Группы, направляющие новый заместитель в бензольном ядре в орто - и пара - положения:
А) – ОН, – СН3, –NН2, –Cl
В) – ОН, – ОСН3, –NН2, – SO3Н
С) – ОСОСН3, – NНR2, – NO2, – СН2Cl
D) – NНR2, – NНОСОСН3, – СН3, – С ≡ N
Е) – SO3Н, = С = О, – NО2, – СООС2Н5
23. Группы, направляющие новый заместитель в бензольном ядре в мета - положения:
А) – ОН, – СН3, –NН2, –Cl
В) – ОН, – ОСН3, – NН2, – SO3Н
С) – ОСОСН3, – NНR2, – NO2, – СН2Cl
D) – NНR2, – NНОСОСН3, – СН3, – С ≡ N
Е) – SO3Н, = С = О, – NО2, – СООС2Н5
24. Продукт присоединения хлора к бензолу при УФ – излучении:
А) Гексахлорциклогексан.
В) Хлорбензол.
С) Монохлорциклогексан.
D) 1,2 – дихлорбензол.
Е) Дихлорциклогексан.
25. Автор реакции алкилирования бензола в присутствии катализатора AlCl3 до этилбензола:
А) Вюрц.
В) Вюрц – Фиттиг.
С) Фридель – Крафтс.
D) Кольбе.
Е) Зинин.
26. Образует в результате циклической тримеризации бензол :
А) Гексин-1.
В) Пропин.
С) Гексин-2.
D) Этилен.
Е) Этин.
27. Образует в результате циклической тримеризации 1,3,5-триметилбензол:
А) Этин.
В) Пропин.
С) Гексин-2.
D) Гептин.
Е) Октин-1.
28. Вступает в реакцию SE по согласованной ориентации:
А) 1,2-диметилбензол.
В) п-хлортолуол.
С) м-нитротолуол.
D) п-нитрохлорбензол.
Е) м-толуиловая кислота.
29. При взаимодействии брома со стиролом в обычных условиях образуется:
А) о-бромстирол.
В) п-бромстирол.
С) м-бромстирол.
D) 1,2-дибром-1-фенилэтан.
Е) 2,6-дибром-1-винилбензол.
30. При полном гидрировании стирола образуется:
А) Этилбензол.
В) Этилциклогексан.
С) Этинилциклогексан.
D) Винилциклогексан.
Е) Этинилбензол.
31. При окислении бензола кислородом воздуха в присутствии V2О5 образуется:
А) Малеиновая кислота.
В) Бензойная кислота.
С) Бензальдегид.
D) Фталевая кислота.
Е) Щавелевая кислота.
32. При окислении нафталина кислородом воздуха в присутствии V2О5 образуется:
А) Малеиновая кислота.
В) Бензойная кислота.
С) Нафтохиноны.
D) Фталевая кислота.
Е) Щавелевая кислота.
33. В молекуле антрацена особенно подвижны водороды в положениях:
А) 1 и 2
В) 2 и 3
С) 3 и 4
D) 9 и 10
Е) 1 и 4
34. Труднее нитруется с нитрующей смесью:
А) Толуол.
В) Этилбензол.
С) Метоксибензол.
D) Бензойная кислота.
Е) Пропилбензол.
35. Трифенилметан можно получить по реакции:
А) Фриделя-Крафтса из фосгена и бензола.
В) Фриделя-Крафтса из хлороформа и бензола.
С) Вюрца-Фиттига из хлорбензола и хлороформа.
D) Восстановления бензофенона.
Е) Окисления тетрафенилметана.
36. Заместителям первого рода относятся:
А) – OH, – OCH3, – NH2, – SO3H
В) – OCOCH3, – NHR2, – NH2, – CCI3, – CH2CI
С) – NHR, – NHCOCH3, – NR3, – C N, – COOCH3
D) – OC2H5, – NHCH3, – CH3, – NH2,
Е) – COCH3, – CH = O, – C2H5, – OCOC2H5, – NHC2H5
37. При метилировании образует п-толуидин:
А) Анилин.
В) Нитробензол.
С) Толуол.
D) Ксилол.
Е) Фенол.
38. Взаимодействует с толуолом по механизму SR:
А) Br2 (FeBr3)
B) H2SO4
C) CI2 (h)
D) О2 (V2O5)
Е) О3
39. Механизм реакции этилбензола с азотной кислотой:
А) Электрофильное замещение.
B) Электрофильное присоединение.
C) Нуклеофильное замещение.
D) Нуклеофильное присоединение.
E) Радикальное присоединение.
40. Образуется в результате взаимодействия толуола с азотной кислотой:
А) м – нитротолуол.
B) n – нитротолуол.
C) Нитробензол.
D) 3,5 – динитротолуол.
E) 2,3 – динитротолуол.
41. Ароматическое соединение:
А) Фенантрен.
B) Бутадиен.
C) Пергидрофенантрен.
D) Циклогексан.
E) Бутан.
42. Относится к ароматическим соединениям:
А) Нафталин.
B) Бутадиен.
C) Циклопентан.
D) Циклогексан.
E) Бутан.
43. Относится к ароматическим соединениям:
А) Антрацен.
B) Гексан.
C) Пергидрофенантрен.
D) Циклогексан.
E) Пентан.
44. Механизм реакции взаимодействия толуола с хлором при облучении УФ-светом:
А) Нуклеофильное замещение.
B) Электрофильное присоединение.
C) Радикальное присоединение.
D) Радикальное замещение.
E) Электрофильное замещение.
45. Радикал бензола называется:
A) Фенил.
B) Бензил.
C) Винил.
D) Аллил.
E) Бензоил.
46. Продукт взаимодействия бензола с серной кислотой:
A) Сложный эфир.
B) Сульфоновая кислота.
C) Простой эфир.
D) Ангидрид.
E) Соль.
47. Относится к ароматическим соединениям:
A) Пергидрофенантрен.
B) Бутадиен-1,3.
C) Циклогексан.
D) Фенантрен.
E) Гексан.
48. Механизм реакции взаимодействия бензола с ацетилхлоридом в присутствии AlCl3:
A) Электрофильное замещение.
B) Электрофильное присоединение.
C) Нуклеофильное замещение.
D) Нуклеофильное присоединение.
E) Радикальное присоединение.
49. Обесцвечивает бромную воду:
A) Винилбензол.
B) м-диметилбензол.
C) n-диметилбензол.
D) Бензол.
E) Нитробензол.
50. Механизм реакции взаимодействия пропилбензола с бромом при облучении УФ светом:
A) Нуклеофильное замещение SN.
B) Электрофильное присоединение АE.
C) Радикальное замещение SR.
D) Радикальное присоединение А R.
E) Электрофильное замещение SE.
51. Механизм реакции взаимодействия бензола с CH3Br в присутствии АlBr3:
A) Электрофильное замещение SE.
B) Нуклеофильное замещение SN.
C) Радикальное присоединение АR.
D) Радикальное замещение SR.
E) Электрофильное присоединение АE.
52. Механизм реакции бромирования анилина:
A) Радикальное замещение SR.
B) Электрофильное замещение SE.
C) Нуклеофильное присоединение АR.
D) Нуклеофильное замещение SN.
E) Электрофильное присоединение АE.
53. Механизм и продукт реакции взаимодействия бензола с хлором при облучении УФ светом:
A) Хлорбензол SE.
B) Дихлорбензол SN.
C) Гексахлорциклогексан АR.
D) Гексахлорбензол SE.
E) Гексахлорбензол SR.
