- •Полимеризуемые стоматологические адгезивы и композиты. Обзор.
- •Реферат
- •Список принятых сокращений
- •Содержание
- •Введение
- •Основные направления исследований полимеризуемых стоматологических материалов Адгезионные системы
- •Восстановительные пломбировочные материалы Композиты
- •Классификация композитов
- •Модификация полимерной матрицы Мономеры с раскрывающимися кольцами Спироортокарбонаты
- •Циклические эфиры
- •Циклические ацетали и аллилсульфиды
- •Винилциклопропаны
- •Жидкокристаллические, разветвленные и дендриновые мономеры Жидкокристаллические мономеры
- •Разветвленные и дендриновые мономеры
- •Компомеры
- •Ормокеры
- •Аналоги и заместители Bis-gma
- •Фторированные аналоги Bis-gma
- •Заместители Bis-gma
- •Рентгеноконтрастные мономеры
- •Антикариозные мономеры
- •Модификация наполнителей
- •Биоактивные наполнители
- •Наполнители, уменьшающие напряжения усадки
- •Армированные композиты и наночастицы
- •Модификация добавок Инициирующие системы
- •Специальные добавки
- •Заключение
- •Литература
Циклические эфиры
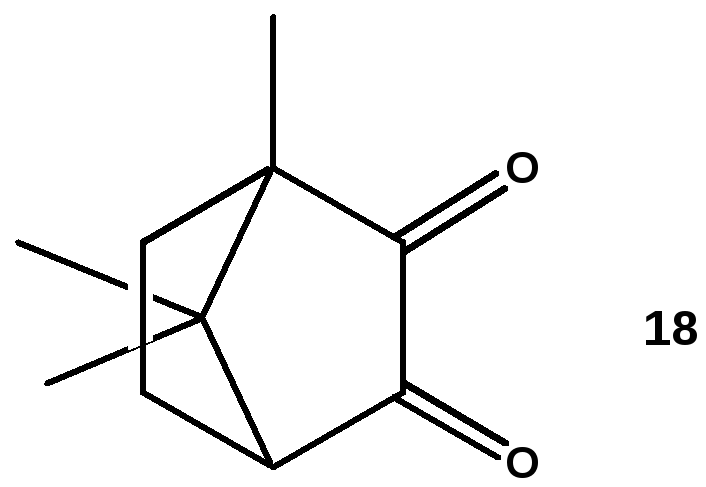
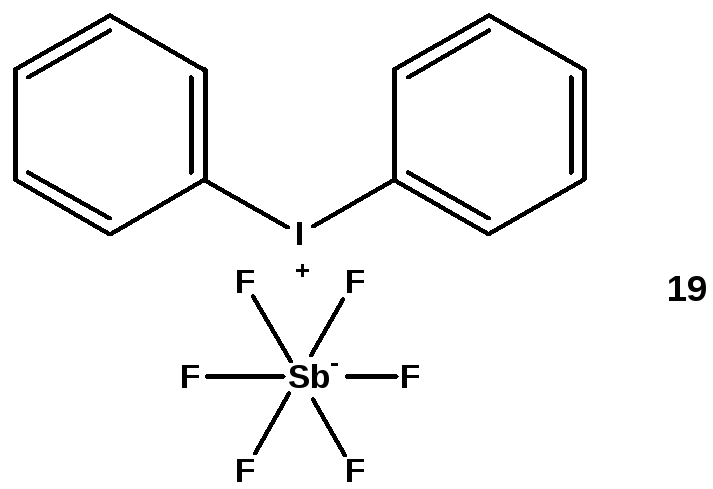
В последние годы внимание исследователей привлекли циклоалифатические эпоксидные соединения, способные к катионной полимеризации при фотоинициировании с низкой усадкой [38,39]. Пример одного из фотоотверждаемых составов приведен на рис. 11. Состав содержит смесь двух катионно-полимеризуемых диэпоксидов: 3,4-эпоксициклогексил-метил-3,4-эпоксициклогексан карбоксилата (структура 17) и диглицидиловый эфир бисфенола А. В качестве активного разбавителя и ускорителя фотоотверждения используется поли(тэтрагидрофуран). Камфорохинон (структура 18), обычно применяемый как фотоинициатор, в данном случае выполняет роль сенсибилизатора (активатора). А фотоинициатором служит дифенилиодиниум гексафторантимонат (структура 19). Вариантами подобных катионно-полимеризуемых составов являются композиции, содержащие другие циклоалифатические диэпоксиды, например диэпоксид структуры 20 (рис. 12), другие катионные фотоинициаторы типа ароматических солей сульфония или ферроцена и другие фотоактиваторы типа этил 4-диметиламинобензоата (структура 21 на рис. 12).
|
9,43% |
Диглицидиловый эфир бисфенола А |
|
|
9,14% |
3,4-Эпоксициклогексил-метил-3,4-эпоксициклогексан карбоксилат |
|
|
4,66% |
Поли(тэтрагидрофуран) с молекулярной массой 250 |
|
|
0,11% |
Камфорохинон |
|
|
0,11% |
Соль иодония |
|
|
76,55% |
Кварцевый наполнитель |
|
Рисунок 11. Состав (% масс.) композита основанного на свето-отверждаемых эпоксидных смолах [38].
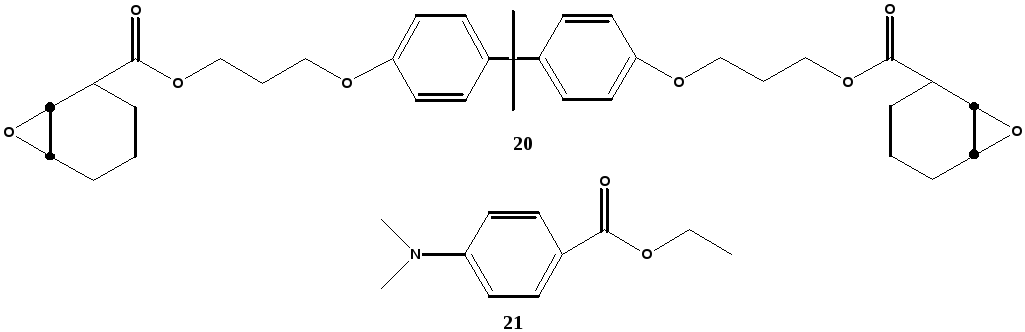
Рисунок 12. Компоненты, улучшающие составы эпоксидных смол [38].
Наряду с эпоксидными смолами для стоматологического применения были предложены оксетаны, которые также активно полимеризуются при катионном фотоинициировании с низкой усадкой (структуры 22-24 на рис. 13).
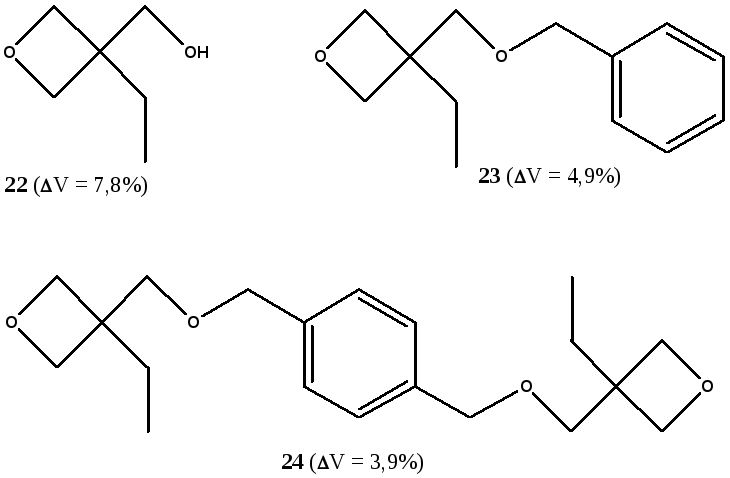
Рисунок 13. Структуры и объемная усадка оксетанов 22-24 при катионной фотополимеризации, инициируемой бис-[4-(дифенилсульфонио)-фенил]-сульфид-бисгексафторфосфатом [38].
Несмотря на ряд преимуществ по сравнению с диметакрилатами, циклические эфиры имеют свои недостатки (табл. 11).
Таблица 11. Преимущества и недостатки фотоотверждаемых композитов на основе циклических эфиров, катионно-полимеризуемых с раскрытием циклов.
|
Преимущества |
Недостатки |
|
Низкая полимеризационная усадка |
Скорость отверждения при комнатной температуре намного ниже |
|
Низкая чувствительность к кислороду |
Чувствительны к основаниям (аминам, уретанам, пигментам или наполнителям) |
|
Отличные адгезионные свойства полимеров |
Чувствительность к влаге (вода является агентом передачи цепи) |
|
Хорошая химическая устойчивость полимеров |
Кислотные примеси влияют на стабильность при хранении |
|
Возможны гибридные системы с метакрилатами |
Высокое водопоглощение полимеров |
|
|
Токсикологический риск эпоксидов и фотоинициаторов |
|
|
Нет достаточного опыта применения этих материалов |
Циклические ацетали и аллилсульфиды
Циклические кетенацетали полимеризуются с раскрытием кольца по свободно-радикальному и катионному механизму с незначительной усадкой, что делает их перспективными мономерами для стоматологических материалов. Впервые различные 1,3-диоксаланы были исследованы в качестве стоматологических мономеров в 1972 г [38] (рис.14).
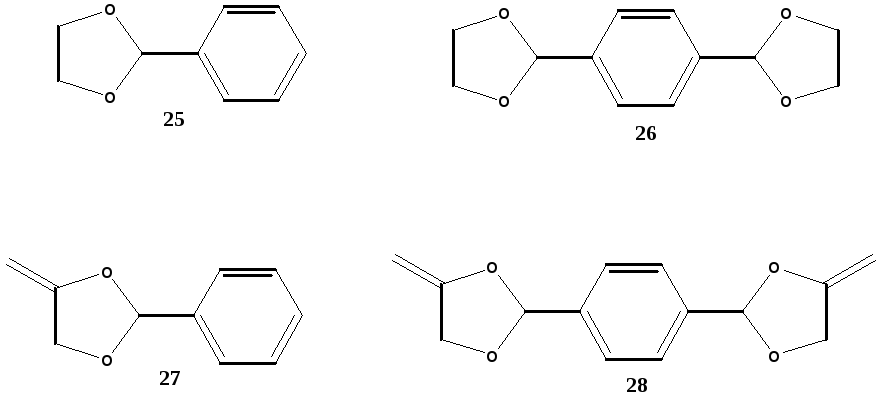
Рисунок 14. Не-винильные 25-26 и винильные 27-28 1,3-диоксаланы изученные в стоматологических композитах [38].
Более перспективным мономером является семичленный циклический винильный кетен ацеталь – 2-метилен-1,3-диоксепан (структура 29 на рис. 15). Он полимеризуется с раскрытием кольца до высоких степеней конверсии при фото- и термо- инициировании, давая особо чистый поли(-капролактон) (рис. 15).
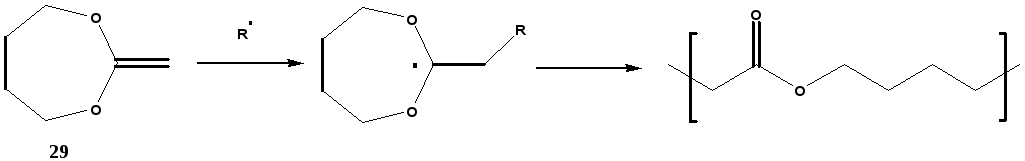
Рисунок 15. Механизм свбодно-радикальной полимеризации с раскрытием кольца 2-метилен-1,3-диоксепана 29 [38].
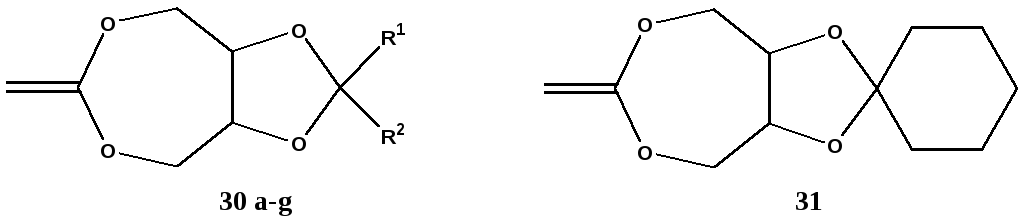
Далее были синтезированы бицикличные 2-метилен-1,3-диоксепаны (структура 30-31 на рис. 16) [47]. Мономер 30gпоказал при полимеризации объемное расширение 2,9% за счет превращения более плотной структуры кристаллического мономера в менее плотную структуру аморфного полиэфира. К сожалению полиэфиры на основе данных мономеров имели температуру стеклования от –8 до 350С, что было неприемлемо для стоматологического применения. Кроме того, 2-метилен-1,3-диоксепаны, как обогащенные электронами олефины, очень чувствительны к воде и нуклеофильным соединениям (аминам, спиртам и т.д.). Пасты композитов на их основе, особенно со стеклонаполнителем, оказались не стабильны при хранении и склонными к спонтанному отверждению в течение нескольких дней. Наконец, 2-метилен-1,3-диоксепаны были значительно менее реакционно-способны, чем метакрилаты.
|
R1 |
CH3 |
C2H5 |
C2H5 |
Фенил |
CH=CH2 |
3-CH3-фенил |
4-CH3-фенил |
|
R2 |
CH3 |
CH3 |
H |
H |
CH3 |
H |
H |
|
30 |
a |
b |
c |
d |
e |
f |
g |
Рисунок 16. Бицикличные 2-метилен-1,3-диоксепаны [38].
Более стабильными в присутствии воды оказались циклические аллилсульфиды. Например, 6-метилен-1,4-дитиэпан или 3-метилен-1,5-дитиациклооктан (структуры 32 и 33 на рис. 17, соответственно) спокойно выдерживали воздействие воды и кислот. Циклические аллилсульфиды полимеризовались с раскрытием кольца по свободно-радикальному механизму, давая нерастворимые кристаллические высокомолекулярные гомополимеры. Жидкие 6-метилен-1,4-дитиэпаны (структуры 34-33 на рис. 18) приводят к сшитым полимерам.
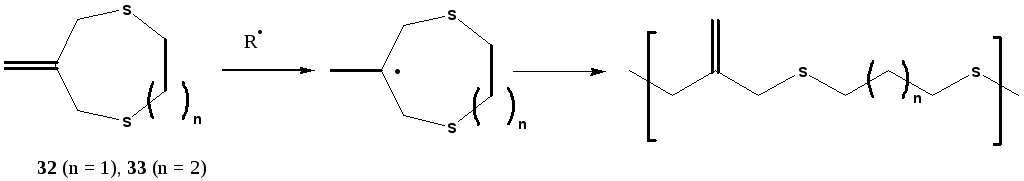
Рисунок 17. Свободно-радикальная полимеризация с раскрытием кольца циклических аллилсульфидов [38].
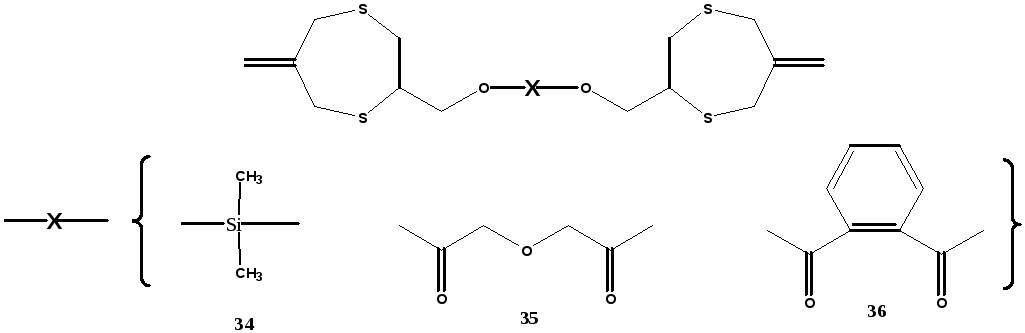
Рисунок 18. Структуры жидких 6-метилен-1,4-дитиэпанов 34-36 [38].
Главной проблемой применения циклических аллилсульфидов в стоматологических материалах является значительно меньшая реакционная способность этих мономеров по сравнению с метакрилатами и слишком гибкая аморфная структура, образующихся полимеров.