
ИВЛ - Сатишур
.pdf
Глава 1. Физиология и патофизиология внешнего дыхания |
I |
|
сурфактанта внутри нее и тем эффектив |
стической тяги легочной ткани в плев |
|
нее снижается поверхностное натяжение. |
ральной полости создается отрицатель |
|
Когда альвеолы растянуты, концентрация |
ное давление. При расширении грудной |
|
сурфактанта снижается, таким образом, |
клетки в начале вдоха отрицательное |
|
поверхностное натяжение возрастает, об |
давление в плевральной полости возра |
|
легчая выдох. Конечное действие сурфак |
стает, что приводит к поступлению ат |
|
танта состоит в стабилизации альвеол: бо |
мосферного воздуха в легкие и их рас |
|
лее мелкие альвеолы защищены от |
правлению. Нарушение герметичности |
|
дальнейшего спадения, большие — от |
плевральной полости (пневмоторакс) |
|
чрезмерного перерастяжения. Большое |
вызывает коллапс легочной ткани и |
|
количество альвеол (до 300 миллионов у |
дискоординацию биомеханики дыхания. |
|
взрослых) формирует огромную площадь |
|
|
газообмена — 80—90 м2. |
Регуляция дыхания |
|
|
|
|
Правое и левое легкое заключены в |
Самостоятельное дыхание управляется |
|
грудную клетку и разделены средосте |
|
|
нием, в котором расположены сердце, |
дыхательным центром, представляющим |
|
крупные сосуды и пищевод. Правое |
собой сложную функциональную систе |
|
легкое состоит из трех долей, левое — |
му. Он состоит из центральных и пери |
|
из двух. Доли разделяются на сегмен |
ферических дыхательных хеморецепто- |
|
ты и дольки. Каждая долька соответ |
ров, двух групп медуллярных нейронов, |
|
ствует объему легочной ткани, вентили |
а также эфферентной системы, по кото |
|
руемому одной бронхиолой. Легочная |
рой передается команда к дыхательным |
|
ткань снаружи и грудная клетка изнут |
мышцам. Дыхательный центр обладает |
|
ри покрыты плевральными мембранами |
автоматизмом (например, обеспечивает |
|
(соответственно висцеральной и пари |
регуляцию дыхания во время сна), а так |
|
етальной плеврой), между которыми |
же изменяет паттерны внешней вентиля |
|
располагается плевральная полость |
ции под влиянием импульсов со сторо |
|
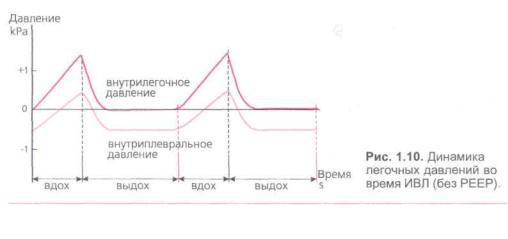
(рис. 1.6). Вследствие постоянной эла |
ны хеморецепторов (рис. 1.7). |
|

8 Часть I. Общие вопросы вентиляции легких
I |
Центральные хеморецепторы распо |
лагаются в продолговатом мозге и реа |
|
гируют на изменения рН цереброспи |
|
нальной жидкости (ЦСЖ). Уровень рН |
|
|
ЦСЖ очень чувствителен к изменени |
|
ям РаСОг При увеличении РаС02 про |
|
исходит снижение рН ЦСЖ, от хеморе- |
|
цепторов начинает поступать мощная |
|
импульсация в дыхательный центр, что |
|
приводит к увеличению минутной вен |
|
тиляции за счет, прежде всего, учаще |
|
ния дыхания. Метаболический ацидоз |
|
(особенно декомпенсированный) за счет |
|
снижения рН ЦСЖ также является |
|
мощным стимулятором дыхательного |
|
центра: организм пытается компенсиро |
|
вать ацидоз за счет гипервентиляции. |
|
Данное обстоятельство следует учиты |
|
вать при возникновении проблем с син |
|
хронизацией больного на аппаратном |
|
дыхании. У больных с выраженной хро |
|
нической обструктивной патологией |
|
легких (ХОЗЛ), когда имеет место хро |
|
ническая гиперкапния, дыхательный |
|
центр в значительно меньшей степени |
|
реагирует на изменения РаС02 (подроб |
|
нее см. главу 9; стр. 265). |
|
Периферические дыхательные хеморе |
|
цепторы расположены, в основном, в |
|
каротидных артериях и дуге аорты. Эти |
|
рецепторы реагируют преимущественно |
на снижение Ра02 и в меньшей степе ни — на снижение рН крови. На фоне снижения Ра02 импульсация в дыхатель ный центр со стороны периферических хеморецепторов вызывает учащение и углубление дыхания. Наиболее значимое влияние на дыхательный центр перифе рические рецепторы оказывают при сни жении Ра02 менее 70 мм рт.ст. (у боль ных ХОЗЛ — менее 60 мм рт.ст.).
Механика дыхания
Вентиляция легких происходит за счет периодических изменений работы дыха тельных мышц, объема грудной полос ти и легких. Основными мышцами вдоха являются диафрагма и наружные межре берные мышцы. Во время их сокраще ния происходит уплощение купола ди афрагмы и приподнятие ребер кверху, в результате объем грудной клетки увели чивается (рис. 1.8) и растет отрицатель ное внутриплевральное давление (Ppl). Перед началом вдоха (в конце выдоха) Ppl приблизительно составляет минус 5 мм вод.ст. Альвеолярное давление (Palv) принимается за 0 (т. е. равно атмосфер ному), оно же отражает давление в ды хательных путях и коррелирует с внут-
10 Часть I. Общие вопросы вентиляции легких
I ным давлением, поэтому во время ап паратного вдоха внутриплевральное и внутрилегочное давление сразу растут вплоть до окончания вдоха (рис. 1.10), затем во время выдоха давление снижа ется. В течение почти всего аппаратно го вдоха параллельно растет и внутригрудное давление. Это способствует снижению венозного возврата к сердцу, увеличению легочного сосудистого со противления и ухудшению условий со кратимости миокарда.
Легочные объемы и спирометрия
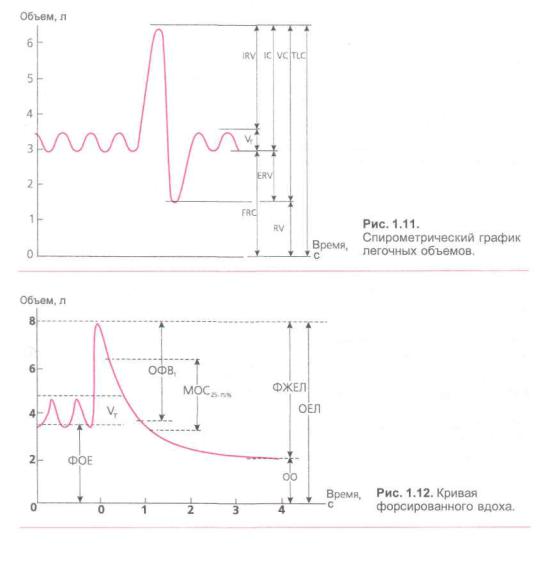
В физиологии дыхания различают не сколько динамических легочных объе мов, меняющихся в зависимости от фун кционального состояния системы внешнего дыхания. Определение легоч ных объемов производят с помощью спирометрии и спирографа — электрон ного или механического прибора, изме ряющего дыхательные потоки и объемы во время вдоха и выдоха. Полученные данные регистрируются и отображаются на специальной аналоговой шкале или цифровом дисплее. На основании дан ных спирометрии строится график ле гочных объемов (рис. 1.11).
Выделяют следующие основные ле гочные объемы (по русскоязычной и международной номенклатуре) (9, 26):
ДО — дыхательный объем (VT — Tidal Volume): это объем дыхательного газа во время спокойного вдоха и выдоха. У взрослых он составляет 7—9 мл/кг.
РОВд — резервный объем вдоха (IRV — Inspiratory Reserve Volume): дополни тельный объем, который человек может вдохнуть по окончании спокойного вдоха. В норме он составляет 2—2,5 л. РОВыд — резервный объем выдоха (ERV — Expiratory Reserve Volume): до полнительный объем, который человек может выдохнуть после окончания спо койного выдоха. В норме равен 1—1,5 л. Евд — емкость вдоха (1С — Inspiratory Capacity): объем максимального вдоха после спокойного выдоха. Равен сумме
ДО и РОВд (VT + IRV).
ЖЕЛ — жизненная емкость легких (VC — Vital Capacity). Один из важней ших показателей функции внешней вентиляции; представляет собой объем максимального выдоха (вдоха) после максимального вдоха (выдоха): ЖЕЛ = ДО + РОВыд + РОВд (VC - VT + ERV + IRV). В норме ЖЕЛ составляет 60— 70 мл/кг. Снижение показателя менее 40 мл/кг свидетельствует о серьезной функциональной недостаточности сис темы внешнего дыхания (снижение по датливости легких, прогрессировавие обструктивной патологии, нарушение нейромышечного управления дыханием и т.д.).
Глава 1. Физиология и патофизиология внешнего дыхания |
11 |
00 — остаточный объем (RV — Residual volume): объем, остающийся в легких после максимального выдоха. Составляет около 1,5—2 л.
ФОЕ — функциональная остаточная емкость (FRC — Functional residual volume): представляет собой объем газа, который остается в легких после спо койного выдоха. ФОЕ равен сумме РОВыд и 00 (FRC = ERV + RV) и составляет в норме 2,5—3,5 л. Косвен но ФОЕ коррелирует с площадью газо обмена. ФОЕ уменьшается при:
•ожирении;
•горизонтальном положении тела;
•снижении тонуса диафрагмы;
•беременности и гестозах;
•рестриктивной патологии легких.
ОЕЛ — общая емкость легких (TLC — Total lung capacity): объем легких во время максимального вдоха.
Во время спирометрии определяют также объем форсированного выдоха за 1 секунду (ОФВр или FEV,) (рис. 1.12): результаты принято выражать в процен-

12 Часть I. Общие вопросы вентиляции легких
тах ОФВ, (FEV,) по отношению к фор сированной жизненной емкости (ФЖЕЛ, FVC). В норме ОФВ, составляет 70— 80 % от ФЖЕЛ (FEV/FVC = 70-80 %). При обструктивной легочной патологии отношение FEV,/FVC снижается менее 50 %. Еще более точным показателем об структивной патологии легких является максимальная объемная скорость пото ка в середине форсированного выдоха
(MOC2S_75%, или FEF25„75), т. к. она не зависит от субъективного экспираторно
го усилия пациента (9).
Анализ спирометрических показателей позволяет косвенно судить о преимуще ственно рестриктивной или обструктив ной легочной патологии (таблица 1Л).
Объем закрытия легких
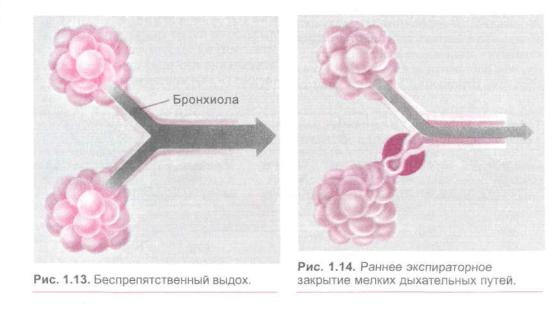
Во время выдоха дыхательные пути ис пытывают на себе давление со стороны
легочной ткани вследствие положитель ного внутриальвеолярного давления. В норме воздухоносные пути выдерживают такое напряжение, и выдох продолжает ся до полного уравновешивания давления между альвеолами и атмосферой (рис. 1.13). Однако при патологии дистальных дыхательных путей (не содержа щих хрящевых колец) их стенка стано вится менее упругой и легко подвергается сдавлению со стороны окружающей ле гочной ткани (рис. 1.14). На определен ной стадии выдоха бронхиола блокиру ется и часть выдыхаемого газа остается в альвеолах — развивается синдром «воз душной ловушки», или раннего экспира торного закрытия дыхательных путей (11, 12). Объем легких, при котором начина ют спадаться бронхиолы, называется ем костью закрытия легких. Если величина емкости закрытия приближается к ФОЕ, отмечается существенное ухудшение оксигенации. Дело в том, что «закрытые»
Глава 1. Физиология и патофизиология внешнего дыхания 13
альвеолы продолжают перфорироваться, но значительно хуже вентилируются; та ким образом, развивается шунтирование малооксигенированной крови справа на лево и гипоксемия. Феномен раннего эк спираторного закрытия бронхиол наблю дается при бронхиальной астме, ХОЗЛ, во время форсированного выдоха, в положе нии лежа на спине, а также может быть связан с возрастом (у пациентов старше 50 лет).
Во время ИВЛ предупредить либо уменьшить экспираторное закрытие мелких дыхательных путей можно с помощью создания ПДКВ (PEEP), ко торое приводит к увеличению объема легких (подробнее см. главу 4; стр. 72).
т. д.). В связи с этим в объеме общей минутной вентиляции (VE) выделяют альвеолярную минутную вентиляцию « (VA), непосредственно участвующую в га зообмене:
vA =f(vT -vr )
где VT — дыхательный объем, VD — объем анатомического мертвого пространства,
f — частота дыхания.
Величина VD составляет у взрослых около 2—2,2 мл/кг. Например, у чело века весом 70 кг VD будет приблизитель но равен 150 мл. Альвеолярная венти ляция при VT = 500 мл и ЧД = 14/мин составит:
Объем мертвого пространства
Объем газа в дыхательных путях и лег ких, не участвующий в газообмене, на зывается анатомическим мертвым про странством (VD). Иными словами, это объем дыхательного газа, не достигший альвеол. Он содержится и циркулирует в верхних и нижних дыхательных путях (носоглотка, гортань, трахея, бронхи и
V A = 14 х ( 5 0 0 - 1 5 0 ) = 4,7 л/мин
Величина VA колеблется у здоровых людей в пределах от 4 до 5 л/мин. Как видно из формулы, реальная альвеоляр ная вентиляция в большей степени сни жается при уменьшении дыхательного объема и частоты дыхания. При сниже нии дыхательного объема и росте часто ты дыхания минутная альвеолярная вен тиляция также уменьшается за счет значительного роста относительной ми-

14 Часть I. Общие вопросы вентиляции легких
нутной вентиляции мертвого простран ства (см. таблицу 1.2). Обращает на себя внимание, что минутная альвеолярная вентиляция снижается при уменьшении ДО и росте ЧД, хотя общий МОД оста ется неизменным. Наибольшая альвео лярная вентиляция наблюдается при до статочно большом ДО и редкой ЧД.
В патофизиологии дыхания важна не столько абсолютная величина VD, сколь ко отношение VD/VT, которое отражает степень участия подаваемого дыхатель ного объема в газообмене. Рассчитать VD/VT можно по модифицированному уравнению Бора:
где РА С02 — альвеолярное парциальное напряжение С02 , РЕ С02 — парциальное напряжение С0 2 в смешанном выдыхаемом воздухе.
РЛС02 приблизительно равно РаС02.
Внорме отношение VD/VT не превыша ет 0,3 (т. е. «мертвое пространство» со ставляет около 1/3 от вдыхаемого ды хательного объема).
Именно альвеолярная вентиляция VA определяет эффективность элиминации С02 из легких. При увеличении часто ты дыхания и снижении дыхательного объема рост вентиляции мертвого про странства происходит в большей степе ни, чем рост вентиляции альвеол. Таким образом, отношение VD/VT становится
> 0,3, и внешнее дыхание с точки зре ния удаления С02 оказывается значи тельно менее эффективным. Чрезмер ный уровень гиперкапнии может развиваться при VD/VT> 0,5, что наблю дается, например, при обострении ХОЗЛ. Альвеолы, в которых отсутству ет газообмен из-за недостаточной (отсут ствующей) перфузии, составляет альве олярное мертвое пространство. Сумма анатомического и альвеолярного мерт вого пространства называется физиоло гическим мертвым пространством (ФМП). Таким образом, ФМП представляет со бой фракцию дыхательного объема, ко торая не участвует в газообмене.
Вентиляционно-перфузионные соотношения
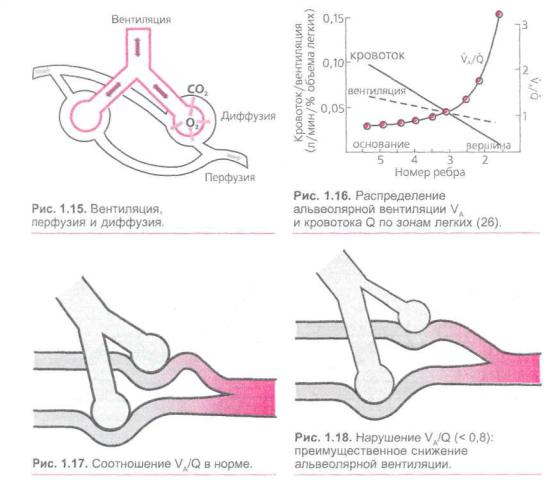
Вентиляция, перфузия и диффузия яв ляются основными компонентами газо обмена (рис. 1.15). Как в целом в лег ких, так и в отдельных их участках даже в норме не бывает абсолютно равного соотношения между вентиляцией и пер фузией. Например, в норме альвеоляр ная вентиляция (VA) составляет 4—4,5 л/ мин, а минутный объем кровообраще ния (Q) — 5~6 л/мин. К. тому же при дыхании в покое вентилируются не все зоны легких. Таким образом, в норме вентиляционно-перфузионное соотно шение (VA/Q) составляет 0,8—0,85.
Таблица 1.2. Динамика минутной альвеолярной вентиляции в зависимости от дыхательного объема и частоты дыхания (9, 26)
Дыхательный |
Мертвое пространство, |
Частота |
Минутная |
Минутный объем |
объем, мл |
мл (при массе |
дыхания, |
альвеолярная |
дыхания, л/мин |
|
тела 70 кг) |
в минуту |
вентиляция, л/мин |
|
|
|
|
|
|
800 |
150 |
10 |
6,5 |
8,0 |
667 |
150 |
12 |
6,2 |
8,0 |
533 |
150 |
15 |
5,75 |
8,0 |
400 |
150 |
20 |
5,0 |
8,0 |
250 |
150 |
32 |
3,2 |
8,0 |
Глава 1. Физиология и |
офизиология внешнего дыхания 15 |
Соотношение VA/Q очень неравномер но в различных зонах легких. В выше расположенных зонах (вне зависимос ти от того, стоит человек или лежит) вследствие большей величины транспульмонарного давления и большего размера альвеол значительно преоблада ет вентиляция (VA/Q > 2). В нижних отделах вследствие гравитации преобла дает перфузия (VA/Q < 0,7), а вентиля ция относительно снижена. Вот почему при длительной ИВЛ в положении на спине именно задне-базальные отделы легких наиболее подвержены ателектазированию, особенно при отсутствии или слабых движениях диафрагмы. На рисунке 1.16 показано распределение
вентиляции и кровотока в различных отделах легких.
В норме разные величины VA/Q в различных отделах легких в целом ком пенсируют друг друга и среднее соотно шение VA/Q= 0,8 остается достаточным для эффективного газообмена (рис. 1.17).
Преимущественное снижение вентиляции
Общее снижение VA/Q < 0,8 (рис. 1.18) приводит к тому, что кровь, протекаю щая через недостаточно вентилируемые или вообще невентилируемые альвеолы, значительно хуже оксигенируется. Раз-

16 Часть I. Обшие вопросы вентиляции легких
вивается патологическое шунтирование венозной крови справа налево со зна чительное снижение РаОг Такая альве олярная гиповентиляция развивается, например, при массивной пневмонии, ОРДС, тяжелой обструктивной патоло гии (в норме низкое VA/Q отмечается только в нижерасположенных отделах легких).
Для предотвращения чрезмерного снижения VA/Q и развития гипоксемии в организме человека срабатывает реф лекс Эйлера—Лилиестранда (рис. 1.19) (9, 26). Этот рефлекс заключается в вазоконстрикции мелких сосудов легких в тех зонах, где имеется альвеолярная гиповентиляция. Он является важным механизмом поддержания приемлемого VA/Q и предупреждения выраженного венозного шунтирования не только при патологии, но и в норме (в нижерасполо женных отделах легких с низким VA/Q). С другой стороны, в ситуации, когда имеются обширные зоны альвеолярной гиповентиляции, рефлекс Эйлера—Ли лиестранда может вызвать излишне вы сокое легочное сосудистое сопротивле ние и рост нагрузки на правые отделы сердца.
Венозное шунтирование справа нале во существует и в норме, однако не превышает 5 % от всего минутного объема кровообращения в легких.
Преимущественное снижение легочной перфузии
При выраженном снижении перфузии (ТЭЛА, тяжелая гиповолемия) альвео лы вентилируются, однако плохо или вообще не перфузируются (рис. 1.20). В этом случае VA/Q увеличивается и суще ственно возрастает объем физиологичес кого мертвого пространства — развива ется эффект «анатомического» шунтирования. При определенном уве личении объема альвеолярного мертво го пространства развивается тяжелое расстройство оксигенации. Блокада движения крови в системе легочной артерии (ТЭЛА) вызывает острую пере грузку правых отделов сердца, вплоть до остановки эффективной сердечной деятельности.
Растяжимость (податливость) легочной ткани
Растяжимость легких (см. также гла ву 8) является мерой эластической тяги, а также эластического сопротив ления легочной ткани, которое пре одолевается в процессе вдоха. Иначе говоря, растяжимость — это мера уп ругости легочной ткани, т. е. ее подат ливость. Математически растяжимость

Глава 1. Физиология и патофизиология внешнего дыхания 17
выражается в виде частного от изме нения объема легких и соответствую щего изменения внутрилегочного дав ления:
Растяжимость может быть измерена отдельно для легких и для грудной клетки. С клинической точки зрения (особенно во время ИВЛ) наибольший интерес представляет именно податли вость самой легочной ткани, отражаю щая степень рестриктивной легочной патологии. В современной литературе растяжимость легких принято обозна чать термином «комплайнс» (от англий ского слова «compliance», сокращен но — С). Истинную эластическую податливость легких отражает так назы ваемый «статический комплайнс» (Cst), измеренный в «статическом» состоянии легких, когда в конце вдоха временно прекращается движение потока дыха тельной смеси по крупным дыхатель ным путям.
Динамическая податливость (Cdyn), которую измеряют во время продолжа ющегося потока дыхательной смеси, зависит еще и от сопротивления дыха тельных путей, поэтому отражает рас тяжимость легких в меньшей степени:
Податливость легких снижается: |
I |
• с возрастом (у пациентов старше 50 |
|
лет); |
|
• в положении лежа (из-за давления |
|
органов брюшной полости на диаф |
|
рагму); |
|
• во время лапароскопических хирур |
|
гических вмешательств в связи с на |
|
ложением карбоксиперитонеума; |
|
• при острой рестриктивной патологии |
|
(острые полисегментарные пневмо |
|
нии, ОРДС, отек легких, ателектази- |
|
рование, аспирация и т. д.); |
|
• при хронической рестриктивной па |
|
тологии (хроническая пневмония, |
|
фиброз легких, коллагенозы, силико |
|
зы и т.д.); |
|
• при патологии органов, которые ок |
|
ружают легкие (пневмоили гидро |
|
торакс, высокое стояние купола ди |
|
афрагмы при парезе кишечника и |
|
т.д.). |
|
Чем ниже (хуже) податливость лег |
|
ких, тем большее эластическое сопро |
|
тивление легочной ткани надо преодо |
|
леть, чтобы достигнуть того же |
|
дыхательного объема, что и при нор |
|
мальной податливости. Следовательно, |
|
вслучае ухудшающейся растяжимости легких (снижении Cst) при достижении того же дыхательного объема давление
вдыхательных путях существенно воз
растает. Действительно, если VT остает
ся величиной постоянной, a Cst снижа ется, то APaw (Ppeak — PEEP) должно увеличиваться:
Внорме Cst составляет:
•у взрослых — 50~150 мл/мм вод.ст.,
•у детей 1 — 5 лет — 20—40 мл/мм вод.ст.,
•у младенцев до 1 года — 10—20 мл/ мм вод.ст.,
•у новорожденных — 3 — 5 мл/мм вод.ст.
VT = Cst x APaw
Данное положение очень важно для понимания: при объемной ИВЛ, когда принудительный дыхательный объем подается у больного с ухудшающейся податливостью легких (сниженном Cst), существенный рост пикового давления в дыхательных путях и внутрилегочно го давления значительно увеличивает
риск баротравмы.
&
IM
*У
