Отчеты по лабораторным работам - 2003 / 2 / фУРФУРОЛ
.DOCОтчет о лабораторной работе 2
Полуэмпирический расчет молекулы фурфурола методом MNDO (МПДП).
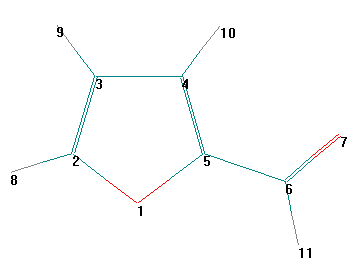
Общий вид молекулы Общий вид молекулы с нумерацией атомов
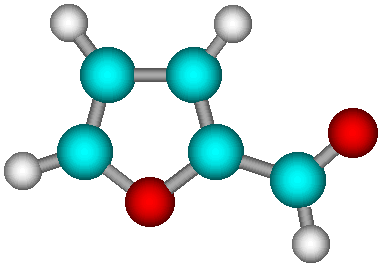
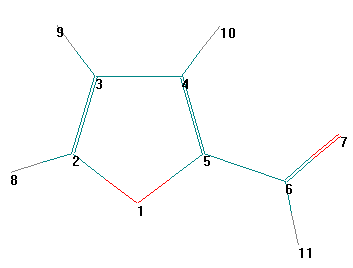
Цель работы. Знакомство с программным комплексом HyperChem 5.1. Проведение полуэмпирического квантовохимического расчета по методу MNDO с помощью программного комплекса HyperChem 5.1 и химическая интерпретация полученных результатов.
Интерпретация полученных результатов
1. Строение молекулы п-метоксифенола.
-
Длина связи
Данные ММ расчета, A
Данные MNDO расчета, A
O1-C2
1,372
1,359
C2-C3
1,335
1,394
C3-C4
1,444
1,436
C4-C5
1,335
1,400
C5-O1
1,372
1,371
C5-C6
1,46
1,481
C6=O7
1,22
1,220
C6-H11
1,08
1,109
C2-H8, C3-H9, C4-H10
1,08
1,081
Точность проведенного расчета составляет 0.02 Å
2. Построение диаграммы энергетических уровней. Графическое изображение ВЗМО и НВМО.
Энергия ВЗМО (№18) -9.5573 эВ ; Энергия НВМО (№19) –0,3697 эВ
Энергетическая диаграмма
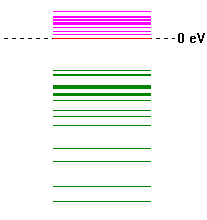
Вид ВЗМО Вид НВМО (HyperChem 6)
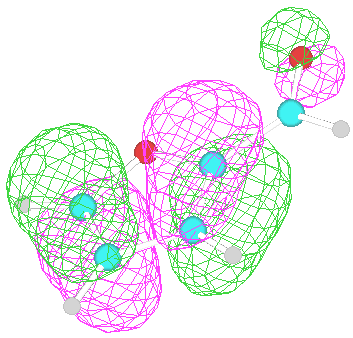
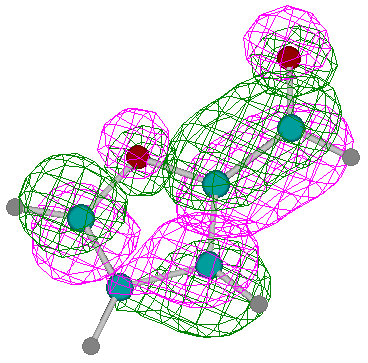
3. Вклады атомных орбиталей в ВЗМО и НВМО.
|
|
ВЗМО (HyperChem 6) |
НВМО (HyperChem 6) |
|
O1 C2 C3 C4 C5 C6 O7 |
0.00055 0.56884 0.38159 -0.32602 -0.61221 -0.01168 0.22265 |
-0.31319 0.44659 -0.12154 -0.45403 0.44376 0.39762 -0.35571 |
Положительные значения коэффициентов при атомных орбиталях дают связывающие вклады в МО, отрицательные значения - разрыхляющие вклады
4. Определение нуклеофильных и электрофильных свойств
Энергия НВМО отрицательна, следовательно фурфурол – электрофил
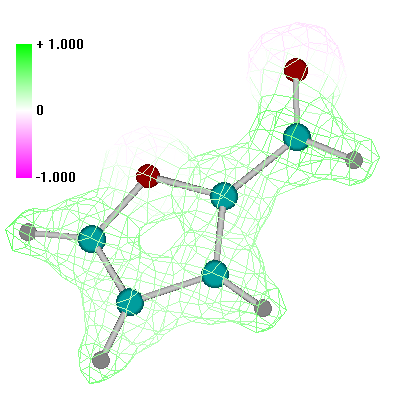
5. Построение распределения электростатического потенциала
|
|
Данный рисунок показывает области положительного и отрицательного распределения электростатического потенциала и визуализирует неподеленные электронные пары на атомах кислорода (красный цвет говорит об отрицательном значении потенциала). Это позволяет, например, сделать предположение о взаимодействии молекулы с растворителем. Очевидно, что катионы стремятся подойти к области отрицательного потенциала, анионы - к положительной области. |
6. Квантово-химическое обоснование модели резонансных структур.
В случае молекулы фурфурола представляет интерес сравнить распределение заряда с классическими представлениями
|
|
Атом Заряд O1 -0.111829 2C 0.029238 3C -0.155820 4C -0.029388 5C -0.128409 6C 0.332581 O7 -0.294948 8H 0.122578 9H 0.097905 10H 0.102387 11H 0.035706 |
Наблюдаемое распределение зарядов согласуется с существующим представлением, что фурфурол очень легко будет атаковаться электрофилами по карбонильному атому кислорода. Электрофильное замещение в кольцо будет проходить по α-атому углерода. |