Лабораторные работы / Лабораторная работа 2 - 2000 / Пример / p-metoxiphenol_report / Отчет
.docОтчет о лабораторной работе 2
Полуэмпирический расчет молекулы п-метоксифенола методом MNDO (МПДП).
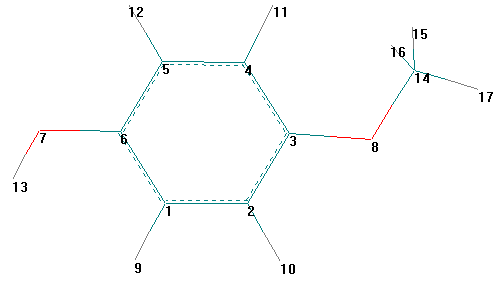
Общий вид молекулы Общий вид молекулы с нумерацией атомов
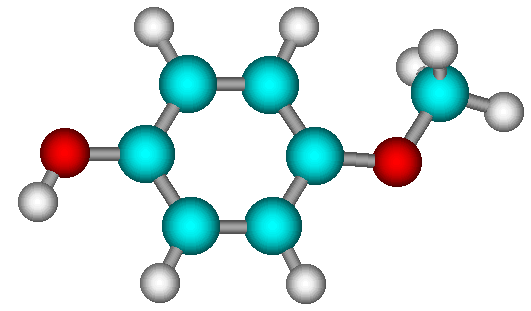
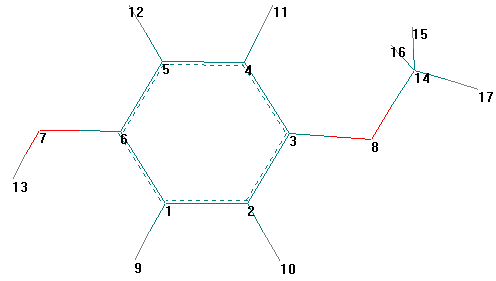
Цель работы. Знакомство с программным комплексом HyperChem 5.1. Проведение полуэмпирического квантовохимического расчета по методу MNDO с помощью программного комплекса HyperChem 5.1 и химическая интерпретация полученных результатов.
Интерпретация полученных результатов
1. Строение молекулы п-метоксифенола.
-
Длина связи
Данные ММ расчета
Данные MNDO расчета
Эксперимент (РСА)
C1 –C2
1.396
1.400
1.394
C1 –H9
1.103
1.091
1.084
C3 –O8
1.369
1.364
1.36
O7 –H13
0.942
0.947
0.97
O8 –C14
1.407
1.400
1.426
C14 – H15
1.114
1.117
1.096
Точность проведенного расчета составляет 0.02 Å
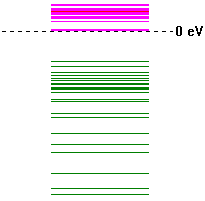
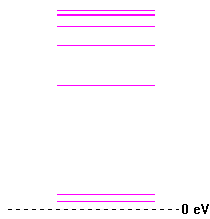
2. Построение диаграммы энергетических уровней. Графическое изображение ВЗМО и НВМО.
Энергия ВЗМО (№24) -8.478 эВ ; Энергия НВМО (№25) +0.145 эВ
Энергетическая диаграмма
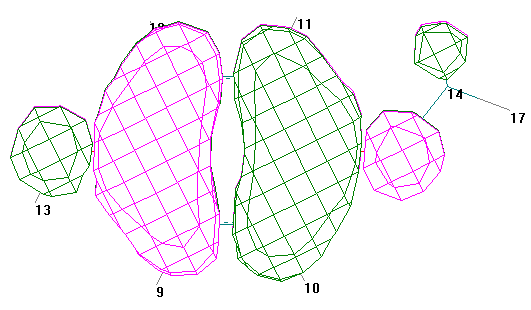
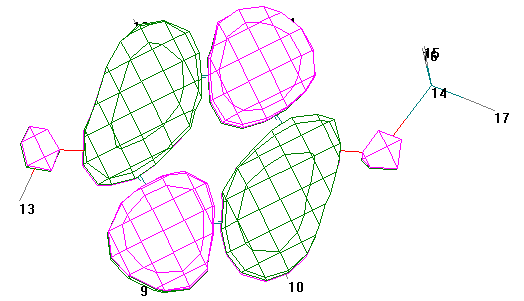
Вид ВЗМО Вид НВМО (HyperChem 6)
3. Вклады атомных орбиталей в ВЗМО и НВМО.
|
|
ВЗМО |
ВЗМО (HyperChem 6) |
НВМО |
НВМО (HyperChem 6) |
|
С1 Pz |
-0.24785 |
-0.24750 |
0.55814 |
-0.55808 |
|
C2 Pz |
0.31922 |
0.31952 |
-0.36640 |
0.36655 |
|
C3 Pz |
0.46873 |
0.46867 |
-0.23027 |
0.23019 |
|
C4 Pz |
0.25777 |
0.25785 |
0.55826 |
-0.55824 |
|
C5 Pz |
-0.32313 |
-0.32309 |
-0.35533 |
0.35554 |
|
C6 Pz |
-0.46792 |
-0.46786 |
-0.22846 |
0.22818 |
|
O7 Pz |
0.32531 |
0.32517 |
0.07288 |
-0.07278 |
|
O8 Pz |
-0.33180 |
-0.33195 |
0.07081 |
-0.07082 |
|
C14 Pz |
0.01447 |
0.01460 |
0.00997 |
-0.01014 |
Положительные значения коэффициентов при атомных орбиталях дают связывающие вклады в МО, отрицательные значения - разрыхляющие вклады
4. Определение нуклеофильных и электрофильных свойств
Энергия НВМО положительна, следовательно п-метоксифенол - нуклеофил
5. Построение распределения электростатического потенциала
|
|
Данный рисунок показывает области положительного и отрицательного распределения электростатического потенциала и визуализирует неподеленные электронные пары на атомах кислорода (красный цвет говорит об отрицательном значении потенциала). Это позволяет, например, сделать предположение о взаимодействии молекулы с растворителем. Очевидно, что катионы стремятся подойти к области отрицательного потенциала, анионы - к положительной области. |
6. Квантово-химическое обоснование модели резонансных структур.
В случае молекулы п-метоксифенола представляет интерес сравнить распределение заряда с классическими представлениями
|
|
C1 С2 С3 С4 С5 C6 O7 O8 C14 |
-0.112 -0.045 0.099 -0.101 -0.051 0.076 -0.249 -0.285 0.215 |
Наблюдаемое распределение зарядов согласуется с существующим представлением, что замещение бензола донорным заместителем приводит к возрастанию отрицательного заряда в орто- и пара- положениях, а замещение акцепторным заместителем приводит к возрастанию положительного заряда на атоме углерода, связанном с акцептором. Полученные результаты дают количественную оценку данного эффекта. |