Лабораторные работы / Лабораторные работы - 2003 / Отчёты / 2 / nitrobenzol_otchet
.docОтчет о лабораторной работе 2
Полуэмпирический расчет молекулы нитробензола
методом MNDO (МПДП).
О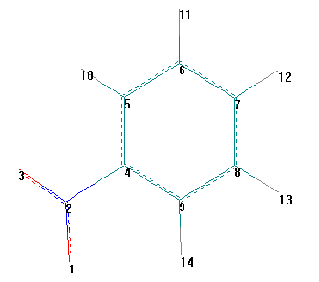
 бщий
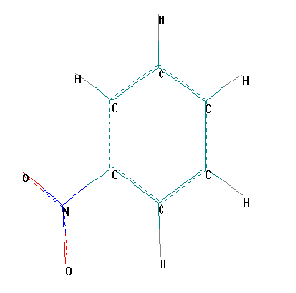
вид молекулы
Общий вид молекулы с нумерацией
бщий
вид молекулы
Общий вид молекулы с нумерацией
Цель работы. Знакомство с программным комплексом HyperChem 5.1. Проведение полуэмпирического квантовохимического расчета по методу MNDO с помощью программного комплекса HyperChem 5.1 и химическая интерпретация полученных результатов.
Интерпретация полученных результатов:
-
Строение молекулы нитробензола.
Длина связи Данные ММ расчета Данные MNDO расчета
N3-O1 1.22136 1.21201
N3-O2 1.22136 1.21201
N3-C4 1.47615 1.49935
C4-C5 1.39832 1.41558
C5-C6 1.39867 1.41558
C6-C7 1.39625 1.40648
C7-C8 1.39867 1.40608
C8-C9 1.39625 1.40648
C9-C4 1.39832 1.41558
C5-H10 1.10289 1.09154
C9-H14 1.10289 1.09154
C6-H11 1.10345 1.09079
C8-H13 1.10345 1.09079
C7-H12 1.10327 1.09085
Точность проведенного расчета составляет 0.02 Å
-
Построение диаграммы энергетических уровней. Графическое изображение ВЗМО и НВМО.
|
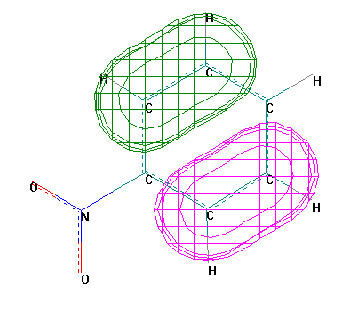
ВЗМО: |
|
|
|
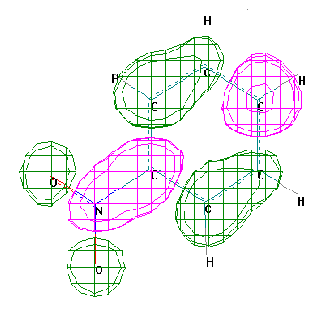
НСМО: |
|
Энергия ВЗМО (№23) –10.31эВ ; Энергия НВМО (№22) –1.22эВ
3. Вклады атомных орбиталей в ВЗМО и НВМО.
ВЗМО НВМО
Pz C 1 -0.00003 -0.55932
Pz C 2 0.00228 -0.31030
Pz C 3 0.00344 0.23148
Pz C 4 0.00002 0.59407
Pz C 5 -0.00343 0.23149
Pz C 6 -0.00232 -0.31030
Pz N 7 0.00002 -0.01794
Pz O 8 0.70712 -0.13074
Pz O 9 -0.70707 -0.13069
Положительные значения коэффициентов при атомных орбиталях дают связывающие вклады в МО, отрицательные значения - разрыхляющие вклады
4. Определение нуклеофильных и электрофильных свойств
Энергия НВМО отрицательна следовательно нитробензол - нуклеофил
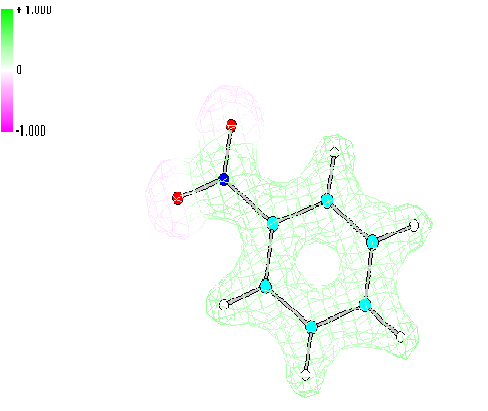
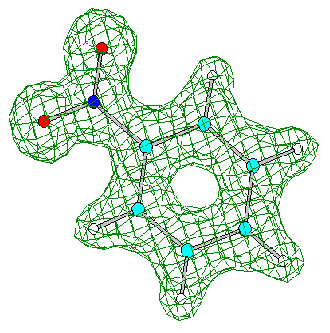
5. Построение распределения электростатического потенциала
Данный рисунок показывает области положительного и отрицательного распределения электростатического потенциала и визуализирует неподеленные электронные пары на атомах кислорода (красный цвет говорит об отрицательном значении потенциала). Это позволяет, например, сделать предположение о взаимодействии молекулы с растворителем. Очевидно, что катионы стремятся подойти к области отрицательного потенциала, анионы - к положительной области.
|
|
|
6. Квантово-химическое обоснование модели резонансных структур.
В случае молекулы нитробензола представляет интерес сравнить распределение заряда с классическими представлениями
|
атом заряд 1 -0.342091 2 0.486946 3 -0.342056 4 -0.084305 5 0.015605 6 -0.077538 7 -0.008995 8 -0.077538 9 0.015612 10 0.095087 11 0.075793 12 0.072596 13 0.075794 14 0.095088 |
|
Наблюдаемое распределение зарядов согласуется с существующим представлением, что замещение бензола акцепторными заместителями приводит к возрастанию отрицательного заряда в мета- положениях, а замещение акцепторным заместителем приводит к возрастанию положительного заряда на атоме углерода, связанном с акцептором.
Полученные результаты дают количественную оценку данного эффекта.