
Джефферсон - Сборник упражнений и задач - 2000 / Student Guide8
.pdf
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
55 |
Глава 8
Гликолиз, цикл лимонной кислоты, система транспорта электронов. Реакции этих метаболических путей.
Резюме главы
В этой главе описываются метаболические пути гликолиза, цикла лимонной кислоты и транспорта электронов. Приводятся детали химических ст руктур и названия ферментов. В дополнение к этому упоминаются пируваткарбо ксилазная реакция и кофермент биотин. Рассматриваются промежуточные продук ты в цепи транспорта электронов и в создании протонного градиента, а также механизм образования АТР. Для каждого восстановленного кофактора приводится расч ет образующихся эквивалентов АТР.
Цели урока
♦Различия в потребности и выделении энергии, в зависимости от того, что служит исходным материалом для гликолиза - гликоген или свободная глюкоза.
♦Названия и структуры каждого промежуточного продукта в путях гликолиза и цикла лимонной кислоты.
♦Названия ферментов, участвующих в гликолитическом пути и цикле лимонной кислоты.
♦Термины, применяемые к функциональным группам, претерпевающим превращения в процессе гликолиза и цикла трикарбоновых кислот.
♦Стадии гликолиза и цикла лимонной кислоты, в ходе которых образуются высокоэнергетические молекулы.
♦Пируваткарбоксилазная реакция, которая поддерживает запасы оксалоацетата на достаточном уровне и использует биотин.
♦Названия главных переносчиков электронов при образовании АТР из восстановленных кофакторов.
♦Значение кофермента Q (убихинона).
♦Роль протонного градиента через митохондриальную мембрану.
♦Транслоказный механизм переноса молекул ATP и ADP.

56 |
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
|
|
|
|
♦ |
Реакция, катализируемая АТР-синтазой. |
♦ Количество АТР, которое может |
образоваться из каждого восстановленного кофермента в ходе механизма транспорта электронов.
Прогулка по главе
Гликолиз
Гликолиз - (glyco = сахар) + (lysis = расщепление), - заключается в расщеплении шестиуглеродного сахара глюкозы на две трехуглеродные молекулы пирувата. Гликолиз может начинаться с глюкозы или с ее полимерной формы - гликогена. Более эффективен путь получения энергии из гликогена, поскольку для инициации процесса гликолиза, начинающегося с глюкозы, должна быть затрачена энергия одной молекулы АТР. Каждый из метаболитов цикла гликолиза имеет химическое название и многие из них часто приводятся в сокращенном виде. Каждый этап может быть описан согласно происходящему химическому превращению, причем каждую реакцию катализирует свой специфичный фермент.
Заполните следующее
Метаболит |
Сокращение |
Структура |
Реакция (название |
||
фермента) |
|||||
|
|
|
|
||
|
|
|
|
|
|
Глюкоза |
Обычно не |
? |
|
Фосфорилирование |
|
|
сокращается |
|
|
(гексокиназа) |
|
|
|
|
|
|
|
Глюкозо-6-фосфат |
G-6-P |
|
|
Перестройка(фосфогекзо- |
|
|
|
|
|
зоизомераза) |
|
|
|
|
|
|
|
Фруктозо-6-фосфат |
F-6-P |
CH2OH |
|
Фосфорилирование |
|
|
|
| |
|
(фосфофруктокиназа-1) |
|
|
|
C=O |
|
|
|
|
|
| |
|
|
|
|
|
CH2OH |
|
|
|
|
|
| |
|
|
|
|
|
CH2OH |
|
|
|
|
|
| |
|
|
|
|
|
CH2OH |
|
|
|
|
|
| |
|
|
|
|
|
CH OPÎ 2- |
|
||
|
|
2 |
3 |
|
|
Фруктозо-1,6-дифосфат |
F-1,6-P |
? |
|
Расщепление С-С связи |
|
|
|
|
|
(альдолаза) |
|
|
|
|
|
|
|
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
57 |
|||
|
|
|
|
|
|
|
|
|
|
Метаболит |
Сокращение |
Структура |
Реакция (название |
|
фермента) |
||||
|
|
|
||
|
|
|
|
|
Глицеральдегид-3-фосфат |
G-3-P |
? |
Окисление и |
|
|
|
|
фосфорилирование с Рi |
|
|
|
|
(глицеральдегид-3-фосфат- |
|
|
|
|
дегидрогеназа |
|
|
|
|
|
|
1,3-дифосфоглицерат |
1,3-ÄÔÃ |
? |
Субстратное |
|
|
|
|
фосфорилирование ADP |
|
|
|
|
(фосфоглицераткиназа; |
|
|
|
|
необратима) |
|
|
|
|
|
|
3-фосфоглицерат |
3-PG |
? |
Перестройка |
|
|
|
|
(фосфоглицератмутаза) |
|
|
|
|
|
|
2-фосфоглицерат |
2-PG |
? |
Дегидратация с |
|
|
|
|
образованием двойной |
|
|
|
|
связи (енолаза) |
|
|
|
|
|
|
Фосфоенолпируват |
PEP |
? |
Субстратное |
|
|
|
|
фосфорилирование ADP |
|
|
|
|
(пируваткиназа; |
|
|
|
|
необратима) |
|
|
|
|
|
|
Пируват |
Обычно не |
O O |
Декарбоксилирование и |
|
|
сокращается |
|| || |
сопряжение с коэнзимом А |
|
|
|
HO-C-C-CH3 |
(пируватдегидрогеназа) для |
|
|
|
|
поступления в цикл |
|
|
|
|
лимонной кислоты |
|
|
|
|
|
|
Последующие пояснения к отдельным реакциям помогут поня ть как функционирует цикл. Обратите внимание, что четыре последних этапа происходят дважды для каждой молекулы глюкозы, входящей в цикл. Глюкозо-6-фосфата изомеризуется во фруктозо-6-фосфат. Фруктозо-6-фосфат превращается в 1,6-дифосфат, так что оба трехуглеродных фрагмента, образующиеся в результате обратной реакции альдольной конденсации (см. заметки по органической химии), содержат фосфат. Специфические условия внутри клетки создают ситуацию, при которой отсутствует хорошая корреляция между величиной G0′ и реальной величиной G. Это обусловлено значительными отличиями истинных концентраций реагентов и продуктов от стандартных условий (концентрация 1 М), а также тем, что из одной исходной молекулы реагента образуются два продукта. Затем происходит реакция изомеризации и оба трехуглеродных фрагмента могут вступать в следующий этап, в котором альдегид окисляется до фосфорного эфира. Фосфат из молекулы 1,3- дифосфоглицерата с помощью фермента киназы переносится на ADP с образованием АТР. Эта реакция известна как реакция субстратного фосфорилирования. Продукт реакции - 3-фосфоглицерат, - далее превращается в пируват в результате реакций переноса фосфата с атома С-3 на С-2, удаления

58 |
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
|
|
молекулы воды при участии фермента енолазы и переноса фосфата на ADP (образуется АТР) под действием киназы (фермент назван так, как если бы он “работ ал” в обратном направлении). Из одной молекулы глюкозы образуется две молекулы АТР (из гликогена три). Образующийся NADH повторно окисляется либо аэробно в митохондриях, либо анаэробно. Аэробный процесс включает перенос электронов от NADH в митохондриях, либо через глицерофосфатный, либо малатаспартатный шунт, причем последний является энергетически более эффективным.
Заполните следующее
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
59 |
|
|
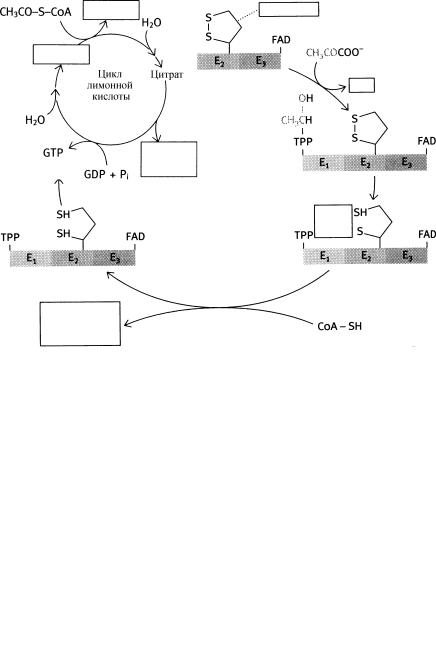
Образующиеся в процессе гликолиза две молекулы пирувата поступают в митохондрии, где в ходе реакции окислительного декарбоксилирования они превращаются в ацетил-СоА. В этом процессе, катализируемом мультиферментным комплексом, принимает участие ряд кофакторов, включая тиаминпирофосфат и липоевую кислоту.
Заполните следующее
Цикл лимонной кислоты
Двууглеродная ацетильная группа, присоединенная к коферменту А, поступает в цикл лимонной кислоты, чтобы превратиться в СО2 с образованием трех молекул NADH, одной FADH2, одной GTP и CoA-SH (не ацилированный кофактор). При этом происходит поглощение воды.
Заполните следующее
60 |
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
|
|
В этом цикле принимает участие девять химических соедине ний (считая промежуточный продукт цис-аконитат) и восемь ферментов. Образование оксалоацетата можно считать как исходной, так и конечной точкой цикла.
Заполните следующее
Метаболит |
Структура |
Реакция (название фермента) |
|
|
|
Ацетил-СоА |
O |
Kонденсация с оксалоацетатом с |
|
|| |
образованием цитрата (цитрат синтаза) |
|
CoA-S-C-CH3 |
|
|
|
|
Оксалоацетат |
? |
Kонденсация с ацетил-СоА с |
|
|
образованием цитрата (цитрат синтаза) |
|
|
|
Цитрат |
? |
Перегруппировка с образованием öèñ- |
|
|
аконитата (аконитаза) |
|
|
|
Öèñ-аконитат |
? |
Промежуточный продукт в |
|
|
перегруппировке цитрата с образованием |
|
|
изоцитрата |
|
|
|
Изоцитрат |
? |
Окислительное декарбоксилирование с |
|
|
образованиемa α-кетоглутарата |
|
|
(изоцитратдегидрогеназа) |
|
|
|
α-Kетоглутарат |
? |
Декарбоксилирование и конденсация с |
|
|
коферментом А с образованием |
|
|
сукцинил-СоА |
|
|
(α-кетоглутаратдегидрогеназа) |
|
|
|
Сукцинил-СоА |
? |
Гидролиз до сукцината (сукцинил-СоА- |
|
|
синтетаза; необратима) |
|
|
|
Сукцинат |
? |
Окисление до фумарата; |
|
|
алкена(сукцинатдегидрогеназа) |
|
|
|
Фумарат |
? |
Стереоспецифическая гидратирация |
|
|
(фумараза) |
|
|
|
Малат |
? |
Окисление: спирта до кетона |
|
|
(малатдегидрогеназа ) |
|
|
|
Оксалоацетат |
? |
Возврат к началу цикла |
|
|
|

Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
61 |
|
|
Двууглеродный остаток ацетата конденсируется с оксалоацетатом с образованием цитрата, который перегруппировывается в изоцитрат; последний декарбоксилируется с образованием α− кетоглутарата и одной молекулы NADH. Далее α−кетоглутарат подвергается декарбоксилированию и остающийся четырехуглеродный фрагмент переносится на СоА, при этом образуется одна молекула NADH. Образовавшийся сукцинил-СоА теряет молекулу СоА, при этом из GDP и Pi синтезируется GTP, а образующийся сукцинат дегидрируется с образованием фумарата и одной молекулы FADH2, а в ходе последующей гидратации фумарата образуется малат; окисление последнего приводит к образованию одной молекулы NADH и оксалоацетата, который может опять вступать в новый цикл.
Составляющие цикл промежуточные продукты не существуют изолированно от остальных путей метаболизма и участвуют в поддержании их равновесия (что описывается ниже). Одна из наиболее важных реакций обеспечения организма оксалоацетатом заключается в карбоксилировании пирувата, которое катализирует фермент пируваткарбоксилаза. Для его работы необходимы кофактор биотин, НСО3- è ÀÒÐ.
Заполните следующее
Транспорт электронов
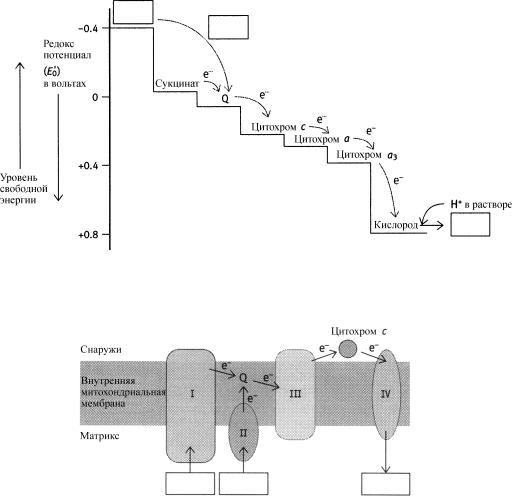
Заключительная стадия 3 «имеет» дело с образовавшимися молекулы NADH и FADH2 Она протекает во внутренней митохондриальной мембране или на ней. В полной последовательности реакций участвует ряд переносчиков электронов. Простетической группой цитохромов служит гем,
62 |
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
|
|
содержащий железо, которое переходит из двухвалентного (фeppо-форма, Fe2+) в трехвалентное состояние (ферри-форма, Fe3+)и наоборот. Существуют также негемовые переносчики электронов, содержащие железо-серные центры, принимающие электроны от FADH2 è FMNH2 и переносящие их на кофермент Q (убихинон), который хорошо растворим и подвижен в неполярной фазе мембраны, где в виде семихинонового свободного радикала и функционирует в качестве одноэлектронного переносчика. Есть также переносчики электронов, фиксированные в мембране. Электроны переносятся в энергетически выгодном направлении от молекул легко отдающих к молекулам легко их принимающим. Процесс может быть описан как транспорт электронов от молекул с низким окислительно-восстановительным потенциалом к молекулам с более высоким потенциалом. В этом процессе происходит высвобождение свободной энергии ( G < 0).
Заполните следующее
Заполните следующее
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
63 |
|
|
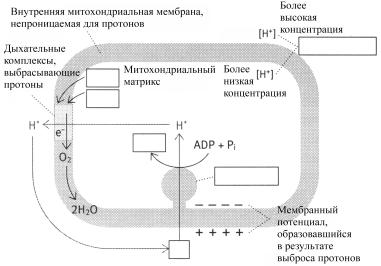
Переносимые электроны доставляются на кислород, в реакции которого с Н+, образуется вода. Сопряжение энергии, высвобождающейся при транспорт е электронов от одного переносчика к другому, с синтезом АТР достигается путем генерирования протонного градиента: протоны (Н+) перекачиваются на наружную сторону мембраны, а затем через эту мембрану возвращаются назад, регулируя АТР-синтазный комплекс, который и синтезирует АТР из ADP + Pi; этот процесс получил название хемиосмотического механизма. Механизм функционирования протонного градиента полностью не ясен, однако то, что известно о роли, выполняемой коферментом Q в комплексе III позволяет предположить, что кофермент Q превращается в QH2, принимая протоны из матрикса (изнутри) внутренней митохондриальной мембраны, а когда QH2 вновь возвращается в исходное состояние Q, протоны высвобождаются на наружной стороне мембраны. Таким путем создается градиент.
Заполните следующее
Синтез АТР связан с конформационными изменениями АТР-синтазы, вызываемыми обратным трансмембранным потоком протонов в матрикс. Хорошей аналогией является представление об АТР-синтазе как о протонном насосе, действующим наоборот; вместо использования АТР для перекачки протонов, он способен перекачивать протоны и синтезировать АТР. Механизм транспорта, известный как АТР-ADP транслоказа, осуществляет перенос этих несущих энергию соединений из митохондрий, где синтезируется АТР, в другие компартаменты клетки, где АТР используется. Значительное количество энергии для этого процесса также сопряжено с перемещением протонов через мембрану. Для синтеза одной молекулы АТР АТР-синтаза перекачивает три протона и один дополнительный протон для транслокации ADP, ATP и фосфата. Таким образом, для синтеза одной молекулы АТР необходимы четыре протона. Количество протонов, перекачиваемых в ответ на NADH или FADH2, передающих свои электроны на кислород, зависит от ряда факторов. Для NADH
64 |
Глава 8: Гликолиз, цикл лимонной кислоты, система транспорта электронов |
|
|
это число может составлять 2,5 или 1,5, а для FADH2 - 1,5. Начиная со свободной глюкозы (а не с гликогена) суммарный выход АТР составляет либо 30, либо 32 молекулы, в зависимости от того, какой челночный механизм используется для транспорта цитоплазматического NADH в митохондрии. В клетках E.coli отсутствуют митохондрии и для функционирования сходного метаболического пути используется клеточная мембрана. Существуют и другие пути использования энергии, запасаемой при работе протонного градиента, например, образование тепла клетками бурой жировой ткани у новорожденных детей, некоторые типы перекачки ионов или вращение жгутиков у ряда бактерий.
Обзор вопросов в конце главы 8
∙Фосфогексозоизомераза осуществляет перенос карбонильной группы от атома углерода С-1 глюкозы на С-2 с образованием фруктозы. Следующую за ней реакция катализирует альдолаза, для которой необходим кетонный карбонил.
∙Субстратное фосфорилирование означает, что в ходе реакции качестве источника фосфата
используется фосфат из одного из субстратов (а не Pi ). Существует несколько реакций субстратного фосфорилирования: две в гликолизе и одна в цикле лимонной кислоты.
∙В соответствие с правилами номенклатуры фермент пируват киназа получил свое название по реакции, обратной той, что происходит в организме. Энергетика системы направляет реакцию в сторону образования АТР, поскольку фосфоенолпируват является более “высокоэнергетическим” интермедиатом, по сравнению с АТР.
∙При гликолизе, начинающемся с гликогена, образуется больше АТР (3 молекулы), чем при использовании глюкозы (2 молекулы), так как на активацию глюкозы необходимо затратить одну молекулу АТР, тогда как неорганический фосфат присоединяется к высвобождаемому из гликогена мономеру глюкозы в реакции, не требующей АТР.
∙Существует два мембранных челночных пути для NADH, причем малат-аспартатный шунт более эффективен, чем глицерофосфатный. Отчасти различия в количестве энергии, генерируемой
этими восстановленными кофакторами, объясняются тем, по какому пути NADH и FADH2 передаются по цепи транспорта электронов.
∙“Пропущенная молекула” Н2О в цикле лимонной кислоты образуется в реакции
GDP + Pi → GTP + Í2Î,
которая часто записывается без упоминания воды.
∙При окислении изоцитрата образуется α−кетокислота с карбонильными остатками у соседних
атомов углерода. Такое соединение может затем терять СО2, образуя при этом в одну стадию тиоэфир с коферментом А..
