
Джефферсон - Сборник упражнений и задач - 2000 / Appendix
.pdfПриложение: Ответы на дополнительные вопросы к главам |
253 |
Приложение
Ответы на дополнительные вопросы к главам
Глава 1
1.Горение углеводородов и разбавление концентрированных кислот и оснований.
2.(а) Энтальпия является функцией термодинамического состояния, которая описывает
содержание тепла в системе.
(б) Энтропия является мерой хаотичности или неупорядоченности системы.
(в) Свободная энергия определяет то количество доступной для совершения работы энергии, которое высвобождается в ходе химической реакции.
3.log 1 равен 0 и эта ситуация означает, что нет разницы в энергии между исходными реагентами
èпродуктами.
4. Используя уравнение G0′ = -RT lnK , и решая для K = exp{-( G0′ / RT)},
K = e{11 400(8,3)(310)} = e(4,43) = 84,0,
Это очень большое число, которое означает, что равновесие сильно сдвинуто вправо, поскольку значение G0′ отрицательно.
5.В модели «ключ-замок» субстрат комплементарен активному центру фермента. Согласно модели индуцированного соответствия, активный центр фермента изменяет свою конформацию, связываясь с переходным состоянием субстрата, поэтому последний должен сначала принять форму этого переходного состояния.
6.HPO42-.
7.[H+] = 10-10.
8.pH = -log(0,025) = 1,6.
9.Карбоксильная группа муравьиной кислоты.
10.Кривая должна начинаться при щелочном значении рН, снижаться по мере добавления кислоты, достигая плато при значениях рН около 4,76. Далее рН будет снижаться до достижения максимального значения рН около 1.
11.Между значениями рН = 8 и рН = 10.
12.ðÍ = ðKa + log([соль/кислота]) = 3,1 + log(1/4) = 2,5.
13.Буфер представляет собой смесь слабой кислоты и ее сопряженного основания, способную поглощать или освобождать Н+, необходимые для поддержания рН раствора.
254 |
Приложение: Ответы на дополнительные вопросы к главам |
|
|
14.Притяжение зарядов ионов должно замениться ион-дипольным взаимодействием растворителя с ионами.
15.Н-связи образуются с между атомами Н у атома азота и кислорода карбонильной группы. Они не образуются с атомами водорода у атомов углерода.
16.Вода полярна, а масло неполярно. Не существует сил притяжения между молекулами двух типов, которые могут преодолеть силы притяжения между молекулами одного и того же типа.
Глава 2
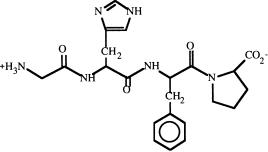
1.
2.Третичная структура представляет собой полную нативную структуру для белка с единственной полипептидной цепью. Третичная структура включает в себя вторичную.
3.Пролин вызывает излом структуры спирали.
4.Цистеин.
5.Сахар.
6.Это структурные белки. Коллаген является прочной молекулой фибриллярного типа, а эластин представляет собой эластичный неструктурированный белок. Коллаген обнаружен в мышцах, а эластин является компонентом кровеносных сосудов.
Глава 3
1.Кардиолипин представляет собой симметричную молекулу, в которой глицерин связан с двумя остатками фосфатидной кислоты. Каждая молекула фосфатидной кислоты содержит две цепочки жирной кислоты, остов глицерина и фосфат.
2.Амидная связь.
3.По количеству остатков сахаров и присутствию фосфата.
4.Снижение температуры делает мембраны более ригидными. У рыб, обитающих в холодной воде, состав мембран характеризуется высоким содержанием ненасыщенных жирных кислот.
5.Существует шесть возможных структур ТАГ. Назвав одну из жирных кислот “А”, а другую “В”, возможны следующие варианты: ААА, ААВ, АВА, ВВА, ВАВ, ВВВ.
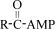
Приложение: Ответы на дополнительные вопросы к главам |
255 |
|
|
6. Òðè èîíà Na+ поступают в канал изнутри, и АТР фосфорилирует белки канала. В то время как три иона Na+ выкачиваются из клетки через канал в окружающую среду, два иона К+ поступают в канал снаружи. Фосфат удаляется из белка канала и два иона К+ поступают внутрь клетки.
Глава 4
1.ÑÎ2 + Í2Î Í2ÑÎ3 Í2ÑÎ3 ÍÑÎ3- + Í+ ÍÑÎ3- ÑÎ32- + Í+.
2.рН поддерживается в результате функционирования ионных каналов, действия СО2 и карбоангидразы.
3.Соединение просто не превращается в заметных количествах и выводится из организма в неизмененном виде.
4.Гликоген - полисахарид, запасаемый организмом для выработки энергии, а целлюлоза - структурный компонентом древесины.
5.Желчные кислоты содержат как полярные, так и неполярные функциональные группы.
6.Как и у клеточной мембраны хиломикроны имеют снаружи фосфолипидную полярную голову, но структуры хиломикронов обладают, в отличие от клетки, гидрофобным содержимым.
7.Длинноцепочечные жирные кислоты.
8.
Глава 5
1.
Тип ткани |
Обмен энергии |
|
|
Печень |
Запасы гликогена |
|
|
Мышца |
Очень малые запасы; используются сахара или жиры |
|
|
Головной мозг |
Очень малые запасы; используется только сахара (глюкоза) |
|
|
Жировая ткань |
Запасы жиров |
|
|
Эритроциты |
Очень малые запасы; используются только сахара (глюкоза) |
|
|
2.Эти соединения не являются “телами” и не все из них представляют собой кетоны.
3.Электроны удаляются из пищевых молекул и акцептируются кислородом с образованием воды.
4.Холодовой стресс. У новорожденных детей и у животных, находящихся в зимней спячке есть клетки (бурой жировой ткани), специализирующиеся на выработке тепла.
5.Триацилглицеринами (ТАГ).
256 |
Приложение: Ответы на дополнительные вопросы к главам |
|
|
6.Они разрушаются.
7.Глюкагон является гормоном, а гликоген - полимерной формой хранения глюкозы.
8.Адреналин высвобождается надпочечниками, печень освобождает глюкозу в кровь, жировая ткань высвобождает жирные кислоты, а скелетные мышцы начинают расщеплять запасенный гликоген.
Глава 6
1.Сахара, отличные от глюкозы, как правило, превращаются в метаболиты, которые поступают либо в гликолиз, либо - в цикл лимонной кислоты.
2.Желчные кислоты, стероидные гормоны, эфиры холестерина.
3.Òðè.
4.Этот белок переносит с кровью липиды, главным образом, жирные кислоты.
5.Превращение одного изомера в другой.
6.Глюкоза является шестиуглеродным сахаром и поэтому может быть отнесена к гексозам.
7.Глюкагон активирует расщепление гликогена, а инсулин его ингибирует. Инсулин активирует синтез гликогена, а глюкагон его ингибирует.
8.В стереохимии ОН-группы у С-4 атома углерода.
9.Соединения, отличающиеся только по стереохимической конфигурации одного центра.
10.Он не метаболизируется с образованием энергии.
11.Хиломикроны высвобождаются через лимфатическую систему из тонкого кишечника в кровь. Они доставляют жирные кислоты в клетки и превращаются в остатки хиломикронов. Эти остатки поглощаются затем печенью.
12.Из рисунка в учебнике диаметр хиломикронов, ЛПОНП, ЛПНП, и ЛПВП составляет соответственно 1500, 500, 250 и 50 ангстрем.
13.Хиломикроны > ЛПОНП > ЛППП > ЛПНП > ЛПВП.
14.Адреналин и глюкагон.
Глава 7
1.Поскольку свободная энергия освобождается в ходе реакции, ее содержание в продуктах меньше, чем в исходных реагентах.
2.-2820 êÄæ . ìîëü-1.
3.1/2Î2 + 2Í+ + 2å- → Í2Î.
4.Добавьте два Н+ к левой части каждого уравнения реакции.
5.Аэробный означает в присутствии О2, а анаэробный - в его отсутствии.
6.Это двойная мембрана.
7.При анаэробных условиях. Примерами являются мышцы и ферментация дрожжей.
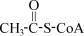
Приложение: Ответы на дополнительные вопросы к главам |
257 |
|
|
8.
9.Пируватдегидрогеназный комплекс.
10.Ацетил-СоА, NADH, Í+ è ÑÎ2.
11.Электроны уходят через проводник, соединяющий два электрода, отрицательно заряженные анионы переносятся через солевой мостик для сохранения электронейтральности.
12.G0′ = -nF Å0′ = -2 x (96,5 êÄæ . Â-1 . ìîëü-1) x (0,25 Â) = -48,25 êÄæ . ìîëü-1.
Да, эта реакция благоприятна, поскольку G0′ < 0.
13. Реакция, о которой идет речь в вопросе представляет собой сумму двух следующих полуреакций.
2Fe2+ → 2e- + 2Fe3+.
1/2O2 + 2H+ + 2e- → H2O.
Поскольку Fe2+ окисляется (теряя электроны), то знак Е0′ должен быть изменен перед двумя добавляемыми значениями; поэтому Е0′ = (-0,77 В) + (0,82 В) = 0,05 В. Так как потенциал положителен и G0′ = -nF Å0′, то это означает, что G0′ è E0′ будут иметь противоположные знаки и значение G0′ будет отрицательным, а реакция будет благоприятной. Таким образом, Fe2+ будет окисляться до Fe3+ в присутствии O2.
14.В этом случае при истощении запасов глюкозы для поддержания сахара крови мы могли бы использовать жиры для получения глюкозы.
15.Углеродный скелет различных аминокислот может превращаться в такие соединения, как пируват, ацетил-СоА и некоторые метаболиты лимонной кислоты.
16.(а) Гликолиз происходит в цитоплазме.
(б) Цикл лимонной кислоты имеет место в митохондриальном матриксе.
(в) Транспорт электронов осуществляется в митохондриальной мембране.
Глава 8
1.Пируватдегидрогеназный комплекс.
2.Цикл Кребса и цикл трикарбоновых кислот (ЦТК).
3.Спиральный, поскольку осуществляется одна и та же последовательность реакций при отщеплении от различных молекул двух атомов углерода.
4.Глицерофосфатдегидрогеназа, 3-фосфоглицераткиназа и пируваткиназа.
5.Изоцитратдегидрогеназа, α-кетоглутаратдегидрогеназа, сукцинатдегидрогеназа и малатдегидрогеназа.
6.При транспорте электронов протоны перекачиваются через внутреннюю митохондриальную мембрану (изнутри снаружу) и среда внутри становится менее кислой (рН внутри выше).
258 |
Приложение: Ответы на дополнительные вопросы к главам |
|
|
7.Различия в положении карбонильной группы: в глюкозе у атома углерода С-1, а во фруктозе
óатома углерода Ñ-2.
8.Этот фермент превращает 3-фосфоглицерат в 2-фосфоглицерат, так что оба трехуглеродных фрагмента из шестиуглеродной молекулы глюкозы могут превращаться одним и тем же путем.
9.Гексокиназа, фосфофруктокиназа, 3-фосфоглицераткиназа и пируваткиназа. Общим у всех является перенос высокоэнергетического фосфата.
10.Цитоплазматическая форма использует NAD+/NADH, а митохондриальная - FAD/FADH2.
11.Внешняя мембрана проницаема для большинства метаболитов.
12.Окисленная форма имеет дисульфидную связь, а восстановленная форма содержит две SHгруппы.
13.α-Кетоглутарат сходен по структуре с глутаматом.
14.Это карбонильный атом углерода.
15.При окислении изоцитрата α-кетоглутарата. Обе стадии катализируют ферменты дегидрогеназы: изоцитратдегидрогеназа и α-кетоглутаратдегидрогеназа.
16.Òðè.
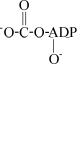
17.
èëè
18.На стадии транспорта электронов.
19.Fe3+.
20.Наличие неспаренного электрона. Большинство электронов либо спарены в составе химических связей (два электрона на связь), либо существуют в виде одиночных пары (группы из двух).
21.Восстановительный потенциал отражает способность соединения отдавать электрон, так что в случае присоединения электронов другим соединением оно будет восстанавливаться.
22.Транспорт электронов по электронтранспортной цепи, сопряженный с трансмембранным
переносом протонов. Поток электронов от NADH и FADH2 ê Î2 вызывает перекачивание протонов из матрикса через внутреннюю митохондриальной мембрану наружу; обратный поток протонов в матрикс управляет синтезом АТР из ADP и Pi.
23.Образование тепла у новорожденных детей и передвижение при помощи вращения жгутика у бактерий.
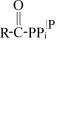
Приложение: Ответы на дополнительные вопросы к главам |
259 |
|
|
Глава 9
1. Поскольку жир находится в более высоко восстановленном состоянии, по сравнению с углеводами, то большее число электронов может быть извлечено при его окислении и пройти через электронтранспортную цепь для синтеза АТР.
2.
Ýòàï |
Для каждого цикла |
Пример для С22 жирной |
|||
|
|
|
кислоты |
|
|
|
|
|
|
|
|
á-окисление |
1 |
NADH |
1 x 10 = 10 |
NADH |
|
|
1 |
FADH2 |
1 x 10 |
= 10 |
FADH2 |
|
|
|
|||
Цикл лимонной кислоты |
3 NADH |
3 x 11 = 33 NADH |
|||
|
1 |
FADH2 |
1 x 11 |
= 11 |
FADH2 |
|
1 |
GTP |
1 x 11 |
= 11 |
GTP |
|
|
|
|
|
|
Транспорт электронов |
|
|
Всего: |
|
|
|
2,5 ATP/NADH(ìàêñ) |
43 x 2,5 = 107,5 ATP |
|||
|
1,5 ATP/1 FADH2 |
22 x 1,5 = 33,0 ATP |
|||
|
1 |
ATP/GTP |
11 x 1,0 = 11,0 ATP |
||
|
|
|
|||
Цена активации жирной |
-2 ATP |
Всего = 151,5 - 2 = 149,5 АТР |
|||
кислоты |
|
|
|
|
|
|
|
|
|
|
|
3.Жирные кислоты взаимодействуют с АТР и коэнзимом А с образованием àöèë-ÑîÀ, ÀÌÐ è PPi.
4.Жирные кислоты транспортируются из цитозоля в митохондриальный матрикс для
последующего окисления.
5.Гликолиз (через пируват), цикл лимонной кислоты и β-окисление жиров связаны между собой посредством ацетил-СоА.
6.Поскольку эта молекула не запасается, а кофакторы СоА необходимы для протекания других реакций, то ацетильная группа превращается в кетоновые тела.
7.
èëè
8.Она участвует в транспорте жирных кислот через внутреннюю мембрану митохондрий.
9.Жирнокислотная ацильная группа.
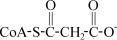
260 |
Приложение: Ответы на дополнительные вопросы к главам |
|
|
10.3-Гидрокси-3-метилглутарил-СоА; он имеет сходное с глутаматом строение.
11.Кобальт.
12.Он входит в цикл лимонной кислоты.
13.FADH2, образующийся при окислении молекул насыщенных ацил-СоА, прямо окисляется О2
ñобразованием Н2Î2
Глава 10
1. Такая организация этих путей, которая обеспечивает их термодинамически благоприятное протекание; поэтому такие пути регулируются раздельно.
2.
3.Ферменты цикла лимонной кислоты, включающие дегидрогеназу/гидратазу/дегидрогеназу, сходны; в синтезе жирных кислот имеет место обратное превращение: кетон → спирт → алкен →насыщенное (СН2) соединение.
4.Добавляются два атома углерода, а третий теряется в виде СО2.
5.Линолевая и линоленовая кислоты.
6.Простагландины, тромбоксаны и лейкотриены.
7.(а) Ингибирование синтеза фермента ГМГ-CoA-редуктазы на генном уровне.
(б) Деструкция фермента ГМГ-CoA-редуктазы.
(в) Инактивация фермента при фосфорилировании.
8.Ловастатин и симвастатин ингибируют фермент ГМГ-CoA- редуктазу.
9.ГМГ-CoA-редуктаза катализирует восстановление ГМГ-CoA с образованием мевалоната. Этот фермент является ключевым в регуляции синтеза холестерина.
10.Аденин, рибоза, фосфат, пантотенат и -NHCH2CH2SH.
11.По третьему углеродному атому рибозы, соединенному с остатком аденина.
Глава 11
1.(а) Фосфорилирование глюкозы гексокиназой.
(б) Фосфорилирование фруктозо-6-фосфата фосфофруктокиназой.
(в) Превращение фосфоенолпирувата в пируват.
2.Мышечный белок.
3.Лактат превращается в глюкозу в ходе цикла Кори в печени.
4.Чтобы обеспечить образование фосфоенолпирувата в ходе обходных реакций, катализируемых пируваткарбоксилазой и ФЕП-карбоксикиназой.
5.Аланин содержит α-аминогруппу, а пируват - α-кетогруппу.
Приложение: Ответы на дополнительные вопросы к главам |
261 |
|
|
6. На уровне изоцитрата, который под действием фермента изоцитратлиазы превращается в глиоксилат и сукцинат, и не метаболизируется до α-кетоглутарата и СО2.
Глава 12
1.Поскольку активность такового фермента более чувствительна к изменению концентрации субстрата.
2.Фосфаты - полярные соединения; присоединение фосфата к аминокислотным остаткам, например, серину, вызовет изменение формы молекулы белка, позволяющее этой полярной группе взаимодействовать с другими полярными группами, избегая взаимодействия с неполярными группировками данной белковой молекулы.
3.Активация блокируется или предотвращается.
4.Печень, мышцы и жировая ткань.
5.Фосфоролиз - расщепление гликогена при участии неорганического фосфата. Фосфорилирование - переносе фосфатной группы с одной молекулы (обычно АТР) на другую. молекулу.
6.АМР аллостерически активирует фосфорилазу b. Превращение гликогенфосфорилазы b в “а”-форму происходит в ответ на сАМР, который является вторичным мессенджером для внешней системы регуляции, стимулируемой адреналином.
7.Белковый ингибитор фосфатазы пролонгирует эффект фосфорилирования на активность гликогенфосфорилазы а и гликогенсинтазы. Этот белок активируется сАМР, что приводит к
торможению деактивации гликогенфосфорилазы а. Данный белок инактивируется под действием инсулина, который в свою очередь активирует гликогенсинтазу. Таким образом, совместное действие инсулина и сАМР запускает механизмы запасания глюкозы в виде гликогена и обратное расщепление гликогена до его мономерных единиц.
262 |
|
Приложение: Ответы на дополнительные вопросы к главам |
||
|
|
|
|
|
8. |
|
|
|
|
|
|
|
|
|
|
Эффектор |
Механизм |
Суммарный эффект |
|
|
|
|
|
|
|
В мышечной ткани |
|
|
|
|
|
|
|
|
|
Адреналин и |
Стимулируют расщепление |
Глюкоза для образования |
|
|
глюкагон через |
гликогена |
энергии |
|
|
ñÀÌÐ |
|
|
|
Ингибируют синтез гликогена |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Стимулируют образование |
Глюкоза для образования |
|
|
|
глюкозы из G-6-P |
энергии |
|
|
|
|
|
|
|
|
|
Очень незначительный |
|
|
|
|
синтез G-6-P из пирувата |
|
|
|
|
|
|
|
В ткани печени |
|
|
|
|
|
|
|
|
|
Адреналин и |
Ингибируют синтез гликогена |
|
|
|
глюкагон через |
|
|
|
|
Стимулируют образование |
Синтез глюкозы |
|
|
|
ñÀÌÐ |
|
||
|
|
глюкозы из G-6-P |
|
|
|
|
|
|
|
|
|
Стимулируют синтез G-6-P из |
|
|
|
|
пирувата |
|
|
|
|
|
|
|
|
|
Ингибируют пируваткиназу |
Гликолиз подавляется |
|
|
|
|
|
|
|
Только глюкагон |
|
Ингибирование синтеза |
|
|
|
|
жиров |
|
|
|
|
|
|
|
Инсулин |
Активирует гликогенсинтазу |
Синтез гликогена |
|
|
|
|
|
|
|
В жировой ткани |
|
|
|
|
|
|
|
|
|
Адреналин и |
Предотвращают |
Ингибирование синтеза |
|
|
глюкагон через |
дефосфорилирование ацетил- |
жиров |
|
|
ñÀÌÐ |
СоА-карбоксилазы, |
|
|
|
|
приводящее к ее инактивации |
|
|
|
|
|
|
|
|
|
Активируют протеинкиназу, |
TAГ расщепляется до |
|
|
|
которая фосфорилирует |
свободных жирных кислот, |
|
|
|
гормон-чувствительную |
используемых для получения |
|
|
|
липазу, активируя ее |
энергии |
|
|
|
|
|
|
|
Инсулин |
Активирует ацетил-СоА |
Синтез жиров для запасания |
|
|
|
карбоксилазу |
энерги |
|
|
|
|
|
|
