
Лекция 18.Гетерофункциональные соед.05.12.10
.doc|
Лекция 18 |
Гетерофункциональные
природные соединения
Большинство природных соединений являются гетерофункциональными, т.е. содержат различные функциональные группы. Наиболее часто встречающиеся и наиболее важные из них: СООН, ОН, С=О, NH2.
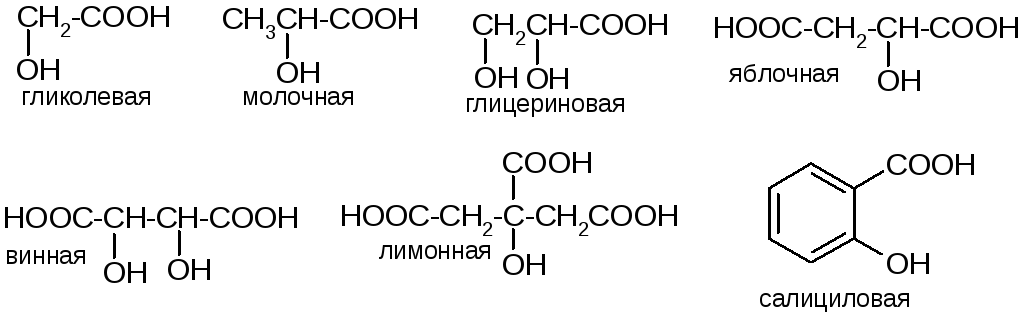
Оксикислоты
Содержат карбоксильные и гидроксильные группы:
Способы получения
1. Гидролиз галогенпроизводных кислот (для всех кроме β-оксикислот):
![]()
2. Гидратация α,β-непредельных кислот (для β-оксикислот):
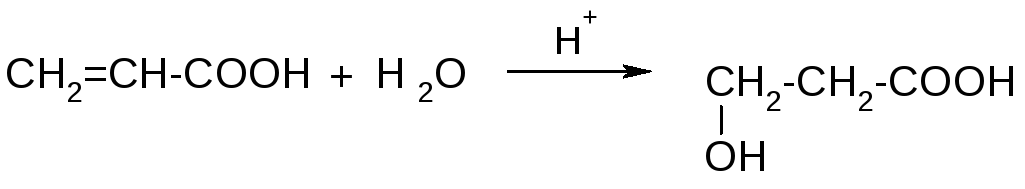
3. Циангидринный способ (для α-оксикислот):
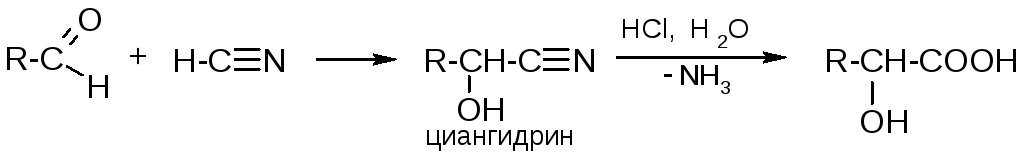
Химические свойства
Оксикислоты объединяют в себе свойства карбоновых кислот и спиртов (см.)
1) Кислотность
Кислотность СООН-группы увеличивается за счет электроноакцепторного влияния ОН-группы, особенно сильно у α-оксикислот:
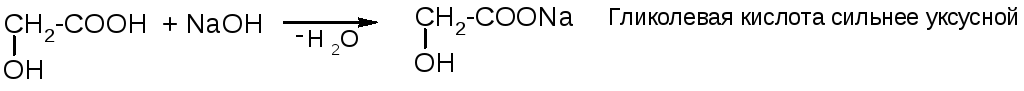
Особые свойства оксикислот связаны с взаимодействием СООН- и ОН-групп.
2) Образование лактидов (α-оксикислоты):
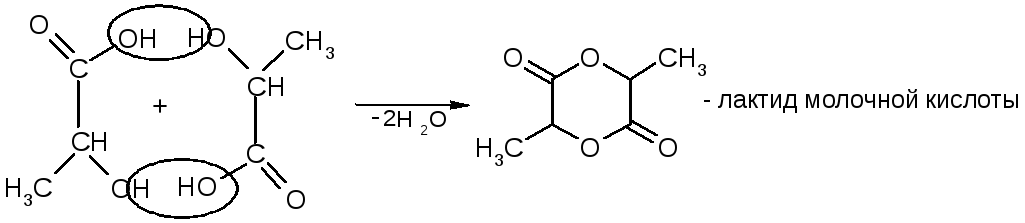
3) Дегидратация (β-оксикислоты):
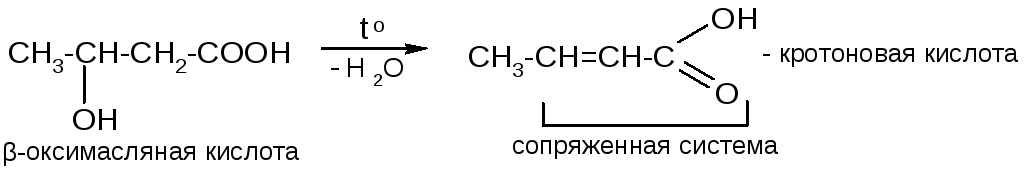
4) Образование лактонов (γ- и δ-оксикислоты):
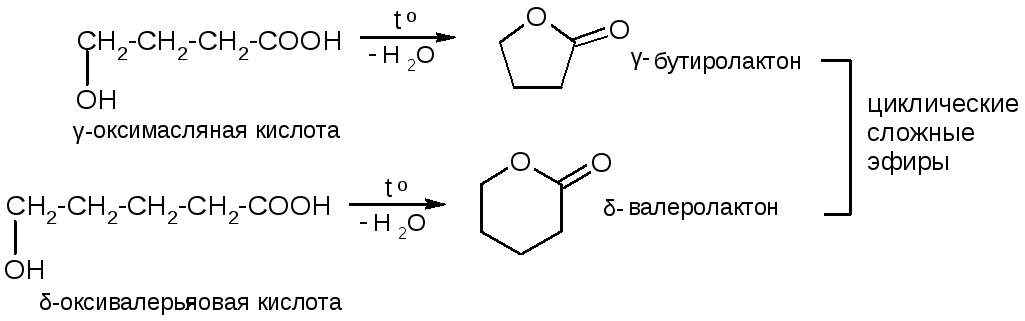
Отдельные представители оксикислот
Молочная кислота. Впервые выделена К Шееле из кислого молока (1780 г.). Широко распространена как продукт биохимического брожения (гликолиз), является одним из ключевых метаболитов в обмене углеводов.
Лимонная кислота. Содержится в лимонах (6-8% сухой массы), в листьях махорки (откуда раньше получалась промышленным способом). Сейчас основной способ её получения – биохимическое лимоннокислое брожение под действием определенного штамма грибов. В организме является одним из ключевых метаболитов энергетического обмена в цикле трикарбоновых кислот (цикл Кребса).
Салициловая кислота. Выделена из коры ивы (Salix). Обладает антисептическими свойствами и применяется в медицине, а также как консервант пищевых продуктов. В медицине и фармации в качестве лекарственных средств широко применяются производные салициловой кислоты по обеим функциональным группам:
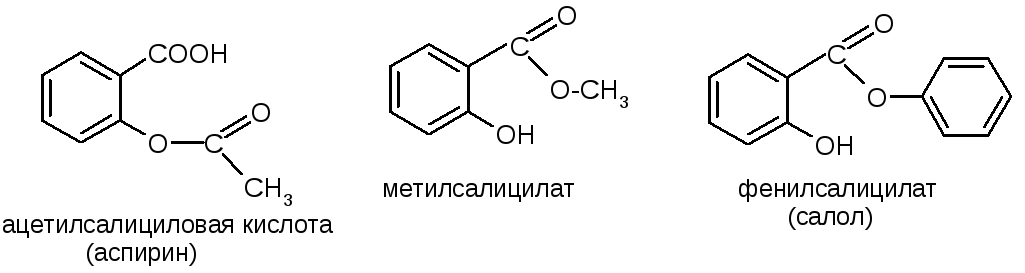
Оксокислоты
Содержат СООН и С=О- группы:
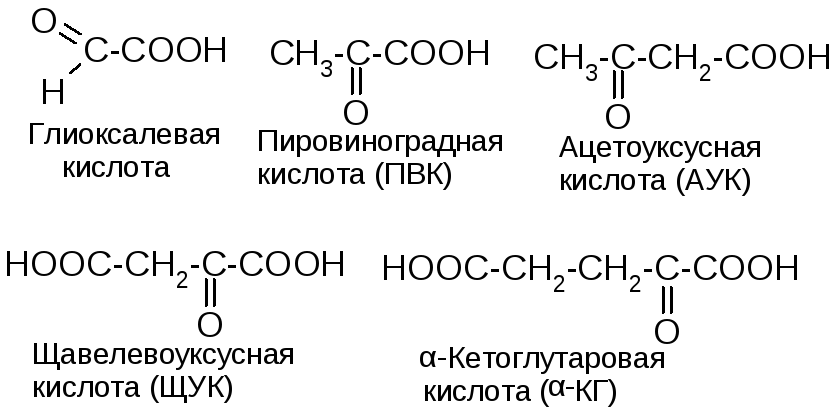
Способы получения
В основном способы получения оксокислот сводятся к образованию СООН и С=О-групп (см. способы подучния карбоновых кислот, альдегидов и кетонов).
1) Гидролиз α-оксонитрилов:
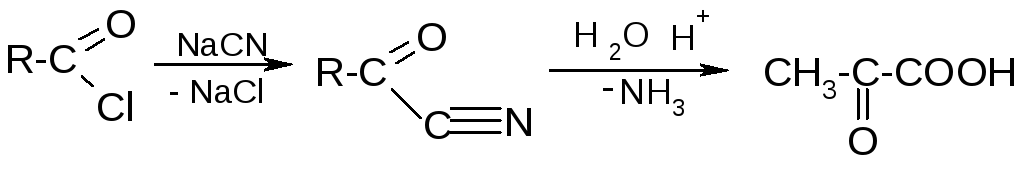
2) Окисление (дегидрирование) оксикислот:
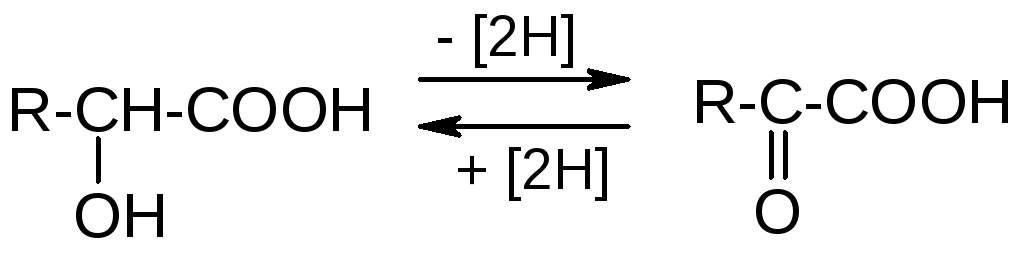
Реакция обратима – оксокислоты могут восстанавливаться (гидрироваться) в оксикислоты. Эти процессы имеют особо важное значение в биохимических превращениях, например, "молочная кислота ↔ пировиноградная кислота".
Химические свойства
Оксокислоты образуют производные по карбоксильной и по карбонильной группам (см. химические свойства карбоновых кислот, альдегидов и кетонов).
1) Кислотность
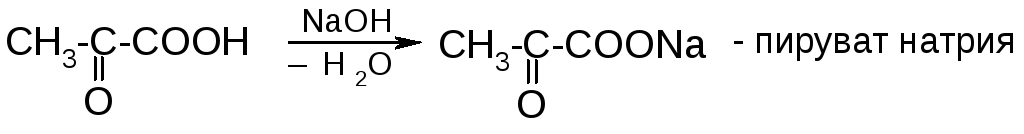
Карбонильная группа более сильный ЭА, чем гидроксильная, поэтому кислотность у оксокислот выше, чем у соответствующих оксикислот.
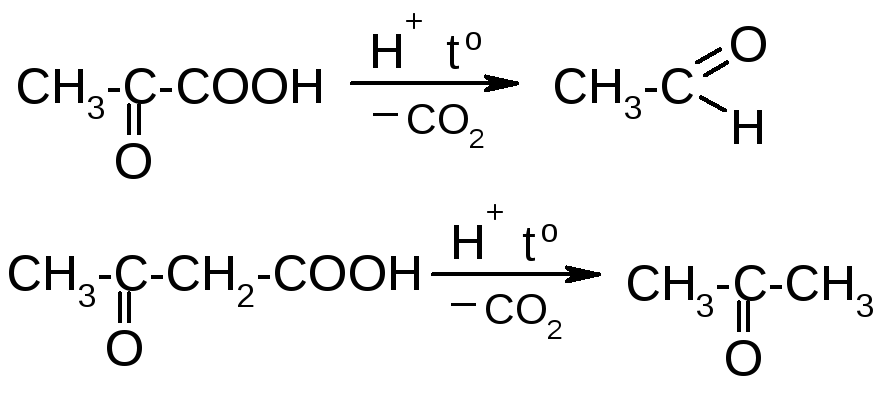
2) Декарбоксилирование
Элетроноакцепторное действие С=О-группы способствует элиминированию карбоксильной группы; α- и β-оксокислоты легко декарбоксилируются:
КЕТО-ЕНОЛЬНАЯ ТАУТОМЕРИЯ β-ОКСОКИСЛОТ
Таутомерия – это способность химического соединения существовать в виде равновесной смеси изомеров (равновесная изомерия)
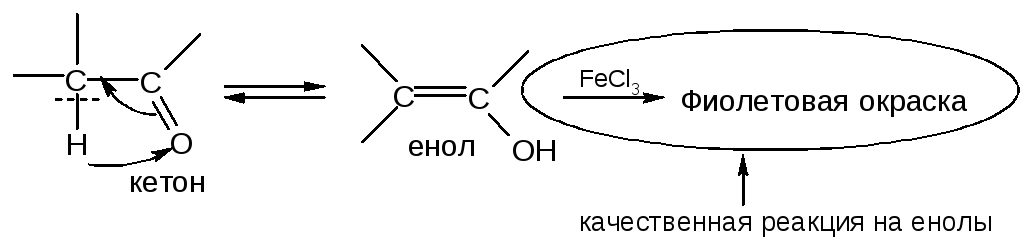
Такое равновесие возможно и в простых альдегидах и кетонах, но там содержание енольной формы ничтожно мало. Совместное ЭА влияние СООН- и С=О-групп в β-кетокислотах 1) значительно увеличивает подвижность протонов у α-углерод-ного атома и 2) образующаяся енольная форма содержит сопряженную систему, что значительно увеличивает её термодинамическую устойчивость.
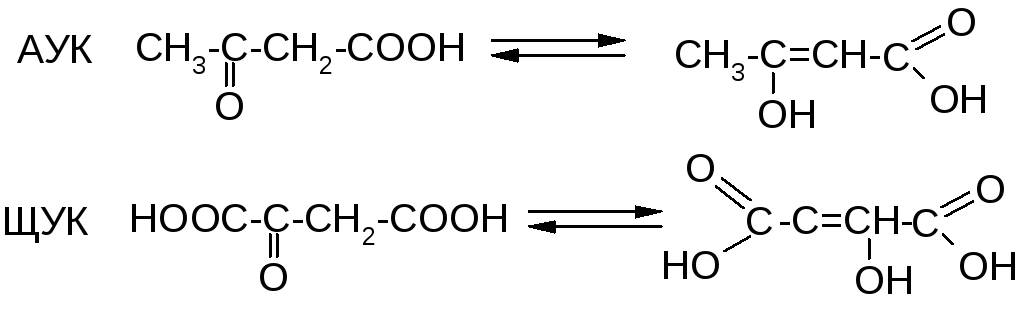
По этим причинам β-кетокислоты существуют в виде равновесия "кетон ↔ енол", где содержание енольной формы достигает многих процентов.
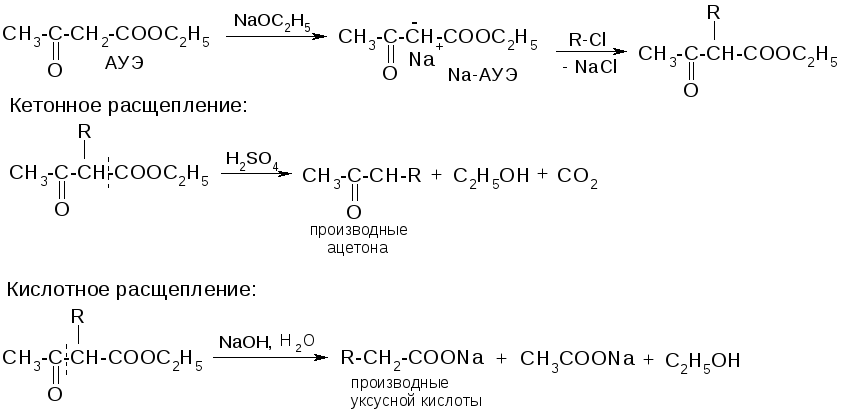
АЦЕТОУКСУСНЫЙ ЭФИР
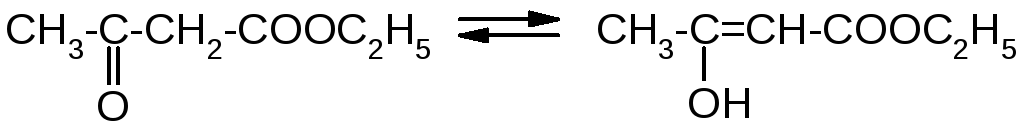
Равновесие содержит около 8% енольной формы и её можно обнаружить с помощью цветной реакции с FeCl3.
Применение в органическом синтезе
Аминокислоты
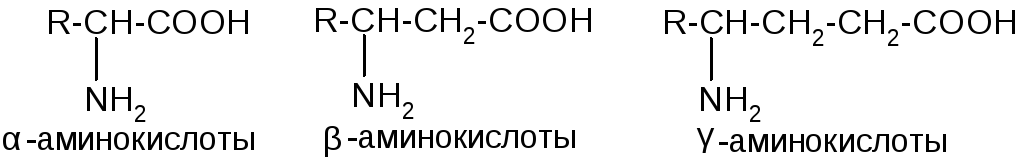
Наибольшее значение имеют α-аминокислоты , т.к. они являются метаболитами в обмене веществ и "строительным материалом" для важнейших биополимеров – полипептидов и белков.
СТЕРЕОИЗОМЕРИЯ α-АМИНОКИСЛОТ
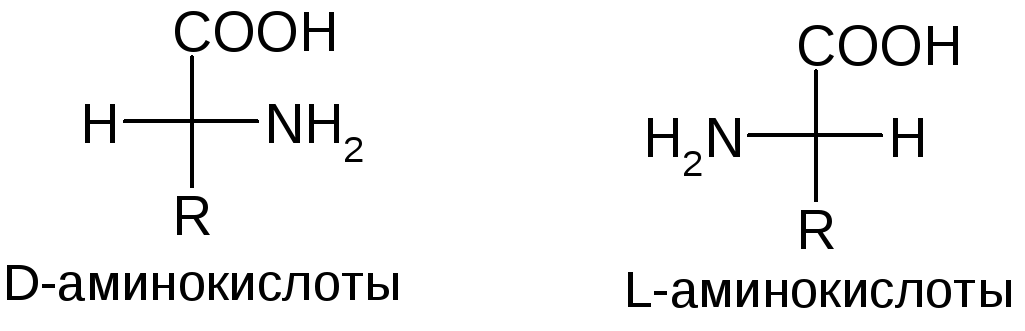
Все аминокислоты, участвующие в обмене веществ и входящие в состав полипептидов и белков, имеют L-конфигурацию (стереоспецифичность ферментов).
Способы получения аминокислот
1) Из галогенопроизводных кислот:
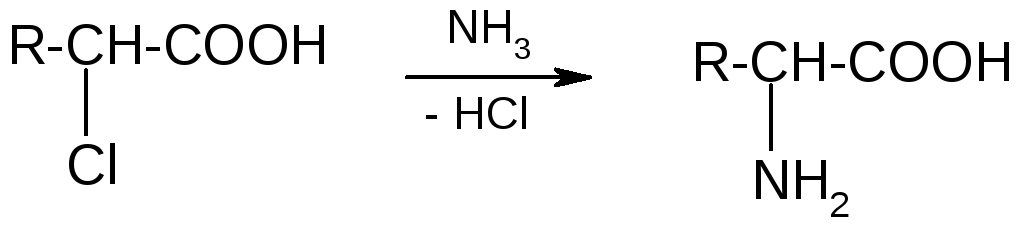
2) Из альдегидов (метод Штреккера-Зелинского):
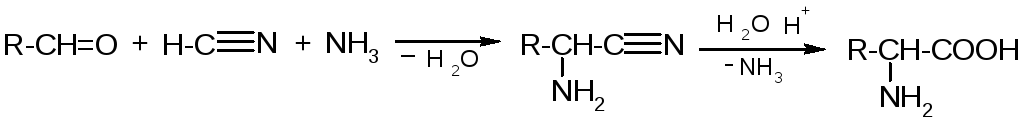
3) Из нитроуксусной кислоты:
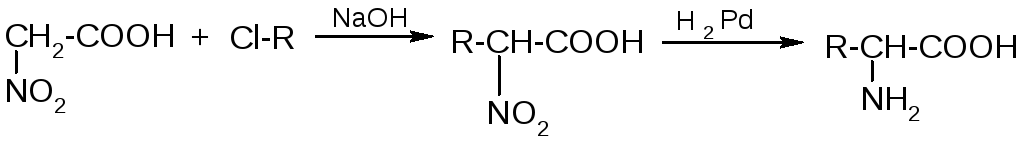
4) Восстановительное аминирование α-оксокислот:
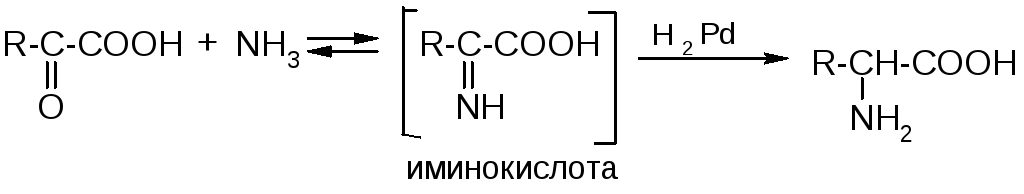
Химические свойства
1) Кислотно-основные свойства
а) амфотерность:
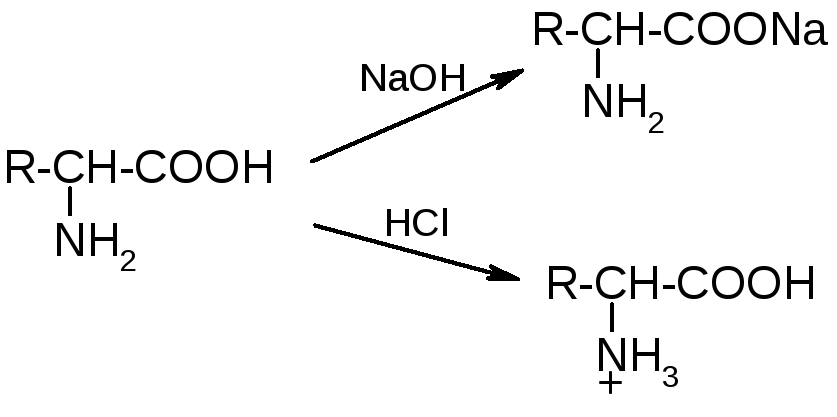
б) образование биполярных ионов (цвиттер-ионов):

в) строение аминокислот в растворе:
Ионогенная группа – это функциональная группа, которая в водном растворе имеет структуру иона.
Аминокислоты содержат две ионогенные группы:
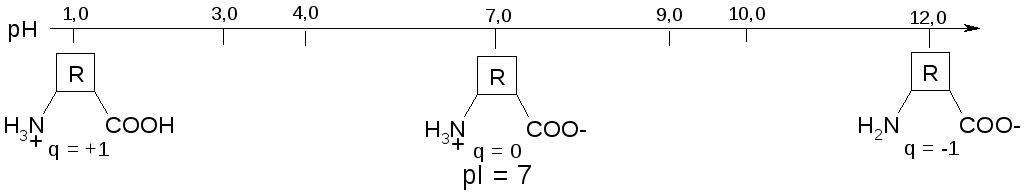
В водном растворе молекулы аминокислот всегда имеют электрический заряд, изменяющийся при изменении рН раствора.
Изоэлектрическая точка (рI) – это значение рН, при котором суммарный заряд молекулы равен О.
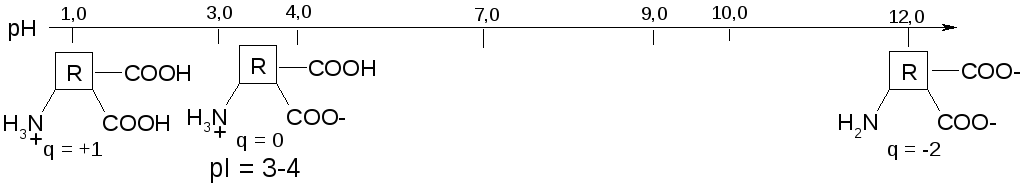
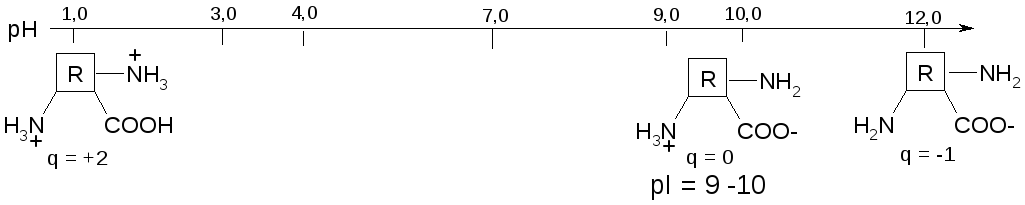
Выводы:
1) Если количества ионогенных групп (COOH и NH2) в молекуле одинаковы, то изолектрическая точка АК находится в области нейтрального рН (pI = 7, нейтральные АК).
2) Если в молекуле преобладают карбоксильные группы, то изолектрическая точка АК находится в кислотной области рН (pI < 7, кислые АК).
3) Если в молекуле преобладают аминогруппы, то изолектрическая точка АК находится в основной области рН (pI > 7, основные АК).
4) Если рН раствора ниже ИЭТ, то молекула имеет положительный заряд, если рН раствора выше ИЭТ, то молекула имеет отрицательный заряд.
Эти закономерности справедливы не только для индивидуальных аминокислот, но и для их полимеров – полипептидов и белков.
2) Реакции карбоксильной группы
Общие реакции: образование солей и функциональных производных.
Декарбоксилирование:
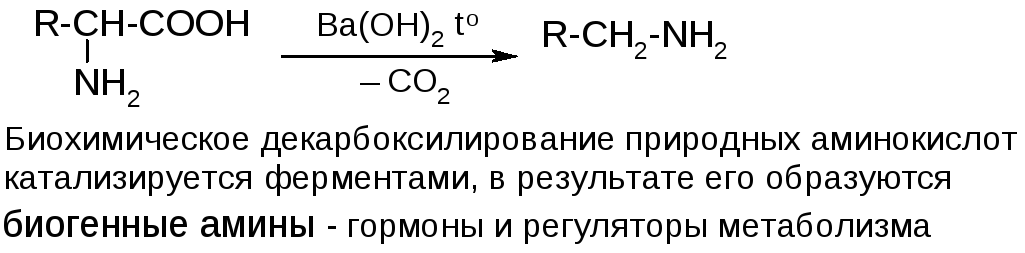
3) Реакции аминогруппы
Общие реакции: образование солей, ацилирование, алкилирование.
Дезаминирование:
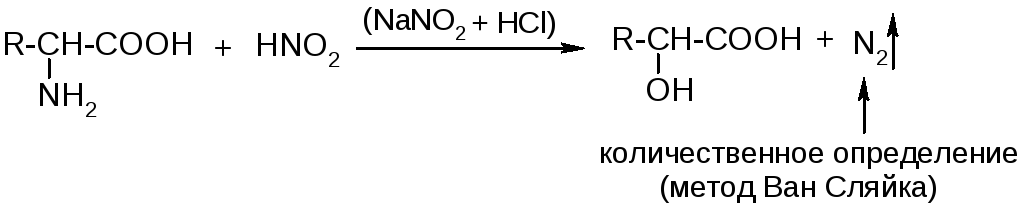
Природные α-аминокислоты
Строение и классификация природных α-аминокислот – см. Учебник (основной курс) – таблица на стр. 584 (первые три колонки) – выучить наизусть!
Биологическое значение и практическое применение аминокислот
Наибольшее биологическое значение имеют α-аминокислоты. Они являются структурными компонентами полипептидов и белков, многие из них служат биологическими предшественниками биогенных аминов – гормонов и биорегуляторов.
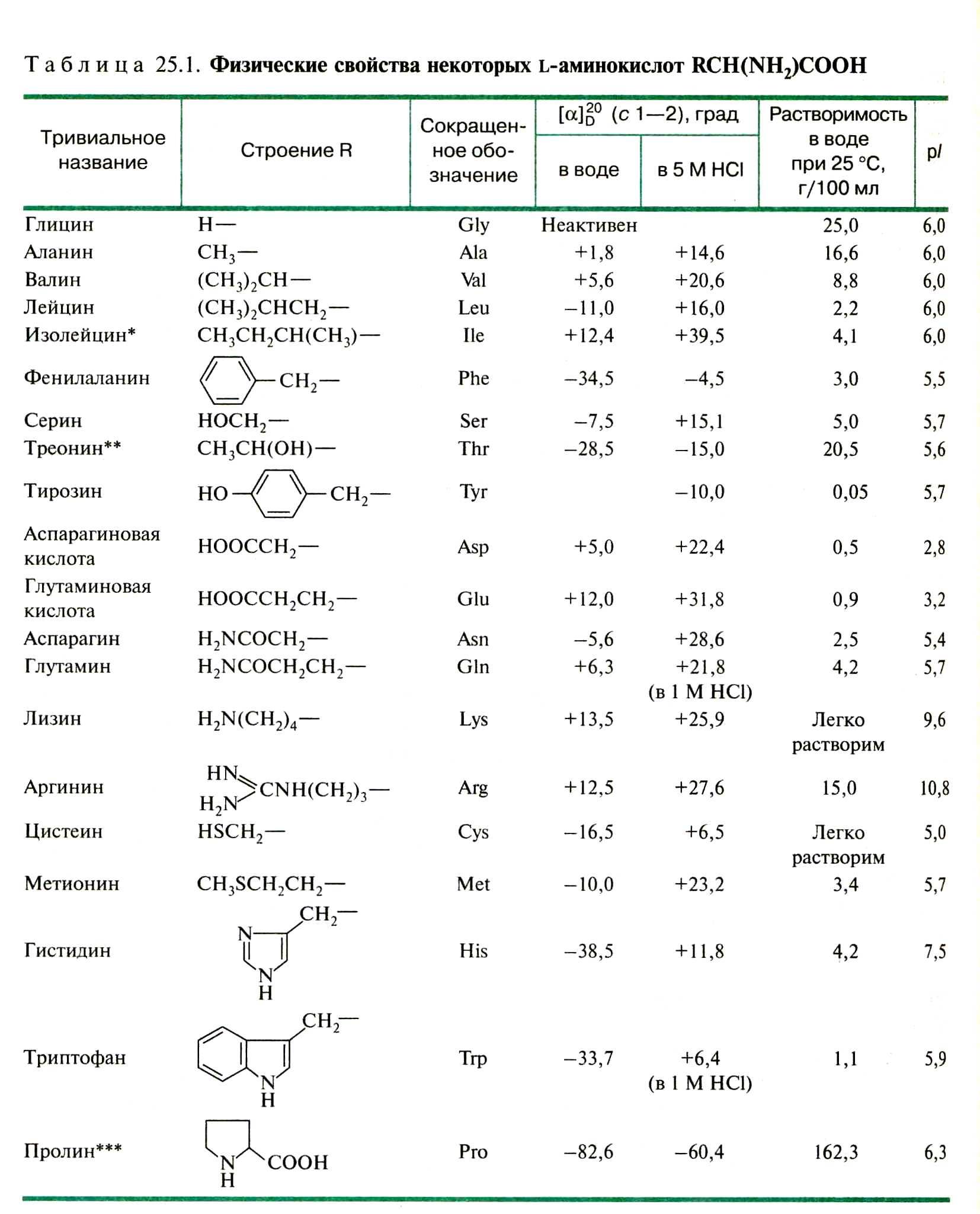
Многие аминокислоты применяются как лекарственные препараты:
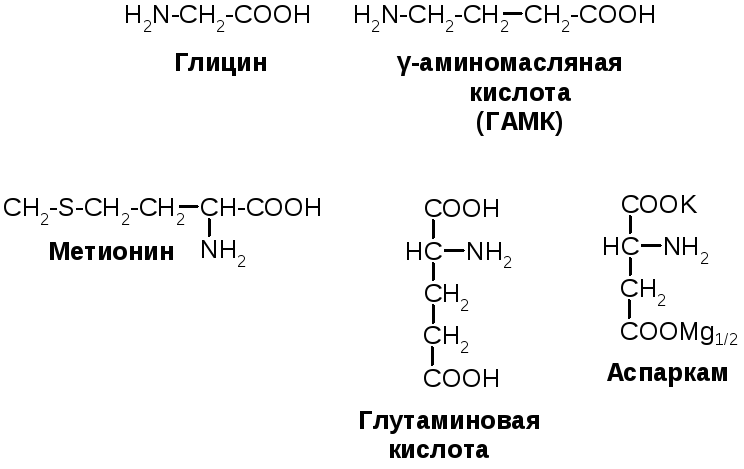
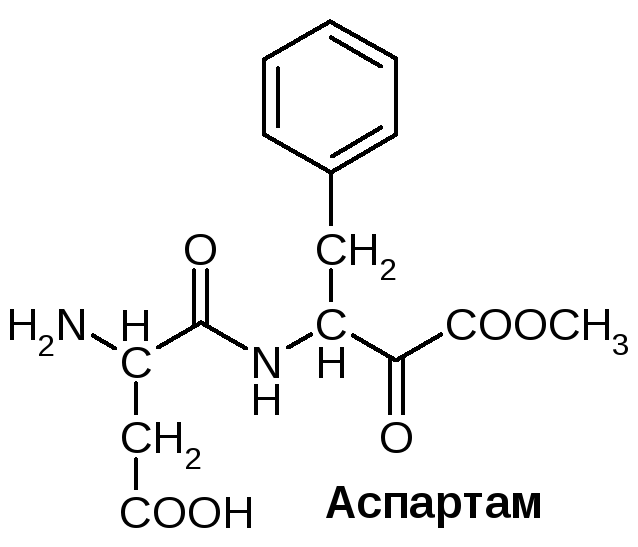
Некоторые аминокислоты (например, глицин) имеют сладкий вкус. Особенно интенсивный сладкий вкус имеет дипептид Асп-Фен. Под названием аспартам он применяется как заменитель сахара для диабетиков:
ЛИТЕРАТУРА:
Основная
1. Белобородов В.Л., Зурабян С.Э., Лузин А.П., Тюкавкина Н.А. – Органическая химия (основной курс), кн. 1 – Дрофа, М., 2003 г., с. 558-604.
1. Тюкавкина Н.А., Зурабян С.Э., Белобородов В.Л. и др. – Органическая химия (специальный курс), кн.2 – Дрофа, М., 2008 г., с. 178-207.
Дополнительная
2. Н.А.Тюкавкина, Ю.И.Бауков – Биоорганическая химия – ДРОФА, М., 2007 г., с. 316-345.
05.12.10
