
- •Специфика органической химии
- •Теория гибридизации
- •Типы гибридных орбиталей
- •Первое валентное состояние атома углерода Гибридизация sp3
- •Мезомерный эффект (эффект сопряжения) [±m]
- •Понятие сопряжения
- •Эффекты сопряжения
- •Правило Морковникова
- •Донорно-акцепторные связи. Семиполярные связи
- •Водородная связь
- •Названия ненасыщенных и ароматических углеводородов
- •Номенклатура гетероциклических соединений
- •Номенклатура июпак для производных различных классов органических соединений
- •Изомерия органических соединений
- •Структурная изомерия
- •Изомерия положения
- •Геометрическая изомерия (зеркальная, цис- транс- изомерия)
- •Оптическая изомерия
- •Устройство поляриметра
- •Диастереомеры
- •Номенклатура стереоизомеров
- •Номенклатура Кана, Ингольда, Прелога (кип)
- •Номенклатура стереоизомеров Потапова в.М., Терентьева а.П. И сотрудников
- •2(Ρ),3-диоксипропаналь
- •3(Ρ),4-дихлорпентен-4-аль
- •Классификация органических реакций и реагентов
- •По способу разрыва (образования) химических связей.
- •Классификация реакций по типу превращений в органических веществах
- •Свободные радикалы
- •Понятие о граничных структурах
- •Алканы (парафины)
- •Физические свойства
- •Промышленная переработка алканов (нефти)
- •Некоторые лабораторные способы получения алканов
- •Нитрование алканов
- •Строение малых циклов (циклопропан, циклобутан)
- •Некоторые закономерности реакции отщепления
- •Дегидратация спиртов (отщепление воды)
- •Дегалогенирование дигалогенпроизводных
- •Восстановление алкинов (ацетиленов)
- •Расщепление четвертичных аммонийных солей по Гофману
- •Присоединение галогенов
- •Строение диенов
- •Химические свойства диенов
- •Реакции присоединения
- •Механизм реакции [ae] для сопряженных диенов
- •Некоторые аспекты применения сопряженных диенов
- •Алкины (ацетилены)
- •Способы получения ацетилена
- •Некоторые способы получения гомологов ацетилена
- •Общая характеристика реакционной способности ацетиленов
- •Физические свойства ацетилена
- •Химические свойства
- •Реакции присоединения
- •Реакции нуклеофильного присоединения к ацетиленам
- •Некоторые свойства виниловых эфиров
- •Ароматические углеводороды
- •Признаки ароматичности
- •Направление реакций ароматических соединений
- •II стадия:
- •Мнемоническое правилосмещения электронной плотности под действием заместителя в ядре
- •Нуклеофильное замещение в ароматических системах (snAr)
- •Механизм реакции snAr
- •Галогенпроизводные углеводородов
- •Методы получения галогенпроизводных
- •Замещение водорода на галоген в условиях радикальных процессов (прямое галогенирование алканов)
- •Галогенирование непредельных углеводородов
- •Получение галогенпроизводных из непредельных углеводородов
- •Общая характеристика реакционной способности галогенпроизводных
- •Важнейшие реакции галогенпроизводных
- •Образование металлорганических соединений
- •Содержание
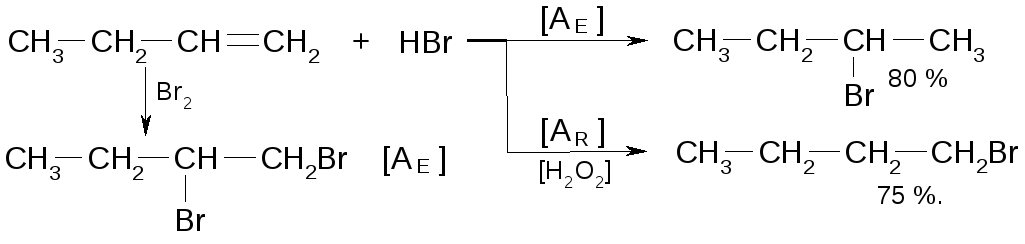
Получение галогенпроизводных из непредельных углеводородов
Во всех случаях ионных реакций работает правило Морковникова.
Алкены
Алкины
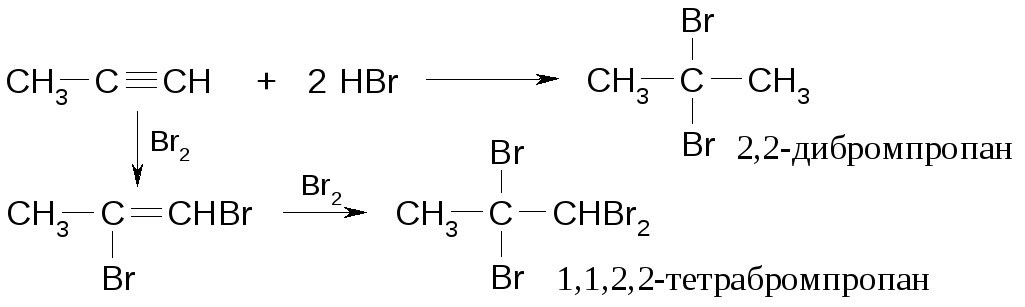
Общая характеристика реакционной способности галогенпроизводных
По реакционной способности к нуклеофильному замещению галогенпроизводные подразделяются:
Галогенпроизводные с нормальной реакционной способностью:
![]()
Галогенпроизводные с пониженной реакционной способностью:
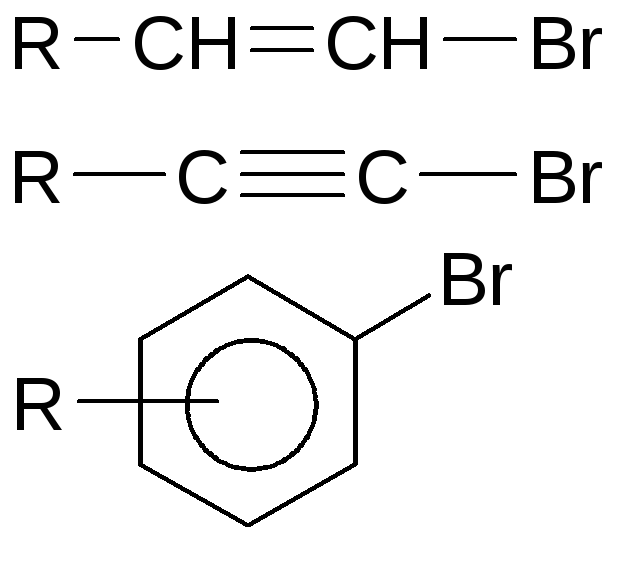
Галогенпроизводые с повышенной реакционной способностью:
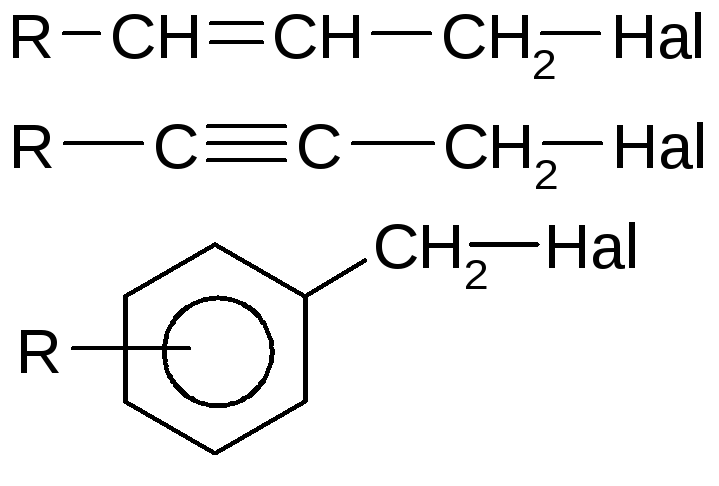
Пониженная реакционная способность объясняется двоесвязанностьюгалогена за счет эффекта сопряжения с находящейся рядом π-системой:

Повышенная подвижность галогена объясняется устойчивостьюобразующихсякарбокатионов:
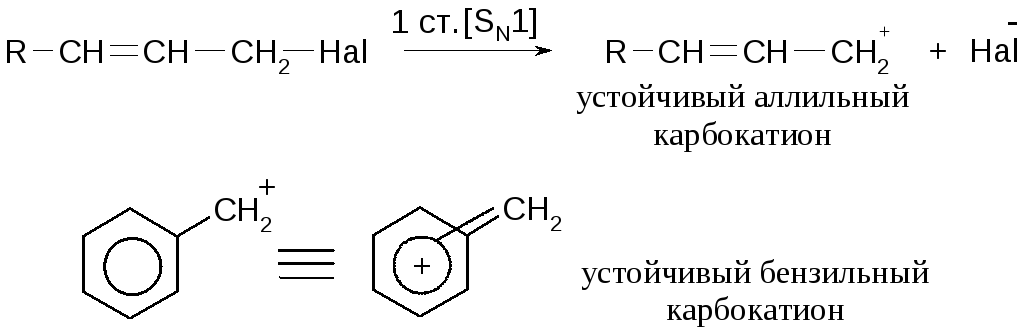
Вследствие устойчивости образующегося карбокатиона реакции нуклеофильного замещения (гидролиз) аллильных и бензильных галогенводородов протекают очень легко.
Разница в реакционной способности перечисленных групп галогенпроизводных проиллюстрируем условиями реакций.
Галогенпроизводные с нормальной реакционной способностью гидролизуют кипячением с водными растворами щелочей (100 С).
Галогенпроизводные с пониженной реакционной способностью замещают галоген в жестких условиях. В промышленности фенолы получают гидролизом галогенпроизводных бензола:
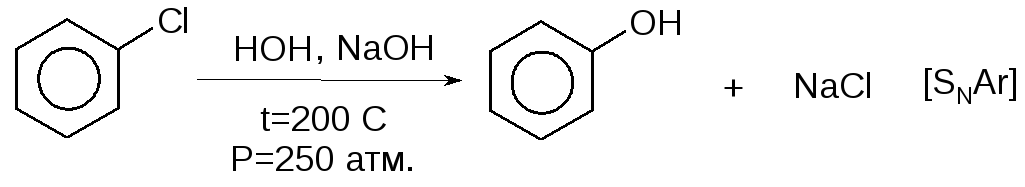
Галогенпроизводные с повышенной реакционной способностью гидролизуются при кипячении с водой.
Если активировать отщепление (замещение) акцепторными группами, то реакция с водой пойдет уже при комнатной температуре. Например, тринитрохлорбензол используют для обнаружения спиртов:
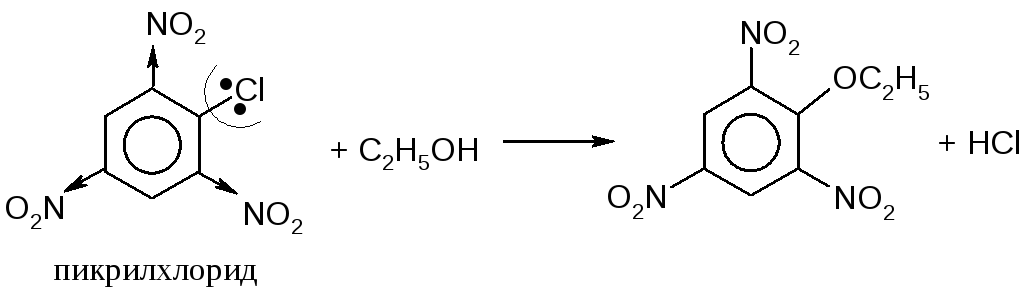
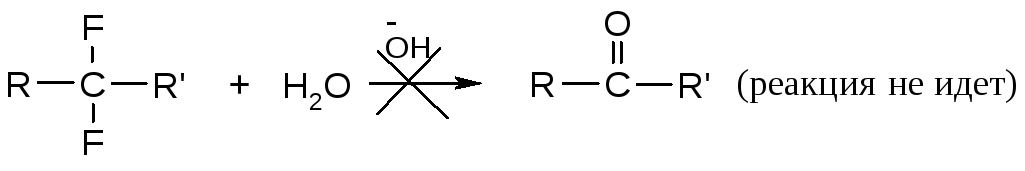
Реакционная способность фторпроизводных зависит от количества атомов фтора и места их расположения в молекуле.
Первичные фторпроизводные реагируют так же, как и другие галогенпроизводные. Для ди-, три- и тетрафторпроизводных выяснена устойчивость их в реакциях отщепления и замещения. Особенно это касается геминальных ди- и полифторпроизводных.
Важнейшие реакции галогенпроизводных
Этот класс соединений используют для синтеза непредельных соединений, циклоалканов, спиртов, альдегидов, кетонов, карбоновых кислот, простых и сложных эфиров, а также их тиоаналогов.
Реакции гидролиза
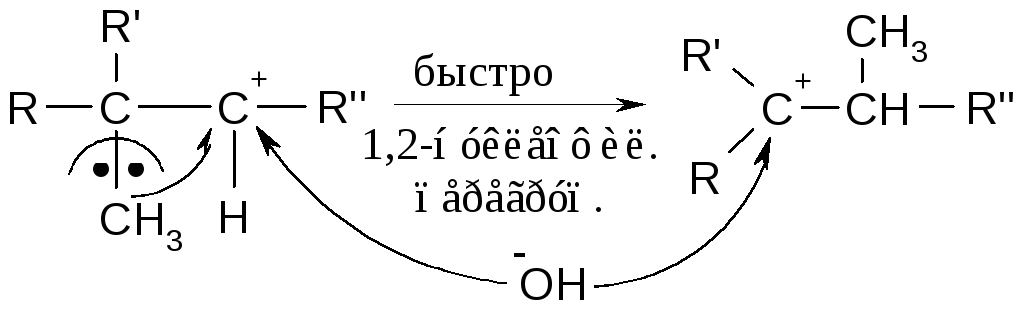
В связи с конкурентностью реакций [SN] и [E] (постоянно сопровождают друг друга), в продуктах этих реакций будут присутствовать спирты, алкены и продукты изомеризации углерод-углеродного скелета.

или перегруппировки:
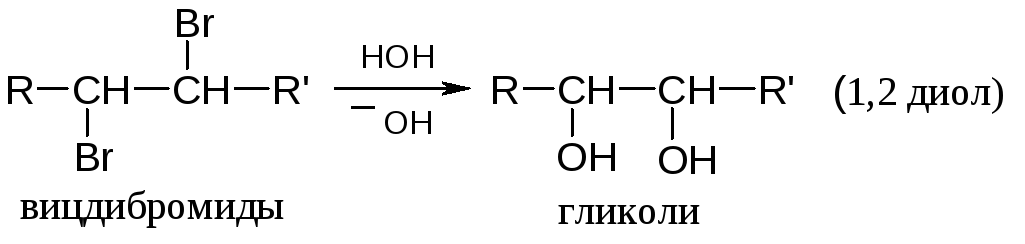
При гидролизе дигалогенпроизводных могут образовываться диолы или карбонильные соединения. Например:
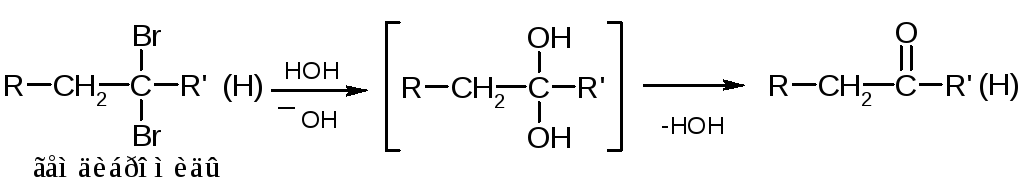

Образование простых эфиров
Простые эфиры легко образуются при взаимодействии галогенпроизводных с алкоголятами спиртов:
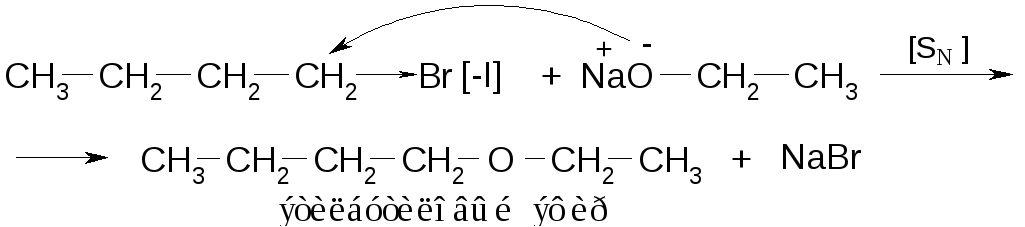
Если вместо алкоголятов использовать соли карбоновых кислот (литиевые, серебряные), то образуются сложные эфиры:
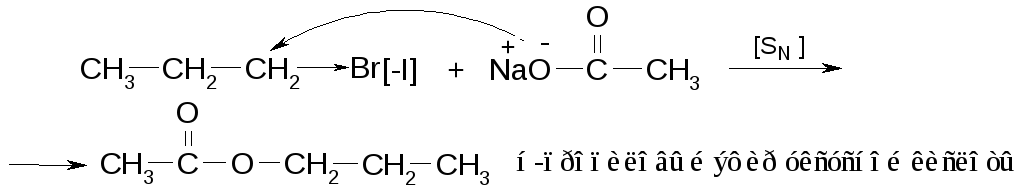
Синтез меркаптанов и сульфидов
Реакции протекают по аналогичной схеме:

Подобные соединения обладают восстанавливающими свойствами.
Образование нитрилов карбоновых кислот
Для растворения неорганических солей используют суперрастворители (диметилформамид, диметилсульфоксид). Например, при небольшом нагревании галогенпроизводные вступают в реакции с цианидами:
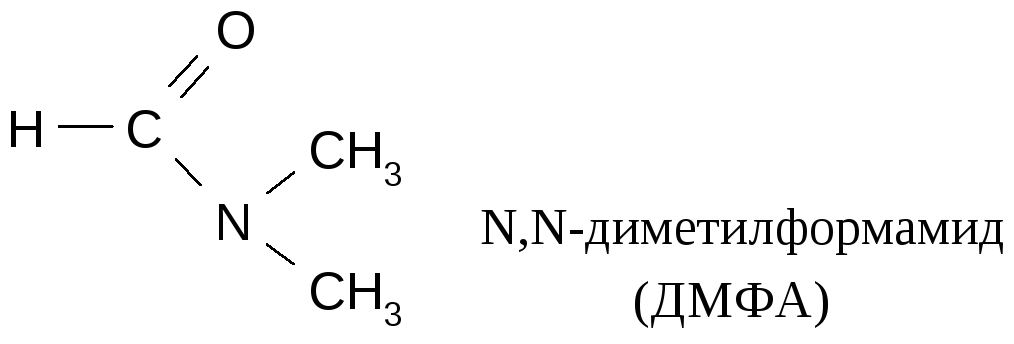
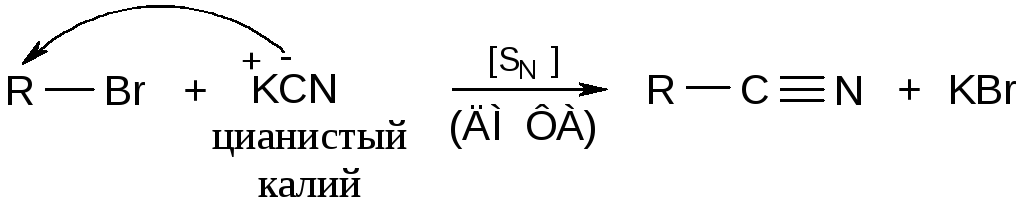
Синтез нитросоединений
Легче всего реакция протекает с азотистокислым серебром, хуже с калиевыми или литиевыми солями:
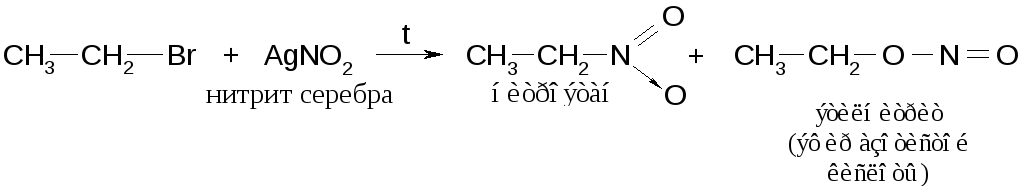
Синтез аминов

Первичные амины получают из алкилгалогенидов и аммиака:

Первичный амин из-за (+I)-эффекта алкильных группнуклеафильнееаммиака, поэтому реакция галогенпроизводного с первичным амином пойдет легче, чем с аммиаком:
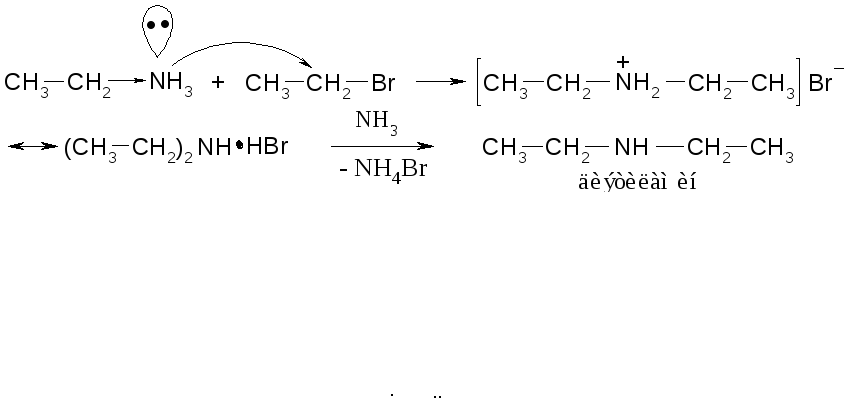
Аналогично получают третичный амин.
Третичные амины могут также участвовать в реакции с галогенпроизводными:
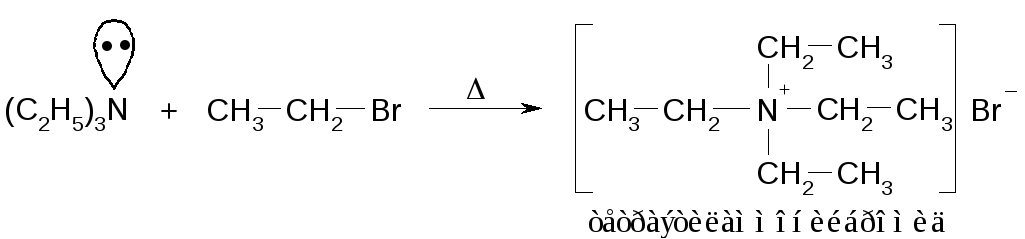
Алкиламмониевые соли являются поверхностно-активными веществами. В некоторых случаях обладают антисептической биологической активностью и уничтожают запахи. Используются в качестве катализаторов в гетерогенных реакциях (способствуют реакции межфазного переноса).
Четвертичные аммониевые соли реагируют со щелочами, давая четвертичные аммониевые основания: [R4N]+OH–. Подобные соединения являются супероснованиями (высокая степень диссоциации), используются для создания суперосновных сред.
