
- •Техническая термодинамика и теплотехника
- •2 Предмет и метод технической термодинамики
- •1Основные понятия и определения
- •4Термодинамическая система
- •3 Основные параметры состояния
- •5 Уравнение состояние
- •6 Работа газа и теплота
- •Термодинамический процесс
- •7 Идеальные газы и их смеси
- •8 Газовые смеси
- •9 Способы задания смеси газов
- •Определение кажущейся молекулярной массы и параметров состояния смеси
- •24 Теплоемкость
- •10 Первый закон термодинамики
- •11 Энтальпия
- •12 Энтропия
- •14 Термический кпд
- •15 Цикл Карно
- •16 Аналитическое выражение 2-го закона т-ки
- •17 Изменение энтропии в необратимых процессах
- •18 Эксэргия
- •19 Термодинамические процессы
- •Политропный процесс
- •28 Термодинамические процессы в реальных газах и парах Свойства реальных газов
- •32 Водяной пар Основные понятия и определения
- •33 Pv-диаграмма водяного пара
- •34 Тs-диаграмма водяного пара
- •35Is-диаграмма водяного пара
19 Термодинамические процессы
При изучении равновесных и обратимых термодинамических процессов идеальных газов должны быть выявлены: во-первых, закономерность изменения основных параметров, характеризующих состояние рабочего тела; во-вторых, особенности реализации условий первого закона термодинамики.
В общем случае два любых параметра рабочего тела могут изменяться произвольно. Однако наибольший интерес представляют частные случаи. К числу частных термодинамических процессов относятся: изохорный, изобарный, изотермический, адиабатный, и политропный, который при определенных условиях может рассматриваться в качестве обобщенного по отношению ко всем выше перечисленным процессам.
Политропный процесс
Политропным процессом называется такой термодинамический процесс изменения состояния физической системы, при котором в течение всего процесса сохраняется постоянство теплоемкости.
Пусть
С – теплоемкость политропного процесса,
тогда используя выражения
![]() или
или
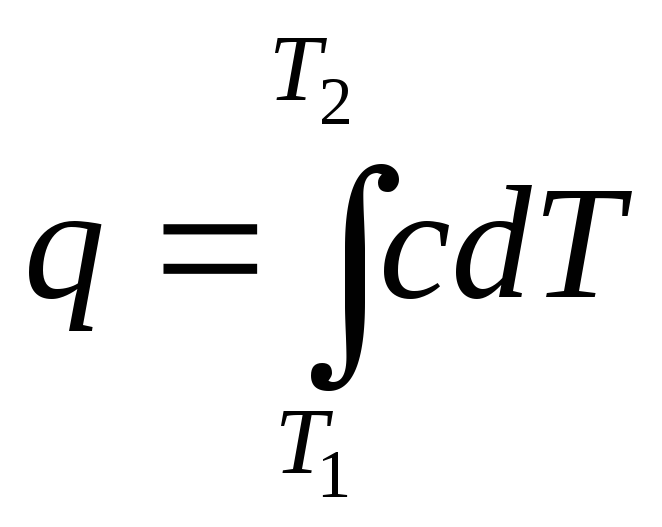 ;
;
![]() и
и
![]() ,
получим уравнение первого закона
термодинамики в виде:
,
получим уравнение первого закона
термодинамики в виде:
![]() . (92)
. (92)
С
учетом выражения
![]() после
ряда преобразований имеем:
после
ряда преобразований имеем:
![]() , (93)
, (93)
откуда получим уравнение политропы:
![]() , (94)
, (94)
где ![]() – показатель политропы.
– показатель политропы.
Согласно определению политропного процесса n может быть любым, но постоянным в некотором интервале числом, которое достаточно близко воспроизводило бы разнообразные встречающиеся в практике линии индикаторных диаграмм.
Очевидно, что при некоторых частных значениях n уравнение (94) должно превращаться в уравнения простейших термодинамических процессов.
20 Действительно, если в уравнении (94) n = 0, получим уравнение изобары:
![]() .
.
В этом случае (для изобарного процесса) уравнение первого закона термодинамики для изолированных систем будет совпадать с формулой (49).
При
![]() получим уравнение изохоры:
получим уравнение изохоры:
![]() ,
,
поскольку
величина
![]() будет бесконечно мала по сравнению с
объемом (
будет бесконечно мала по сравнению с
объемом (![]() ),
ею можно пренебречь, тогда:
),
ею можно пренебречь, тогда:
![]() .
.
22
Из определения изохорного процесса
очевидно, что работа в этом процессе не
совершается, поскольку работа есть
произведение
![]() (работа всегда связана с изменением
объема). Тогдауравнение
первого закона термодинамики для
изолированных систем
(49) при
изохорном процессе
примет вид:
(работа всегда связана с изменением
объема). Тогдауравнение
первого закона термодинамики для
изолированных систем
(49) при
изохорном процессе
примет вид:
![]() . (95)
. (95)
Таким образом, подведенная к изолированной системе теплота в изохорном процессе расходуется только на изменение внутренней энергии системы.
При
![]() получим уравнение изотермы:
получим уравнение изотермы:
![]() ,
,
но поскольку, согласно закону Бойля – Мариотта, если произведение давления и объема есть величина постоянная, то процесс – изотермический, тогда:
![]() .
.
21 В изотермическом процессе не происходит изменения внутренней энергии системы, поскольку температура постоянна. Тогда уравнение первого закона термодинамики для изолированных систем (49) при изотермическом процессе примет вид:
![]() . (96)
. (96)
Таким образом, подведенная к изолированной системе теплота в изотермическом процессе расходуется только на совершение системой внешней работы.
При
![]() получим уравнение адиабаты:
получим уравнение адиабаты:
![]() .
.
23
Показатель адиабаты
![]() еще называют коэффициентом Пуассона.
Величина этого показателя зависит от
числа атомов в молекуле газа. При этом
еще называют коэффициентом Пуассона.
Величина этого показателя зависит от
числа атомов в молекуле газа. При этом
![]() может принимать следующие значения:
может принимать следующие значения:
для одноатомных газов (на самом деле состояние одноатомного газа не существует, оно введено для идеальных газов)
 ;
;для двухатомных газов (CO; О2; N2; Н2; F2; Cl2; воздух и др.)
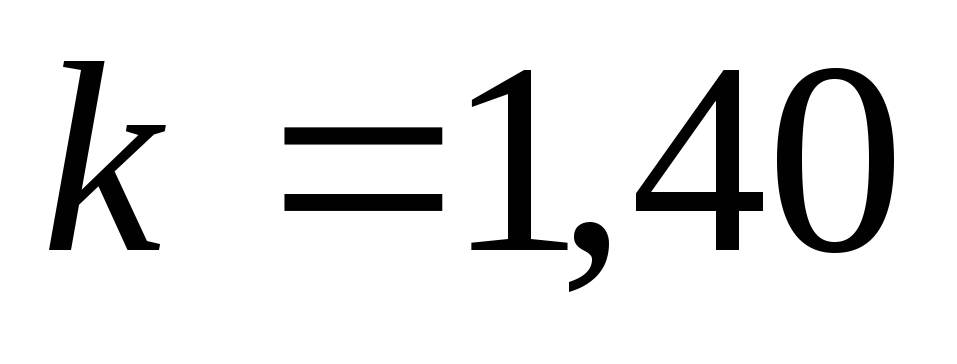 ;
;для трехатомных газов (CO2; N2O; NO2 и др.)
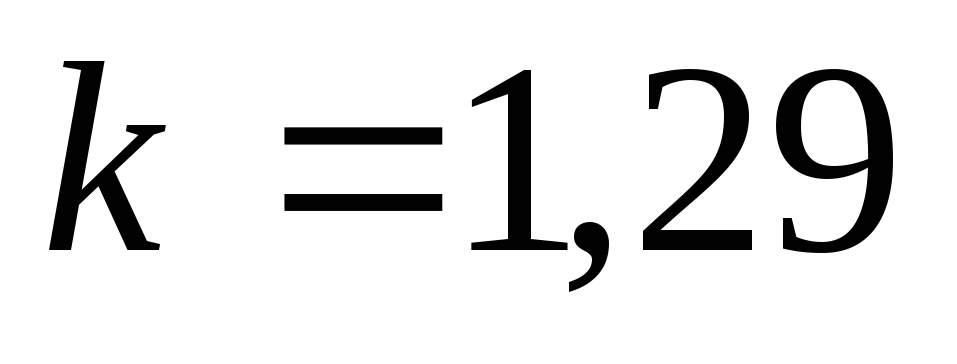 .
.
По
определению, адиабатный процесс – это
процесс, протекающий без теплообмена
с окружающей средой, т.е.
![]() .
Тогдауравнение
первого закона термодинамики для
изолированных систем
(49) при
адиабатном процессе
примет вид:
.
Тогдауравнение
первого закона термодинамики для
изолированных систем
(49) при
адиабатном процессе
примет вид:
![]() (97)
(97)
Таким образом, в адиабатном процессе работа может совершать за счет изменения (уменьшения) внутренней энергии системы в течение некоторого времени.
Таким образом политропный процесс является обобщающим по отношению к простейшим процессам. Для политропы справедливы соотношения:
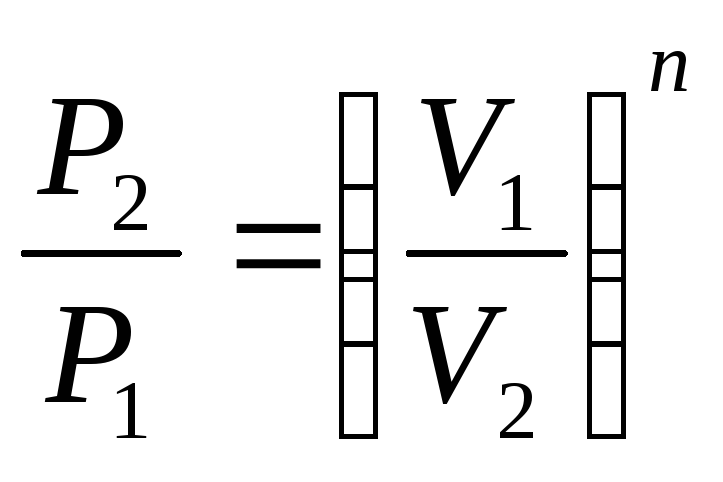 ;
;
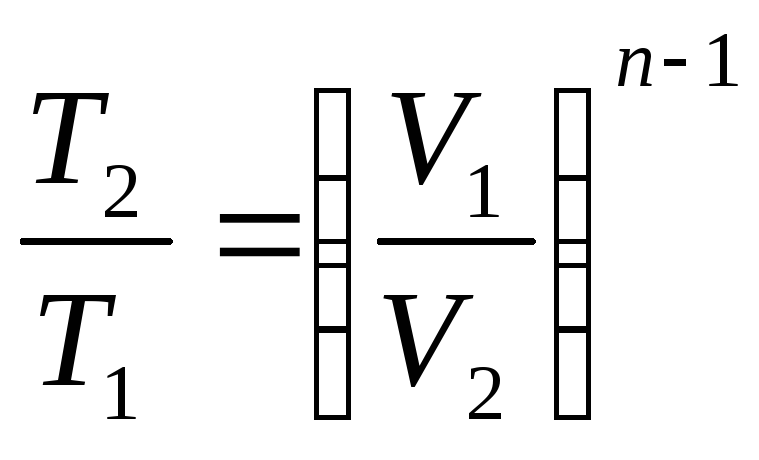 ;
;
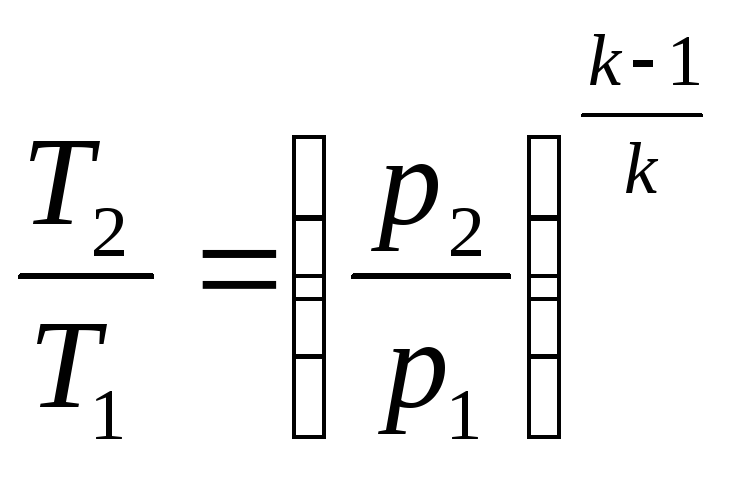 . (98)
. (98)
Работу политропного процесса можно определить по следующим формулам:
![]() ;
;
![]() ;
;
 ;
;
 ;
;
 . (99)
. (99)
В
PV-координатах
работа l
характеризуется
площадью под процессом. Если
![]() то
и
то
и![]() верно и обратное.
верно и обратное.
Теплоемкость политропного процесса можно определить по формуле:
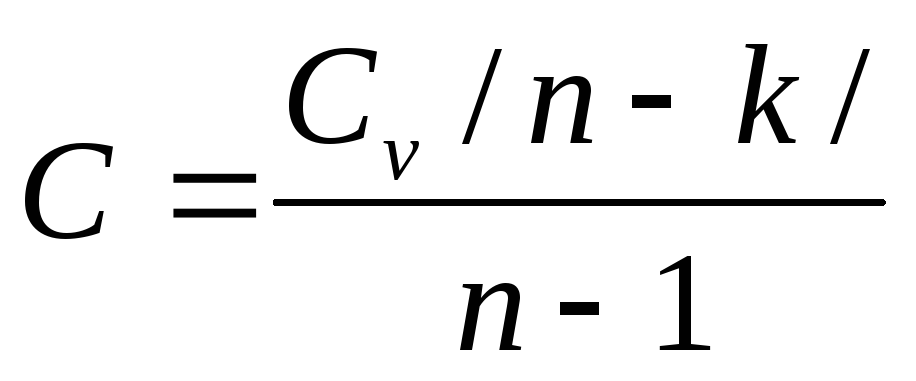 . (100)
. (100)
Таким образом, еще раз подтверждается, что теплоемкость идеального газа зависит от характера термодинамического процесса, что наглядно подтверждается на рисунке 7.
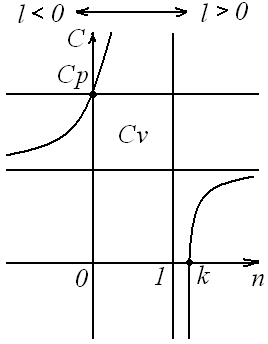
Рисунок 7 – Зависимость теплоемкости С процесса от показателя п политропы
На рисунке 8 представлены совмещенные диаграммы различнох термодинамических процессов.

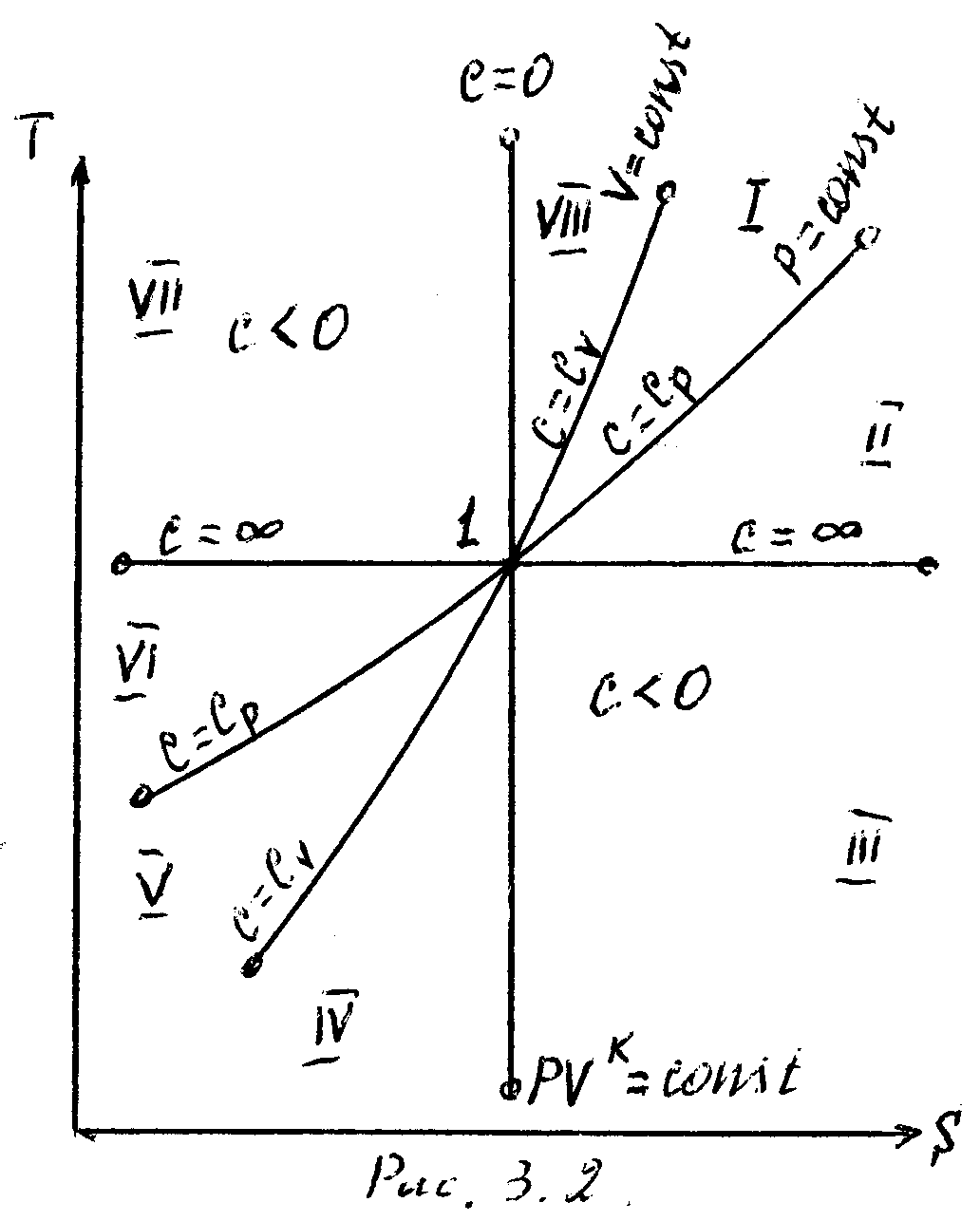
Рисунок 8 - Совмещенные диаграммы различных термодинамических
процессов в PV- и TS – координатах
Если в РV- и ТS – координатах выбрать некоторую произвольную точку 1 и провести из нее все рассмотренные выше термодинамические процессы, то все поле построенной таким образом диаграммы делится на 8 областей, характеризующихся определенными признаками. Так, все процессы слева от точки 1 на РV – диаграмме сопровождаются отрицательной работой. Все процессы справа от точки 1 на TS – диаграмме происходят с подводом теплоты, слева – с отводом теплоты, вверх от изотермы – с увеличением внутренней энергии и энтальпии; вниз – с уменьшением. Области, выделенные на PV – диаграмме, соответствуют процессам с подводом теплоты, а на ТS – диаграмме – процессам с положительной теплоемкостью и т.д.
Для
определения изменения энтропии в
политропном процессе достаточно
уравнение (100) подставить в выражение
![]() ,
и с учетом того, что
,
и с учетом того, что![]() получим:
получим:
![]() . (101)
. (101)
После интегрирования:
![]() . (102)
. (102)
С учетом выражений (98), можно записать:
![]() . (103)
. (103)
Изменения
внутренней энергии и энтропии в
политропном процессе определяются в
ТS – координатах площадями соответственно
под изохорным и изобарным процессами,
происходящими в том же интервале
температур
![]() .
.
