
Пособие-репетитор по химии
ЗАНЯТИЕ 10 10-й класс (первый год обучения)
Основы химической кинетики. Состояние химического равновесия План
1.
Химическая кинетика и область ее
изучения.
2. Скорость гомогенной и гетерогенной реакции.
3. Зависимость скорости реакции от различных факторов: природы реагирующих веществ, концентрации реагентов (закон действующих масс), температуры (правило Вант-Гоффа), катализатора.
4. Обратимые и необратимые химические реакции.
5. Химическое равновесие и условия его смещения. Принцип Ле Шателье.
Раздел химии, изучающий скорости и механизмы протекания химических реакций, называется химической кинетикой. Одним из основных в этом разделе является понятие скорости химической реакции. Одни химические реакции протекают практически мгновенно (например, реакция нейтрализации в растворе), другие – в течение тысячелетий (например, превращение графита в глину при выветривании горных пород).
Скорость гомогенной реакции – это количество вещества, вступающего в реакцию или образующегося в результате реакции за единицу времени в единице объема системы:
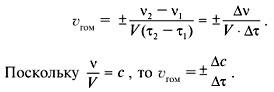
Другими словами, скорость гомогенной реакции равна изменению молярной концентрации какого-либо из реагирующих веществ за единицу времени. Скорость реакции – величина положительная, поэтому в случае выражения ее через изменение концентрации продукта реакции ставят знак «+», а при изменении концентрации реагента знак «–».
Скорость гетерогенной реакции – это количество вещества, вступающего в реакцию или образующегося в результате реакции за единицу времени на единице поверхности фазы:
![]()
Важнейшие факторы, влияющие на скорость химической реакции, – природа и концентрация реагентов, температура, присутствие катализатора.
Влияние природы реагентов проявляется в том, что при одних и тех же условиях различные вещества взаимодействуют друг с другом с разной скоростью, например:

При увеличении концентрации реагентов увеличивается число столкновений между частицами, что приводит к увеличению скорости реакции. Количественно зависимость скорости реакции от концентрации реагентов выражается з а к о н о м д е й с т в у ю щ и х м а с с (К.М.Гульдберг и П.Вааге, 1867 г.; Н.И.Бекетов, 1865 г.). Скорость гомогенной химической реакции при постоянной температуре прямо пропорциональна произведению концентрации реагирующих веществ в степенях, равных их стехиометрическим коэффициентам(концентрации твердых веществ при этом не учитываются), например:
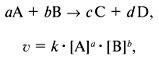
где А и В – газы или жидкости, k – константа скорости реакции, равная скорости реакции при концентрации реагентов 1 моль/л. Константа k зависит от свойств реагирующих веществ и температуры, но не зависит от концентрации веществ.
Зависимость скорости реакции от температуры описывается экспериментальным п р а в и л о м В а н т-Г о ф ф а (1884 г.). При повышении температуры на 10°, скорость большинства химических реакций увеличивается в 2–4 раза:
![]()
где ![]() –
температурный коэффициент.
–
температурный коэффициент.
Катализатором называется вещество, изменяющее скорость химической реакции, но не расходующееся в результате этой реакции. Различают положительные катализаторы (специфические и универсальные), отрицательные (ингибиторы) и биологические (ферменты, или энзимы). Изменение скорости реакции в присутствии катализаторов называется катализом. Различают гомогенный и гетерогенный катализ. Если реагенты и катализатор находятся в одном агрегатном состоянии, катализ является гомогенным; в разных – гетерогенным.
Гомогенный катализ:
![]()
гетерогенный катализ:
![]()
Механизм действия катализаторов является очень сложным и не изученным до конца. Существует гипотеза об образовании промежуточных соединений между реагентом и катализатором:
А
+ кат. ![]() [A
кат.],
[A
кат.],
[A
кат.] + В ![]() АВ
+ кат.
АВ
+ кат.
Для усиления действия катализаторов применяют промоторы; существуют также каталитические яды, ослабляющие действие катализаторов.
На скорость гетерогенной реакции влияют величина поверхности раздела фаз (степень измельченности вещества) и скорость подвода реагентов и отвода продуктов реакции от поверхности раздела фаз.
Все химические реакции делятся на два типа: обратимые и необратимые.
Необратимыми называются химические реакции, протекающие только в одном направлении, т.е. продукты этих реакций не взаимодействуют друг с другом с образованием исходных веществ. Условия необратимости реакции – образование осадка, газа или слабого электролита. Например:
BaCl2 +
H2SO4 =
BaSO4![]() +
2HCl,
+
2HCl,
K2S
+ 2HCl = 2KCl + H2S![]() ,
,
HCl + NaOH = NaCl + H2O.
Обратимыми называются реакции, протекающие одновременно в прямом и обратном направлениях, например:
![]()
При протекании обратимой химической реакции скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие уменьшения концентрации исходных веществ. Обратная реакция, наоборот, в начальный момент времени имеет минимальную скорость, которая постепенно увеличивается. Таким образом, в определенный момент времени наступаетсостояние химического равновесия, при котором скорость прямой реакции равна скорости обратной реакции. Состояние химического равновесия является динамическим – продолжают протекать как прямая, так и обратная реакции, но поскольку скорости их равны, то концентрации всех веществ в реакционной системе не изменяются. Эти концентрации называются равновесными.
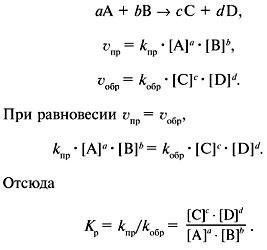
Отношение констант скоростей прямой и обратной реакций является постоянной величиной и называется константой равновесия (Кр). Концентрации твердых веществ не входят в выражение константы равновесия. Константа равновесия реакции зависит от температуры и давления, но не зависит от концентрации реагирующих веществ и от присутствия катализатора, который ускоряет ход как прямой, так и обратной реакции. Чем больше Кр, тем выше практический выход продуктов реакции. Если Кр > 1, то в системе преобладают продукты реакции; если Кр < 1, в системе преобладают реагенты.
Химическое равновесие является подвижным, т.е. при изменении внешних условий может увеличиваться скорость прямой или обратной реакции. Направление смещения равновесия определяется п р и н ц и п о м, сформулированным французским ученым Ле Шателье в 1884 г. Если на равновесную систему оказывается внешнее воздействие, то равновесие смещается в сторону той реакции, которая противодействует этому воздействию. На смещение равновесия влияют изменения концентрации реагентов, температуры и давления.
Увеличение концентрации реагентов и вывод продуктов приводят к смещению равновесия в сторону прямой реакции.
При нагревании системы равновесие смещается в сторону эндотермической реакции, при охлаждении – в сторону экзотермической.
Для реакций, в которых принимают участие газообразные вещества, повышение давления смещает равновесие в сторону реакции, протекающей с уменьшением числа молекул газа. Если реакция протекает без изменения числа молекул газообразных веществ, то изменение давления никак не влияет на смещение равновесия.
