
Курсовая работа / Производство серной кислоты - Вариант 4 - Сучкова - Дьячкова - 2005 / Курсовик мой
.doc
РХТУ им. Д.И.Менделеева
Кафедра Общей Химической Технологии
Курсовая работа
«Производство серной кислоты»
вариант №4
выполнила: Дьячкова Т.В.
гр. О-42
проверила: Сучкова Е.А.
Москва 2005
Задание:
- производительность по 100%-ной серной кислоте, GH2SO4, т/сут: 1400
- состав колчедана (концентрации, массовые %):
- серы CS: 42
- влаги Cвл: 5.0
- состав огарка: (концентрации, массовые %):
- серы CS(ог): 1,0
- состав обжигового газа (концентрации, объемные %):
- СSO2: 14,0
- СSO3: 0,12
- степень использования серы в колчедане, β (%): 85,8
- относительная влажность воздуха (%): 52,0
- температура кипящего слоя (К): 1103
- концентрация СSO2 в газе перед контактным аппаратом (объемные %): 8,5
- конструкция контактного аппарата:
контактный аппарат с вводом холодного газа после второго слоя
Расчетная часть:
-
Расчет материального баланса печи кипящего слоя в процессе обжига колчедана.
-
Рассчитываем общее содержание серы в колчедане:
GS
=
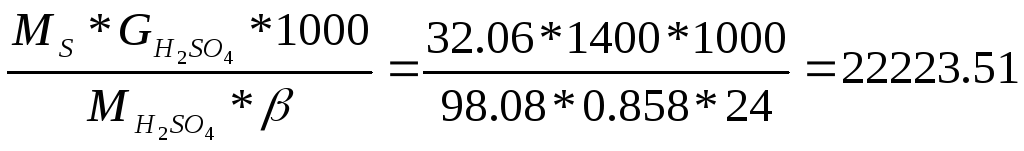 кг/ч;
кг/ч;
-
Количество сухого колчедана:
![]() кг/ч;
кг/ч;
-
Количество влаги в колчедане:
![]() кг/ч;
кг/ч;
-
Количество огарка:
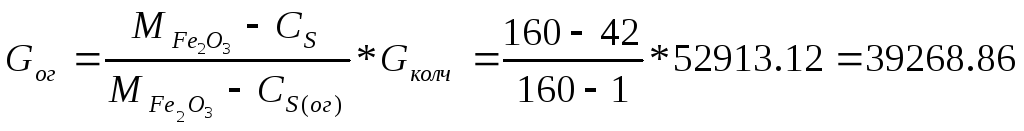 кг/ч;
кг/ч;
-
Количество серы в огарке:
![]() кг/ч;
кг/ч;
-
Потери серы с огарком:
![]() %;
%;
-
Количество выгоревшей серы:
![]() кг/ч;
кг/ч;
-
Общее количество SO2 и SO3 :
![]() м3/ч;
м3/ч;
-
Объем SO2 :
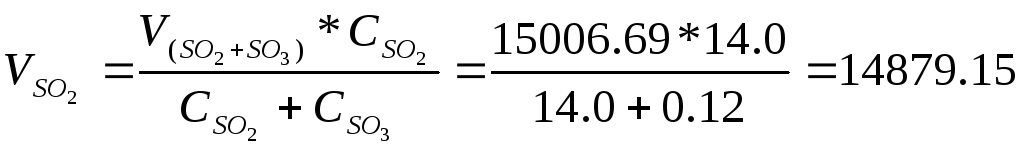 м3/ч;
м3/ч;
-
Объем SO3 :
![]() м3/ч;
м3/ч;
-
Концентрация кислорода в обжиговом газе определяется по формуле:
![]() ,
где n
– содержание кислорода в воздухе, n=21%;
m
– стехиометрическое отношение числа
молекул кислорода к числу молекул SO2,
по балансовому уравнению:
,
где n
– содержание кислорода в воздухе, n=21%;
m
– стехиометрическое отношение числа
молекул кислорода к числу молекул SO2,
по балансовому уравнению:
4
FeS2
+
11 O2
= 8 SO2
+
2 Fe2O3,
![]() ;
;
![]() %;
%;
-
Объем сухого обжигового газа:
 м3/ч;
м3/ч;
-
Объем кислорода в обжиговом газе:
![]() м3/ч;
м3/ч;
-
Объем азота в обжиговом газе:
![]() м3/ч;
м3/ч;
-
Объем сухого воздуха, поступающего на обжиг колчедана (воздух содержит 79% азота):
 м3/ч;
м3/ч;
1.16. Объем паров
воды в воздухе (при 20ºС и относительной
влажности воздуха φ=52% давление паров
воды в нем равно
![]() 9,5
мм.рт.ст.= 1263,5*10-6
МПа ):
9,5
мм.рт.ст.= 1263,5*10-6
МПа ):
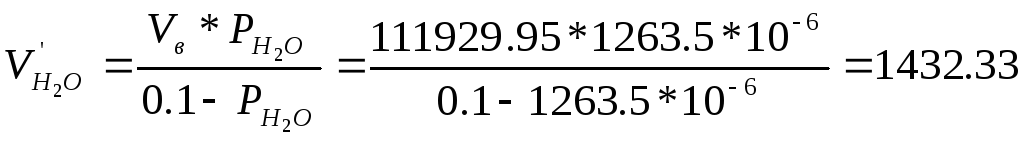 м3/ч;
м3/ч;
Общий объем паров воды в обжиговом газе:
![]() м3/ч;
м3/ч;
-
Расчет плотностей газов:
![]() ;
;
![]() кг/м3;
кг/м3;
![]() кг/м3;
кг/м3;
![]() кг/м3;
кг/м3;
![]() кг/м3;
кг/м3;
![]() кг/м3;
кг/м3;
![]() кг/м3;
кг/м3;
1.17. Материальный баланс:
|
Приход |
Количество |
Расход |
Количество |
||
|
кг/ч |
м3/ч |
кг/ч |
м3/ч |
||
|
Колчедан |
52913,12 |
- |
Огарок |
39268,86 |
- |
|
Обжиговый газ, в т.ч.: |
|
111177,62 |
|||
|
Влага колчедана |
2784,90 |
- |
SO2 |
42509,73 |
14879,15 |
|
Сухой воздух |
144725,43 |
111929,95 |
SO3 |
455,45 |
127,54 |
|
O2 |
4067,36 |
2848,29 |
|||
|
N2 |
110530,83 |
88424,66 |
|||
|
Влага с воздухом |
1151,59 |
1432,33 |
H2O |
3937,98 |
4897,98 |
|
Всего: |
201575,04 |
|
Всего: |
200770,21 |
|
![]()
2. Расчет теплового баланса печи обжига колчедана.
-
Тепло сухого колчедана:
![]() кДж/ч;
кДж/ч;
(Ср(колч)=0,5447 кДж/кг*град – [1]);
-
Тепло влаги колчедана:
(Ср(воды)=4,19
кДж/кг*град – [1]);
![]() кДж/ч;
кДж/ч;
-
Тепло сухого воздуха:
(Ср(возд)=1,3012
кДж/кг*град – [1]);
![]() кДж/ч;
кДж/ч;
-
Тепло влаги воздуха:
(Ср(вод.пара)=1,4934
кДж/кг*град – [1], при 20ºС);
![]() кДж/ч;
кДж/ч;
-
Тепло горения колчедана:
4FeS2 + 11 O2 = 8 SO2 + 2 Fe2O3 + 3415.7 кДж/моль;
Теплота сгорания химически чистого FeS2:
![]() кДж/ч;
кДж/ч;
Количество тепла, выделяющегося при горении колчедана, зависит от степени выгорания серы (содержание серы в FeS2 равно 53,5%):
![]() кДж/ч;
кДж/ч;
Выход огарка:
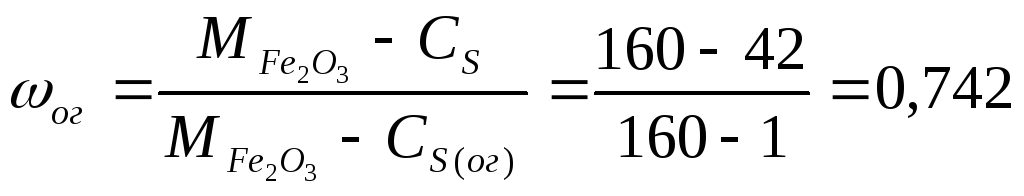 ;
;
Степень выгорания серы:
![]() %;
%;
![]() кДж/ч;
кДж/ч;
-
Приход тепла (кДж/ч):
![]()
![]()
2.7. Тепло огарка: (Ср(ог)=0,7961 кДж/кг*град – [1]);
![]() кДж/ч;
кДж/ч;
-
Тепло обжигового газа:
(Ср(об.г.)=1,4246 кДж/м3*град – [1]);
![]() кДж/ч;
кДж/ч;
-
Теплоотдача печи в окружающую среду:
![]() кДж/ч;
кДж/ч;
-
Расход тепла:
![]() кДж/ч;
кДж/ч;
-
Тепло, затраченное на испарение воды и получение пара:
![]() кДж/ч;
кДж/ч;
-
Тепловой баланс печи:
|
Приход |
Количество |
Расход |
Количество |
||
|
кДж/ч |
% |
кДж/ч |
% |
||
|
Тепло сухого колчедана |
576435,53 |
|
Тепло огарка |
25947409,74 |
|
|
Тепло влаги колчедана |
233374,62 |
|
Тепло обжигового газа |
131458419,09 |
|
|
Тепло сухого воздуха |
3766334,59 |
|
Тепло потери |
1265976,52 |
|
|
Тепло влаги воздуха |
34395,69 |
|
Тепло на получение пара в кипящем слое |
|
|
|
Тепло горения колчедана |
121987111,98 |
|
|||
|
Всего |
126597652,41 |
100 |
Всего |
|
100 |
ХЗ
Состав обжигового газа после обжига серосодержащего сырья в атмосфере воздуха (расчет по данным из таблицы материального баланса):
![]()
|
Состав |
%, объемн. |
%, объемн, перед конт. апп. |
|
SO2 |
13.4 |
8,5 |
|
SO3 |
0.1 |
|
|
H2O |
4.4 |
|
|
O2 |
2.6 |
|
|
N2 |
79.5 |
|
Перед подачей в реактор газ подвергается осушке и очистке от SO3, а также дополнительно разбавляется воздухом до содержания SO2 = 8,5% (объемных).
Состав реакционной массы перед контактным аппаратом (объемные %):
 %;
%;
Коэффициент разбавления:
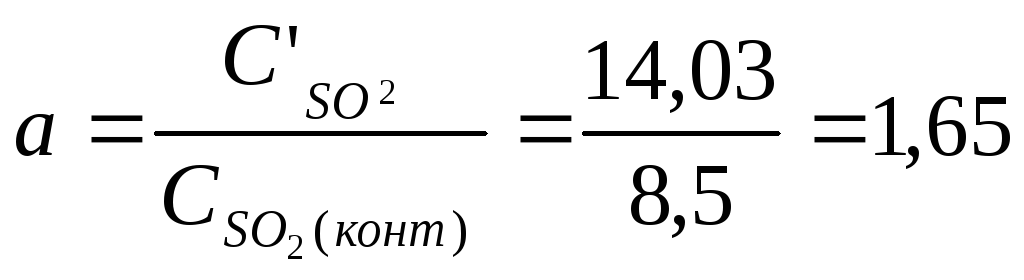
В контактном аппарате протекают реакции:
SO2 + 0.5 O2 = SO3
SO3 + H2O = H2SO4;
Соотношение
![]() ;
;
Расчет количества SO2 для получения заданной производительности по кислоте:
22,4 м3 SO2 - 98 кг H2SO4
VSO2, м3 - GH2SO4 = 1400*1000/24=58333,33 кг/ч;
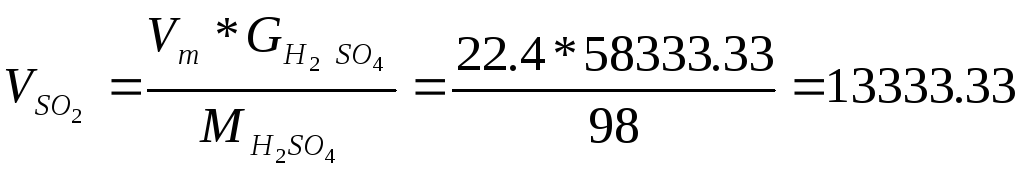 м3/ч
=
м3/ч
=
![]() =
3,7 м3/сек;
=
3,7 м3/сек;
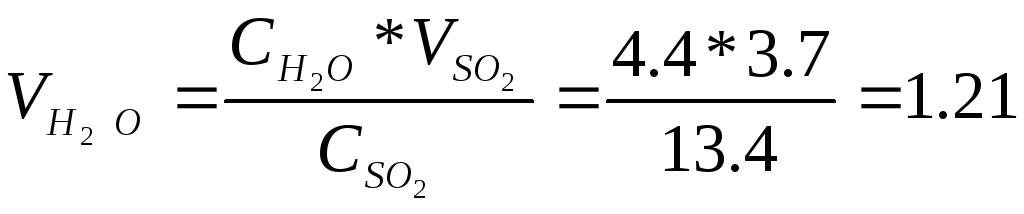 м3/сек;
м3/сек;
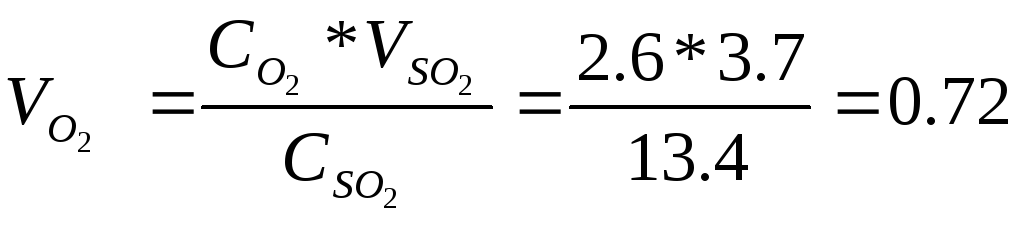 м3/сек;
м3/сек;
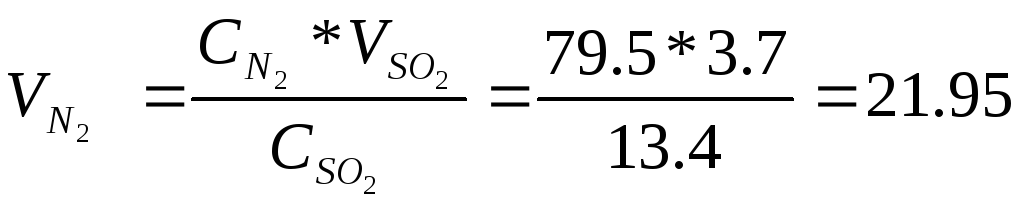 м3/сек;
м3/сек;
После очистки:
![]() м3/сек;
м3/сек;
После разбавления:
![]() м3/сек;
м3/сек;
Общий объем кислорода и азота:
![]() м3/сек;
м3/сек;
Объем кислорода:
![]() м3/сек;
м3/сек;
Объем азота:
![]() м3/сек;
м3/сек;
Концентрации (об.%) газов на входе в контактный аппарат:
![]() %;
%;
![]() %;
%;
![]() %;
%;
Проверка:
![]() %;
%;
