
- •Тема 1. Фізичні основи молекулярно – кінетичної теорії
- •14. Поняття про статистичні і термодинамічні методи досліджень
- •15. Ідеальний газ. Мікроскопічні параметри газу
- •Концентрація газу n (ф.В.)
- •16. Термодинамічні параметри. Основне рівняння молекулярно-кінетичної теорії ідеального газу. Середня кінетична енергія молекул
- •17. Молекулярно-кінетичне тлумачення абсолютної температури. Постійна Больцмана. Шкала Цельсія. Шкала Цельсія.
- •18. Рівняння Клапейрона-Менделєєва. Універсальна газова стала. Закон Дальтона
Тема 1. Фізичні основи молекулярно – кінетичної теорії
14. Поняття про статистичні і термодинамічні методи досліджень
Відправним пунктом молекулярної фізики є висновок про те, що властивості і явища які безпосередньо спостерігаються людиною (тиск газу, нагрівання та теплове розширення тіл, процеси випаровування, тощо) являють собою усереднений результат руху і взаємодії, величезної кількості атомів і молекул. Цей рух і взаємодія молекул підкоряються законам статистики тому метод що використовується для пояснення явищ і властивостей тіл з точки зору молекулярної будови речовини (молекулярно-кінетичний метод), є статистичним методом, що базується на математичній теорії ймовірностей.
Основою МКТ є вчення про дискретність речовини, тобто, усі тіла складаються з дрібних частинок – молекул, між якими існують проміжки.
Молекула - це найдрібніша частинка речовини, що зберігає її хімічні властивості.
Молекули складаються з атомів.
|
Основні положення МКТ |
Докази справедливості основних положень МКТ |
|
1. Існують фотографії молекул. |
|
2. Існування явища дифузії і Броунівського руху. Осмос – це дифузія речовини крізь стінки посуди. |
|
3. Якби не було сил взаємодії, то не існувало б твердих і рідких тіл |
Поряд з молекулярно-кінетичним методом, використається й інший метод вивчення явищ, на основі закону збереження енергії, його називають термодинамічним методом.
Розділ фізики, у якому різні процеси й властивості тіл розглядаються з енергетичної точки зору, називається термодинамікою.
Таким чином, макросистема1може бути досліджена як методами молекулярно-кінетичної теорії, так і методами термодинаміки. У термодинаміці макросистему називають термодинамічною системою.
У сучасній фізиці молекулярно-кінетична теорія і термодинаміка поєднуються в єдину наукову дисципліну - молекулярну фізику методи якої використаються в усіх розділах фізики.
15. Ідеальний газ. Мікроскопічні параметри газу
Ідеальний газ
* Ідеальний газ - це газ, енергією взаємодії між молекулами якого можна знехтувати.
Ідеальний газ - це модель газу, його можна розглядати як абсолютно пружні матеріальні точки, що рухаються хаотично.
* Мікроскопічні параметри газу - це параметри, які описують стан окремих молекул газу.
До
них відносять: m0-
масу молекули;
 -
середню квадратичну швидкість молекул;
-
середню квадратичну швидкість молекул; -
середню кінетичну енергію поступального
руху молекул;n
- концентрацію.
-
середню кінетичну енергію поступального
руху молекул;n
- концентрацію.
Середня
квадратична швидкість молекул
 (ф.в.)
(ф.в.)
1. Середня квадратична швидкість молекул - це мікроскопічний параметр газу.
2. Визначення. Середня квадратична швидкість молекул - це фізична величина, яка чисельно дорівнює квадратному кореню з відношення суми квадратів швидкостей всіх молекул газу до кількості всіх молекул даного газу.
3. Середня квадратична швидкість молекул - це скалярна величина.
4.
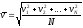
5.
[ ]
= м/с.
]
= м/с.
Середня
кінетична енергія поступального руху
молекул
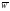 (ф.в.)
(ф.в.)
1. Середня кінетична енергія поступального руху молекул - це мікроскопічний параметр газу.
2. Визначення. Середня кінетична енергія поступального руху молекул - це фізична величина, яка чисельно дорівнює півдобутку маси молекули на квадрат середньої квадратичної швидкості молекули.
3. Середня кінетична енергія поступального руху молекул - це скалярна величина.
4.
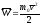
5. [W]=Дж.
