
Otvety
.docxБилет № 1
1)Термодинамика — это отрасль физики, изучающая законы преобразования энергии и процессы перехода ее из одних форм в другие. Рабочее тело— в термодинамике условное несменяемое материальное тело, расширяющееся при подводе к нему теплоты и сжимающееся при охлаждении и выполняющее работу по перемещению рабочего органа тепловой машины. В теоретических разработках рабочее тело обычно обладает свойствами идеального газа. На практике рабочим телом тепловых двигателей являются продукты сгорания углеводородного топлива или водяной пар, имеющие высокие термодинамические параметры (начальные: температура, давление, скорость и т. д.) В холодильных машинах в качестве рабочего тела используются аммиак, гелий, водород, азот. Рабочее тело и параметры его состояния. Работа тепловых машин осуществляется с использованием рабочих веществ — теплоносителей, которые называются рабочими телами. В качестве рабочих тел используются, как правило, вещества в газообразном (парообразном) состоянии. Газы и пары под воздействием внешних условий (температуры и давления) допускают значительные изменения своего объема и поэтому могут совершать при расширении или сжатии существенно большую работу, чем жидкие и твердые тела, которые практически несжимаемы. Если рабочее тело будет находиться в среде, имеющей постоянные давление и температуру, то по истечении достаточного времени в рабочем теле по всему его объему установятся такие же по величине давление и температура. В дальнейшем состояние рабочего тела будет неизменным, пока не изменятся параметры внешней среды. Рабочее тело в этом случае находится в термодинамическом равновесии с окружающей его средой. При неравновесном состоянии параметры рабочего тела по объему неодинаковы и нельзя говорить в целом об его давлении и температуре. Таким образом, физическое состояние рабочего тела в термодинамическом равновесии определяется тремя термодинамическими параметрами состояния: температурой, давлением и удельным объемом (или плотностью). Необходимо отметить, что такими параметрами являются не просто температура и давление, а именно абсолютные их величины.
2)Передача теплоты теплопроводностью через плоскую однослойную стенку. Рассмотрим наиболее распространённый случай, длина и ширина кот.бесконечно велики по сравнению с толщиной б(далее рисунок, отдельно). Стенка имеет во всех своих частях одинаковую толщину, при чём температуры поверхности t´ст и t´´ст поддерживаются постоянными, явл.изотермными поверхностями. Температура меняется только в направлении, перпендикулярном к плоскости стенки, кот.принимаем за ось x. Коэффициент теплопроводности λ постоянен для всей стенки. При стационарном тепловом режиме температура в любой точке тела неизменна и не зависит от времени .
Закон Фурье
Согласно
гипотезе Фурье, количество теплоты
d2Qt,
проходящее через элемент изотермической
поверхности dF
за промежуток времени dt,
пропорционально температурному
градиенту
![]() :
:![]() Здесь
множитель l
называется коэффициентом теплопроводности.
Знак минус указывает на то, что теплота
передается в направлении уменьшения
температуры. Количество теплоты,
прошедшее в единицу времени через
единицу изотермической поверхности,
называется плотностью теплового
потока:
Здесь
множитель l
называется коэффициентом теплопроводности.
Знак минус указывает на то, что теплота
передается в направлении уменьшения
температуры. Количество теплоты,
прошедшее в единицу времени через
единицу изотермической поверхности,
называется плотностью теплового
потока:![]() Проекции
вектора q
на координатные оси соответственно:
Проекции
вектора q
на координатные оси соответственно:
![]() ;
;
![]() ;
;
![]() Уравнения (9.4) и (9.5) являются математическим
выражением основного закона
теплопроводности — закона
Фурье.
Уравнения (9.4) и (9.5) являются математическим
выражением основного закона
теплопроводности — закона
Фурье.
Количество
теплоты, проходящее в единицу времени
через изотермическую поверхность F,
называется тепловым потоком:![]() Полное
количество теплоты, прошедшее через
эту поверхность за время t,
определится из уравнения
Полное
количество теплоты, прошедшее через
эту поверхность за время t,
определится из уравнения
![]() .
.
Билет № 2
1)Идеальный
газ- это вещество, у кот. отсутствуют
силы взаимодействия между его частицами,
а сами частицы не имеют объема, хотя
они материальны. Английский учёный
Бойль и француз Мариотт, Шарль и
Гей-Люссак, считали, что реальные газы
подчиняются их законам, однако в
последствии оказалось, что только при
относительно высоких температур и
низких давлениях это различие во
внимание не принимаются. Поэтому рабочие
тела находятся в таких условиях
рассматриваются в термодинамике как
идеальные газы. При низкой температуре
и высоких давлениях это же реальные
газы по своим свойствам значительно
отличаются от идеальных газов и поэтому
не могут рассматриваться как идеальные.
Следовательно один и тот же газ в
зависимости от условий, в которых он
находится, может рассматриваться как
идеальный или как реальный. Рабочим
телом наз.вещество используемое для
преобразования теплоты в работу. Газовые
Законы: закон Бойля-Мариотта устанавливает
зависимость удельного объема идеального
газа от его давления при постоянной
температуре. При постоянной температуре
удельные объемы газа обратно
пропорциональны его давления.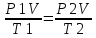 при T=const
Закон Б-Мориотта P1V1=P2V2
;
при T=const
Закон Б-Мориотта P1V1=P2V2
;
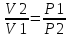 .
Закон Гей-Люссака устанавливает
зависимость удельного объема идеального
газа от его температуры. P=const
.
Закон Гей-Люссака устанавливает
зависимость удельного объема идеального
газа от его температуры. P=const
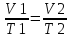 ;
;
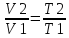 При постоянном давлении удельные
объемы идеального газа прямопропорционально
его абсолютным температурам. Закон
Шарля: устанавливает зависимость
идеального газа от его температуры при
постоянном объеме.
При постоянном давлении удельные
объемы идеального газа прямопропорционально
его абсолютным температурам. Закон
Шарля: устанавливает зависимость
идеального газа от его температуры при
постоянном объеме.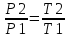 .
Уравнение состояния идеального газа:
.
Уравнение состояния идеального газа:
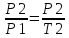
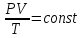
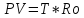 Ro-
удельная газовая постоянная;
Ro-
удельная газовая постоянная;
V=V
*m
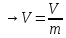
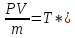 Ro
Pv=m
Ro
T;
R-
универсальная газовая постоянная.
Ro
Pv=m
Ro
T;
R-
универсальная газовая постоянная.
2)Конвективный
теплообмен и теплообмен излучением
обособлены, независимо друг от друга,
однако в практических условиях они
обычно действуют совместно, и такой
теплообмен называется радиационно-конвективным.
В радиационно-конвективном теплообмене
основным может быть теплообмен
излучением, тогда конвективный теплообмен
явл. сопутствующим. Расчёт такого
радиационно-конвективного теплообмена
производится по уравнению Ньютона-Рихмана
с заменой в нем коэффициента теплоотдачи
а коэффициентом а₀, которым учитывается
излучением усиление конвективного
теплообмена. Таким образом: Ф=а₀S(tr-tст),
где Ф- тепловой поток в радиационно-конвективном
теплообмене, Вт; а₀- коэффициент
теплоотдачи с учетом теплообмена
излучением Вт/м2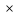 K;
tст-
температура газа и стенки, °C;
K;
tст-
температура газа и стенки, °C;
Билет № 3
1)КЛАПЕЙРОНА-МЕНДЕЛЕЕВА УРАВНЕНИЕ-это уравнение состояния идеального газа с учётом молярной массы.
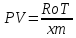
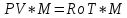
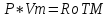
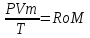
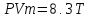
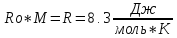
КЛАПЕЙРОНА-МЕНДЕЛЕЕВА УРАВНЕНИЕ, ур-ние состояния идеального газа, устанавливающее связь между его объемом V. давлением р и абс. т-рой Т. Имеет вид: pV=nRT. где п - число молей газа R = 8,31431 Дж/моль .К) - газовая постоянная. Для 1 моля газа pv=RT, где v-молярный объем. Клапейрона - Менделеева уравнение записывают также в форме: pV=NkT, где N - число частиц газа в объеме V, k - постоянная Болыгмана. Если М - масса газа, а m - его мол. масса, то pV=(M/m)RT. Клапейрона - Менделеева уравнение приближенно выполняется для реальных газов при достаточно низких давлениях; с повышением т-ры область давлений, при к-рых состояние реального газа можно описывать Клапейрона - Менделеева уравнением, расширяется. Для молекулярных газов (напр., атм. воздуха) при обычных т-рах и давлениях до 1,01.105 Па (1 атм) Клапейрона - Менделеева уравнение выполняется достаточно точно. Клапейрона - Менделеева уравнение широко используют при расчетах термодинамич. св-в газов, определения работы, совершаемой системой в к.-л. процессе. Ассоциированные газы, напр. пары НСООН, СН3СООН, С3Н7СООН и др. карбоновых к-т, не подчиняются Клапейрона - Менделеева уравнению даже при очень низких давлениях. Ур-ние было установлено опытным путем Б. П. Э. Клапейроном в 1834; оно имело вид: pV=ВТ, где В - постоянная, зависящая от природы газа и его массы. В совр. виде ур-ние было получено в 1874 для 1 моля идеального газа Д. И. Менделеевым в результате объединения законов Гей - Люссака, Бойля-Мариотта и Авогадро. Вывод Клапейрона - Менделеева уравнения возможен на основании представлений молекулярно-кинетич. теории газов.
Универсальная газовая постоянная:
 , где R₀-
удельная газовая постоянная; R-
универсальная газовая постоянная; M-
молекулярная масса.
, где R₀-
удельная газовая постоянная; R-
универсальная газовая постоянная; M-
молекулярная масса.
2)ТЕПЛОВАЯ ИЗОЛЯЦИЯ. Теплоизоляция – это защита зданий, промышленных установок (или отдельных их узлов) от нежелательного теплового обмена с окружающей средой. Так, например, в строительстве и теплоэнергетике теплоизоляция необходима для уменьшения тепловых потерь в окружающую среду, в холодильной и криогенной технике – для защиты аппаратуры от притока тепла извне. Теплоизоляция обеспечивается устройством специальных заграждений, выполняемых из теплоизоляционных материалов (в виде оболочек, покрытий и т.п.) и затрудняющих теплопередачу; сами эти теплозащитные средства также называются теплоизоляцией. При преимущественно конвективном теплообмене для теплоизоляции используются ограждения, содержащие слои материала, непроницаемого для воздуха; при лучистом теплообмене – конструкции из материалов, отражающих тепловое излучение (например из фольги, металлизированной лавсановой пленки); В тепловых промышленных установках теплоизоляция обеспечивает значительную экономию топлива, способствует увеличению мощности тепловых агрегатов и повышению их КПД, интенсификации технологических процессов, снижению расходов основных материалов. Экономическая эффективность теплоизоляции в промышленности часто оценивается коэффициентом сбережения тепла Где Q1 – потери тепла без теплоизоляции, а Q2 – с теплоизоляцией. Задача теплоизоляции зданий – снизить потери тепла в холодный период года и обеспечить постоянство температуры в помещениях в течении суток при колебаниях температуры наружного воздуха. Применяя для теплоизоляции эффективные теплоизоляционные материалы, можно существенно уменьшить толщину и снизить массу ограждающих конструкций и, т.о. сократить расход основных стройматериалов. Материалы и изделия, применяемые для теплоизоляции называются теплоизоляционными. Теплоизоляционные материалы характеризуются низкой теплопроводностью. Основной показатель качества теплоизоляторов – коэффициент теплопроводности. Он является физическим параметром вещества и в общем случае зависит от температуры, давления и рода вещества. Теплоизоляционные материалы должны отвечать следующим нормам : они должны быть температурно- и морозостойкими, негорючими или обладать возможно меньшей горючестью, химически инертными. Они недолжны иметь запаха или воспринимать запахи, обладать достаточной механической прочностью, виброустойчивыми, должны легко обрабатываться и резаться, должны удовлетворять определенным экономическим показателям.
Билет № 4
1)Теплоемкость. Теплоемкостью какого-либо тела называется физическая величина, численно равная количеству теплоты, которое нужно сообщить телу, чтобы повысить его температуру на 1 К
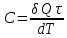
Различают
удельную
(массовую)
теплоемкость c
–
теплоемкость 1 кг
вещества,
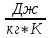 ;
молярную
теплоемкость
сμ
–
теплоемкость 1 моля
вещества,
;
молярную
теплоемкость
сμ
–
теплоемкость 1 моля
вещества,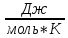 ;
объемную теплоемкость с-
теплоемкость
1 м3
вещества,
;
объемную теплоемкость с-
теплоемкость
1 м3
вещества,
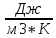
Различают
теплоемкости истинные и средние: Истиной
теплоемкостью - называют теплоемкость
при заданной t;
Среднем значением теплоемкости -
называют среднее значение теплоемкости
в заданном интервале температур, в
пределах кот. производится подвод или
отвод теплоты.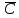 - средняя удельная теплоёмкость;
- средняя удельная теплоёмкость;
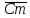 -средняя молярная теплоёмкость.
Теплоемкость является свойством
вещества. Теплоемкость газов и паров
явл.переменными величинами, для идеальных
газов они зависят от их температуры, а
для реальных газов от температуры их
и давления. Для газов теплоемкость
также зависит от процесса, при котором
осуществляется теплоотдача, при этом
выделяют изобарную
сp и
изохорную
теплоемкость сυ.
Такое разделение связано со свойством
газов сильно расширяться при нагревании,
тогда как жидкости и твердые тела
расширяются при нагревании незначительно.
Если подводить некоторое количество
теплоты к газу при постоянном объеме
(изохорный процесс), то теплота будет
затрачиваться только на приращение
внутренней энергии газа (т.е. увеличивается
только температура газа). Если подводить
некоторое количество теплоты к газу
при постоянном давлении (изобарный
процесс), то теплота не только будет
затрачиваться на приращение внутренней
энергии газа (увеличение его температуры),
но и на работу расширения (увеличение
его объема). Таким образом, для увеличение
температуры газа на 1 К
в
изобарном процессе понадобиться большее
количество теплоты, чем в изохорном.
-средняя молярная теплоёмкость.
Теплоемкость является свойством
вещества. Теплоемкость газов и паров
явл.переменными величинами, для идеальных
газов они зависят от их температуры, а
для реальных газов от температуры их
и давления. Для газов теплоемкость
также зависит от процесса, при котором
осуществляется теплоотдача, при этом
выделяют изобарную
сp и
изохорную
теплоемкость сυ.
Такое разделение связано со свойством
газов сильно расширяться при нагревании,
тогда как жидкости и твердые тела
расширяются при нагревании незначительно.
Если подводить некоторое количество
теплоты к газу при постоянном объеме
(изохорный процесс), то теплота будет
затрачиваться только на приращение
внутренней энергии газа (т.е. увеличивается
только температура газа). Если подводить
некоторое количество теплоты к газу
при постоянном давлении (изобарный
процесс), то теплота не только будет
затрачиваться на приращение внутренней
энергии газа (увеличение его температуры),
но и на работу расширения (увеличение
его объема). Таким образом, для увеличение
температуры газа на 1 К
в
изобарном процессе понадобиться большее
количество теплоты, чем в изохорном.
Разница между сp и сυ отражена формулой Майера:
сμ p − cμυ = Rμ ; сp − cυ = R . (7.9)
Также
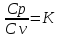
где k – показатель адиабаты. Теплоемкость идеального газа можно вычислить теоретическим путем, применяя методы статистической физики. При этом вычисление теплоемкости сводится к вычислению средней энергии теплового движения отдельных молекул газа, которое складывается из поступательного и вращательного движения молекулы как целого и колебательного движения атомов внутри молекулы.
2) Влажность воздуха – физическая величина, характеризующая содержание в воздухе водяного пара. Влажность воздуха (относительная влажность воздуха) – это отношение парциального давления водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного пара при той же температуре, выраженное в процентах. Относительная влажность воздуха показывает, насколько водяной пар в данных условиях близок к насыщению. Именно от этого зависит интенсивность испарения воды и потеря влаги живыми организмами. Для человека наиболее благоприятна относительная влажность 40–60%. Смесь сухого воздуха (не содержащих молекул воды) с водяным паром называется влажным воздухом. Влажный воздух широко используется в технике. По своему физическому состоянию он близок к идеальным газам. Влажность воздуха при данном давлении и температуре может содержать разное кол-во водяного пара. Смесь, состоящую из сухого воздуха и насыщенного водяного пара, называют насыщенным влажным воздухом. ВЛАЖНОСТЬ ВОЗДУХА - содержание в воздухе водяного пара. Его гл. источники - испарение с поверхности океанов, морей, водоёмов, влажной почвы и растений. Образовавшийся водяной пар переносится вверх турбулентностью и конвекцией, а по горизонтали - ветром. Под влиянием разл. процессов водяной пар конденсируется, образуя туманы, облака, осадки и наземные гидрометеоры: росу, иней и т. д. В. в. измеряется гигрометрами и психрометрами. Интенсивно развиваются дистанц. методы определения В. в. (в т. ч. с борта самолётов и метеорологич. ИСЗ) лазерными и радиометрич. приборами. Отношение действительной, абсолютной влажности не насыщенного воздуха к максимально возможной абсолютной влажности воздуха при той же температуре называют относительной влажностью и обозначают буквой ϕ.
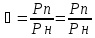
где
Рп –
парциальное
давление водяного пара во влажном
воздухе; Рн –
максимально
возможное парциальное давление водяного
пара
при
данной температуре.
Относительная
влажность обычно выражается в процентах
и изменяется в
пределах
0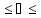 100%.
Для сухого воздуха ϕ=0,
для насыщенного
ϕ=100%.
Для определения содержания пара во
влажном воздухе помимо
относительной
влажности ϕ
необходимо
знать температуру влажного
воздуха,
по которой из паровых таблиц определяется
давление насыщенного
100%.
Для сухого воздуха ϕ=0,
для насыщенного
ϕ=100%.
Для определения содержания пара во
влажном воздухе помимо
относительной
влажности ϕ
необходимо
знать температуру влажного
воздуха,
по которой из паровых таблиц определяется
давление насыщенного
пара Рн .
Билет № 5
1)Основные термодинамические параметры состояния p,v и T однородного тела зависят один от другого и взаимно связаны определенным математическим уравнением вида: F(p,v,T)=0,Которое в термодинамике называют уравнением состояния. Если известно уравнение состояния, то для определения состояния простейших систем- однородных и постоянных по времени, по массе и по составу достаточно знать две независимые переменные из чисел трёх: p=f1(v;T); v=f2(p,T); T=f3(v;p) Если внешние условия, в которых находятся термодинамическая система, изменяются, то будет изменяться и состояние системы. Совокупность изменений состояния термодинамической системы при переходе из одного равновесного состояния в другое называют термодинамическим процессом. Под равновесном состоянием тела понимают такое, при котором во всех точках его объема давление, температура, удельный объем и все другие физические свойства одинаковы. Процесс изменения состояния системы может быть равновесным и неравновесным. Если процесс, протекая, проходит через равновесные состояния, то его называют равновесным. Только равновесные состояния могут быть описаны количественно с помощью уравнения состояния. Равновесный процесс можно осуществить при бесконечно медленном изменении внешних условий или когда изменение параметров, характ. Состояние системы, бесконечно малы по сравнению со значениями самих параметров. Неравновесность реальных процессов определятся прежде всего тем, что под влиянием внешних условий они протекают с конечными скоростями и в рабочем теле не успевает устанавливаться равновесие состояния(графическое изображение). Особое значения в термодинамических процессах представляют замкнутые или круговые, процессы, при которых система, проходя через ряд последовательных состояний, возвращаются в начальное состояние. Круговой процесс так же называется циклом.
2)Докретический
режим истечения можно получить если
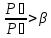 .
К суживающему соплу добавить расширяющуюся
часть. В этом случае давление потока в
min
сечении = Pk,
а давление в max
сечение можно довести до давления P₀.
Такая насадка была предложена Лавалем
(рисунок). Правильно рассчитано сопло
Лаваля дают возможность осуществить
полное расширение рабочего тела до
давления наружной среды и получить
сверхзвуковую скорость. Массовый
расход, как и в критическом режиме
истечения =mtmax
, max
расход определяет площадью сечения
Smin.
В min
сечении должна установлена критическая
скорость истечения и max
массовый расдох. Зная, что при
установившимся постоянном процессе
истечения массовый расход через min
сечение должны равняться массовому
расходу через выходное сечение.
.
К суживающему соплу добавить расширяющуюся
часть. В этом случае давление потока в
min
сечении = Pk,
а давление в max
сечение можно довести до давления P₀.
Такая насадка была предложена Лавалем
(рисунок). Правильно рассчитано сопло
Лаваля дают возможность осуществить
полное расширение рабочего тела до
давления наружной среды и получить
сверхзвуковую скорость. Массовый
расход, как и в критическом режиме
истечения =mtmax
, max
расход определяет площадью сечения
Smin.
В min
сечении должна установлена критическая
скорость истечения и max
массовый расдох. Зная, что при
установившимся постоянном процессе
истечения массовый расход через min
сечение должны равняться массовому
расходу через выходное сечение.
Билет № 6
1)Внутренняя энергия. Энтальпия. Внутренняя энергия U термодинамической системы представляет собой сумму всех видов энергии движения и взаимодействия частиц, составляющих систему. Внутренняя энергия является функцией состояния термодинамической системы. Это означает, что независимо от предыстории системы ее энергия в данном состоянии имеет присущее этому состоянию значение, поэтому приращение внутренней энергии при переходе системы из одного состояния в другое всегда равно разности значений внутренней энергии в конечном и начальном состояниях независимо от пути перехода. Таким образом,
ΔU =U2 −U1 . Внутренняя энергия является величиной аддитивной, т. е. внутренняя энергия системы равна сумме внутренних энергий отдельных ее частей. Под энтальпией понимают энергию расширенной системы состоящей из макротела (газа) и поршня с грузом, уравновешивающего давление газа внутри сосуда, куда заключен газ. При этом энтальпия равна сумме внутренней энергии системы и потенциальной энергии поршня с грузом
H =U + pV . Энтальпия также является функцией состояния и обладает свойством аддитивности. Единицей измерения внутренней энергии и энтальпии является 1 Дж. В термодинамике также используются удельные величины внутренней энергии u, Дж/кг и энтальпии h, Дж/кг (внутренняя энергия и энтальпия для массы системы равной 1 кг). Работа. Теплота. В термодинамике рассматриваются два способа передачи энергии: по средствам совершения работы и передачи некоторого количества теплоты. Работа L и количество теплоты Qτ являются функциями процесса, т. е. их значение будет зависеть от пути перехода (термодинамического процесса). Элементарная работа, совершаемая газом определяется формулой вида δL = pdV Элементарное количество теплоты определяется формулой вида δQτ = cmdT ; где с – удельная (массовая) теплоемкость тела, Также количество теплоты выражается формулой вида δQτ = TdS . где S – энтропия термодинамической системы, Дж/К. Энтропия термодинамической системы является функцией состояния системы и с точки зрения статистической физики служит мерой порядка в системе. Единицей измерения работы и количества теплоты является 1 Дж. В термодинамике также используются удельные величины работы l, Дж/кг и количества теплоты q, Дж/кг (работа и количество теплоты для массы системы равной 1 кг).
2)Если в трубопроводе имеется резкое сжатие(вентиль, кран), то при проходе через это сужение давление понижается, а удельный объем увеличивается. Такой не обратимый процесс расширения потока называют дросселирование.
Рисунок (отдельно нарисованный)
На рисунке поток проходит через узкое отверстие в диафрагме F , установленной в трубопроводе. При этом если до диафрагмы давление было P1, то после оно стало равным P2. Оба эти давления должны измеряться на некотором расстоянии а,в от диафрагмы где давления одинаковы по всему поперечному сечению трубопровода.
Билет № 7
1) Первое начало термодинамики для закрытой системы формулируется следующим образом: количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы против внешних сил. -Изменение внутренней энергии равно сумме кол-во теплоты и работы, совершаемой внешними силами над рабочим телом при его сжатии.
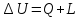 изменение
внутренней энергии, изменяется в Дж;
Q-кол-во
теплоты переданная система; L-
работа совершаемая над рабочим телом
при его сжатии изменяется в Дж; ∆𝒰=q+ℓ
. Первый закон термодинамики для удельных
величин. Первый закон термодинамики
явл. частным случаем всеобщего закона
сохранения и превращения энергии,
утверждает, что теплота может превращаться
в работу, а работу в теплоту, не
устанавливая условий, при кот. возможны
эти превращения. Он совершенно не
рассматривает вопроса о направлении
теплового процесса, а не зная этого
направления, нельзя предсказать его
характер и результаты. Первый закон не
решает вопрос о том, будет ли совершаться
переход теплоты от нагретого тела к
холодному или обратно. Опыты показывают,
что теплота сама собой может переходить
только от нагретых тел к более холодным.
Передача теплоты от нагретого тела к
среде будет происходить до полного
температурного равновесия с окружающей
средой. Только за счёт работы можно
изменить направления движения теплоты.
Работа, как и все другие виды энергии,
участвующие в каком-либо процессе,
легко и полностью превращаются в
теплоту. Процессы превращения работы
в теплоту происходят в природе непрерывно
: трение, удар, торможении.
изменение
внутренней энергии, изменяется в Дж;
Q-кол-во
теплоты переданная система; L-
работа совершаемая над рабочим телом
при его сжатии изменяется в Дж; ∆𝒰=q+ℓ
. Первый закон термодинамики для удельных
величин. Первый закон термодинамики
явл. частным случаем всеобщего закона
сохранения и превращения энергии,
утверждает, что теплота может превращаться
в работу, а работу в теплоту, не
устанавливая условий, при кот. возможны
эти превращения. Он совершенно не
рассматривает вопроса о направлении
теплового процесса, а не зная этого
направления, нельзя предсказать его
характер и результаты. Первый закон не
решает вопрос о том, будет ли совершаться
переход теплоты от нагретого тела к
холодному или обратно. Опыты показывают,
что теплота сама собой может переходить
только от нагретых тел к более холодным.
Передача теплоты от нагретого тела к
среде будет происходить до полного
температурного равновесия с окружающей
средой. Только за счёт работы можно
изменить направления движения теплоты.
Работа, как и все другие виды энергии,
участвующие в каком-либо процессе,
легко и полностью превращаются в
теплоту. Процессы превращения работы
в теплоту происходят в природе непрерывно
: трение, удар, торможении.
2)
Конвективный
теплообмен – одновременный перенос
теплоты конвекции и теплопроводности.
Конвекция - это передача тепла за счёт
движения молекул жидкости или газа.
Передача
теплоты конвекцией осуществляется
перемещением в пространстве неравномерно
нагретых объемов жидкости или газов.
В дальнейшем изложении обе среды
объединены одним наименованием —
жидкость. Обычно при инженерных расчетах
определяется конвективный теплообмен
между жидкостью и твердой стенкой,
называемый теплоотдачей. Согласно
закону Ньютона—Рихмана, тепловой поток
Q
от стенки к жидкости пропорционален
поверхности теплообмена и разности
температур между температурой твердой
стенки tc
и температурой жидкости tж:
![]() .
где
α – коэффициент теплоотдачи, Вт/(м2⋅К);
Tс–
температура поверхности тела (в
дальнейшем – стенки), °С; Tж–
температура жидкости, °С; F
–
площадь поверхности теплообмена,
м2.Коэффициент
теплоотдачи α численно равен теплоте,
отданной в едини-цу времени с единичной
поверхности тела при нагреве жидкости,
омывающей поверхность на один Кельвин.
Главная
трудность расчета заключается в
определении коэффициента теплоотдачи
a,
зависящего от ряда факторов: физических
свойств омывающей поверхность жидкости
(плотности, вязкости, теплоемкости,
теплопроводности), формы и размеров
поверхности, природы возникновения
движения среды, скорости движения. По
природе возникновения различают
два вида движения — свободное и
вынужденное. Свободное движение
происходит вследствие разности
плотностей нагретых и холодных
частиц жидкости, находящейся в поле
действия сил тяжести; оно называется
также естественной конвекцией и зависит
от рода жидкости, разности температур,
объема пространства, в котором
протекает процесс.
Вынужденное
движение возникает под действием
посторонних побудителей (насоса,
вентилятора, ветра). В общем случае
наряду с вынужденным движением
одновременно может развиваться и
свободное. Относительное влияние
последнего тем больше, чем больше
разность температур в отдельных точках
жидкости и чем меньше скорость
вынужденного движения.
Интенсивность
переноса теплоты зависит от режима
движения жидкости в пограничном слое.
При турбулентном пограничном слое
перенос теплоты в направлении стенки
обусловлен турбулентным перемешиванием
жидкости. Однако непосредственно у
стенки, в ламинарном подслое теплота
будет переноситься теплопроводностью.
При ламинарном пограничном слое
теплота в направлении стенки переносится
только теплопроводностью.
.
где
α – коэффициент теплоотдачи, Вт/(м2⋅К);
Tс–
температура поверхности тела (в
дальнейшем – стенки), °С; Tж–
температура жидкости, °С; F
–
площадь поверхности теплообмена,
м2.Коэффициент
теплоотдачи α численно равен теплоте,
отданной в едини-цу времени с единичной
поверхности тела при нагреве жидкости,
омывающей поверхность на один Кельвин.
Главная
трудность расчета заключается в
определении коэффициента теплоотдачи
a,
зависящего от ряда факторов: физических
свойств омывающей поверхность жидкости
(плотности, вязкости, теплоемкости,
теплопроводности), формы и размеров
поверхности, природы возникновения
движения среды, скорости движения. По
природе возникновения различают
два вида движения — свободное и
вынужденное. Свободное движение
происходит вследствие разности
плотностей нагретых и холодных
частиц жидкости, находящейся в поле
действия сил тяжести; оно называется
также естественной конвекцией и зависит
от рода жидкости, разности температур,
объема пространства, в котором
протекает процесс.
Вынужденное
движение возникает под действием
посторонних побудителей (насоса,
вентилятора, ветра). В общем случае
наряду с вынужденным движением
одновременно может развиваться и
свободное. Относительное влияние
последнего тем больше, чем больше
разность температур в отдельных точках
жидкости и чем меньше скорость
вынужденного движения.
Интенсивность
переноса теплоты зависит от режима
движения жидкости в пограничном слое.
При турбулентном пограничном слое
перенос теплоты в направлении стенки
обусловлен турбулентным перемешиванием
жидкости. Однако непосредственно у
стенки, в ламинарном подслое теплота
будет переноситься теплопроводностью.
При ламинарном пограничном слое
теплота в направлении стенки переносится
только теплопроводностью.
