
- •1 Заболевания и повреждения органов грудной клетки
- •Плевральные пункции (асс.)
- •2. Дренирование плевральной полости (асс.)
- •3. Промывание полостей абсцесса (асс.)
- •4. Межреберная спирт-новокоиновая блокада (асс.)
- •5. Вагосимпатическая блокада (асс.)
- •6. Загрудинная блокада (асс.)
- •7. Чтение рентгенограмм и бронхограмм
- •8. Знакомство с ктг органов грудной клетки
- •10. Перевязка и снятие швов (асс.)
- •11. Участие в операциях (асс.):
- •II Заболевания пищевода
- •Бужирование рубцовых структур (ретроградное)
- •Кардиодилятация
- •Чтение рентгенограмм
- •Эндоскопические методы (фгс, лапароскопия)
- •5. Участие в операциях (асс.):
- •III Заболевания органов средостения
- •Чтение рентгенограмм тмг;
- •Кт средостения;
- •3.Пункционная биопсия новообразований;
- •4.Тораковидеоскопия с пункционной биопсией;
- •5. Ассистирование на операциях:
- •IV. Артериальная патология нижних конечностей
- •1.Выявление синдрома перемежающейся хромоты.
- •2.Пальпаторное определение пульсации на магистральных сосудах (бедренной, подколенной и др.)
- •3. Дополнительные методы диагностики артериальной патологии (допплерография, ангиография и т.Д.)
- •VII. Схема обследования больного.
- •4. Аускультация магистральных сосудов
- •5. Виды ангиографии
- •6. А) аорто-бедренное протезирование
- •4. Чтение флеброграмм.
- •5. Показатели свертывающей системы крови, чтение коагулограмм.
- •6. А) венэктомия
- •VI. Ишемическая болезнь сердца
- •1.Чтение экг,
- •2.Проведение велометрии – участие
- •3. Знакомство с рентген-операционной и методом коронарографии
- •VII. Полная аv блокада
- •Чтение экг
- •Методы кардиостимуляции – ответы
- •5.Знакомство с рентген-операционной и методами исследования полостей сердца (зондированием, измерением давления и т.Д.)
- •6. Пункции перикарда (асс.)
- •7.Знакомство с методами гипотермии, искусственного кровообращения.
- •IX. Заболевания желудка
- •1. Чтение ретгенограмм: язвенная ниша, газ в брюшной полости
- •2. Определение печеночной тупости
- •3. Синдром «шум плеска»
- •4. Определение жидкости в брюшной полости
- •5. Пальпация опухоли (размеры, подвижность)
- •6. Наличие отдельных метастаз: Вирхова, Крукенберга
- •7. Фгс, лапароскопия, лапароцентез
- •Глава 10. РН-метрия в хирургической практике
- •10. 1. Обоснование методов лечения
- •10.2. Интраоперационная внутрижелудочная рН-метрия
- •10.3. Оценка результатов оперативного вмешательства
- •9. Зондирование и промывание желудка
- •10. Паранефральная блокада
- •X. Перитонит
- •1. Симптомы Щеткина-Блюмберга, Менделя
- •2. Аускультация брюшной полости (отсутствие перистальтики)
- •3. Перкуссия живота (наличие выпота, отсутствие печеночной тупости)
- •4. Ректальное и вагинальное исследование для определения Дуглас-абсцесса
- •5. Чтение рентгенограмм при поддиафрагмальном абсцессе и газе над куполом диафрагмы
- •6. Фистулография (асс.)
- •7. Участие в операциях:
- •XI. Заболевания щитовидной железы
- •1. Пальпация щитовидной железы
- •2. Симптомы тиреотоксического зоба
- •3. Чтение и трактовка узи щитовидной железы
- •4.Трактовка результатов исследования гормонов (т3, т4, ттг), иммунной системы (иммунограммы)
- •5.Ассистирование на операциях
- •XII. Заболевание печени и желчных путей
- •2. Чтение, трактовка клинических и биохимических показателей крови
- •3. Знакомство с рентгенконтрастными методами исследованиями:
- •4. Узи печени
- •5. Ктг органов брюшной полости с контрастированием
- •6. Участие в операциях:
- •Экстренные
- •Плановые
- •7. Ведение послеоперационного периода:
- •XIII. Заболевание поджелудочной железы
- •1. Симптомы: Курвуазье, Керте, Бонде, Воскресенского, Мейо-Робсона
- •3. Рхпг при механической желтухи
- •4. Участие в операциях:
- •XIV. Грыжи передней и брюшной стенки
- •1.Определение размеров грыжевых ворот
- •2.Симптом «кашлевого толчка»
- •3. Участие в операциях: (асс.)
- •4. Рассечение апоневроза наружной косой мышцы живота скальпелем и ножницами.
- •XV. Заболевания кишечника
- •1.Симптомы непроходимости кишечника (Валя, Склярова, Кивуля, Дансе, «падающей капли»,Обуховской больницы)
- •2.Чтение рентгенограмм (чаша Клойбера), контрастное исследование тонкого кишечника
- •3.Ирригоскопия.
6. А) аорто-бедренное протезирование
Аорто-бедренное шунтирование
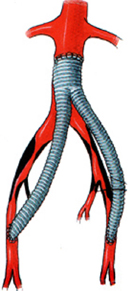 Аорто-бедренное
шунтирование - хирургическое вмешательство,
подразумевающее обход закупоренных
подвздошных артерий искусственным
сосудом с формированием соустья с
бедреными артериями в паховой области.
Односторонее аорто-бедренное шунтирование
подразумевает проведение линейного
шунта от аорты к одной бедренной артерии
(двусторонее АБШ - к двум бедренным
артериям с помощью специального Y
образного шунта). Аорто-бедренное
протезирование применяется при закупорке
(окклюзии) аорты и представляет собой
полное моделирование подвздошных
артерий.
Аорто-бедренное
шунтирование - хирургическое вмешательство,
подразумевающее обход закупоренных
подвздошных артерий искусственным
сосудом с формированием соустья с
бедреными артериями в паховой области.
Односторонее аорто-бедренное шунтирование
подразумевает проведение линейного
шунта от аорты к одной бедренной артерии
(двусторонее АБШ - к двум бедренным
артериям с помощью специального Y
образного шунта). Аорто-бедренное
протезирование применяется при закупорке
(окклюзии) аорты и представляет собой
полное моделирование подвздошных
артерий.
Показания к операции аорто-бедренного шунтирования.
АББШ - наиболее эффективный метод лечения атеросклеротических поражений подвздошных артерий (синдром Лериша). По данным многочисленных исследований, частота ампутаций у больных с синдромом Лериша составляет около 20% в год. Операции на брюшной аорте, если они выполняются по показаниям и технически безупречно, имеют небольшой риск для жизни (не более 3%) и служат 10 лет и более. Операция показана у больных без тяжелой сердечной патологии, без ожирения. Не имеющих тяжелого поражения почек и сонных артерий. Эти заболевания увеличивают риск операции и требуют предоперационной коррекции. Выполнение операции технически возможно при сохранности общей бедренной или глубокой бедренной артерии. При плохом состоянии этих сосудов необходимо дополнять аорто-бедренное шунтирование вторым этажом сосудистой реконструкции. Альтернативой АБШ является ангиопластика и стентирование подвздошных артерий, возможно использование вместо стента специального внутрисосудистого эндопротеза, что улучшает результаты эндоваскулярных операций и приближает их к шунтированию. Выбор метода сосудистой реконструкции в нашей клинике проводится совместным обсуждением сосудистого хирурга и анестезиолога, чтобы минимизировать риск для жизни пациента и добиться стойкого эффекта от операции. Как правило, открытую операцию мы предлагаем достаточно крепким, худым пациентам, с высокой ожидаемой продолжительностью жизни, с хорошим состоянием брюшной аорты, с окклюзией аорты и полной непроходимостью подвздошных артерий. При частично-проходимых подвздошных артериях мы применяем ангиопластику. У ослабленных пациентов с низким прогнозом продолжительности жизни выполняются экстраанатомические варианты шунтирования.
Предоперационная подготовка.
Подготовка больного к операции аорто-бедренного шунтирования включает в себя полноценную диагностику. В нашей клинике последовательно используются ультразвуковые методы исследования артерих нижних конечностей, ЭХО кардиография, функциональная диагностика сердца, УЗИ сонных артерий. Необходима полноценная диагностика состояния почек по анализам и с помощью УЗИ. Для исключения риска послеоперационного кровотечения обязательно проводится гастроскопия. При выявлении язв или эррозий желудка проводится предварительное лечение. Уточнение картины поражения сосудов достигается с помощью компьютерной ангиографии (МСКТ). При выявлении значимых поражений сонных или коронарных артерий решается вопрос о преимущественной реваскуляризации этих бассейнов до операции на аорте. До операции необходимо скоррректировать все имеющиеся нарушния белкового и электролитного обмена, увеличить уровень гемоглобина крови. Накануне операции необходимо прочистить кишечник специальным препаратом и клизмами.
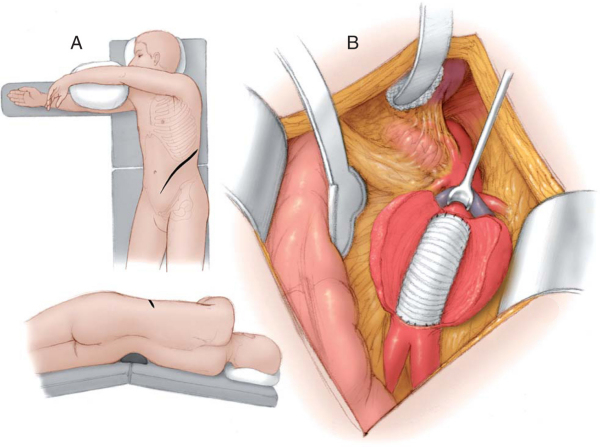 Ход
операции аорто-бедренного шунтирования.
Ход
операции аорто-бедренного шунтирования.
Обезболивание для АБШ - перидуральная анестезия (катетер в околопозвоночное пространство), либо общий наркоз. В обязательном порядке используется следящая аппаратура - монитор давления, ЭКГ, насыщения крови кислородом, давление в легочной артерии. Предпочтительный хирургический доступ - забрюшинный разрез по Робу, он имеет значительные преимущества по сравнению с традиционной лапаротомией (доступом через брюшную полость). При доступе по Робу не повреждаются поясничные нервы и не травмируется кишечник. Это позволяет начать питание больных уже на следующий день после операции, а через сутки можно уже подниматься с постели.
После выделения аорты, оценивается степень ее повреждения атеросклеротическим процессом. Операция заключается в выделении аорты выше места поражения через разрез на боковой стенке живота и бедренных артерий в верхних отделах бедер. В свободный от бляшек участок аорты вшивается искусственный сосуд, сделанный из инертного пластического материала, который не вызывает реакции окружающий тканей. Затем ветви этого сосудистого протеза выводятся к бедренным артериям и вшивается в свободные от поражений участки. Таким образом, обходится закупоренный участок и кровь легко проникает в ноги.Явления недостаточности кровообращения полностью ликвидируются. Шунты служат долго — 95 % проходимы в течение 5 лет и около 90% в течение 10 лет. Продолжительность работы шунта зависит от соблюдения пациентом предписаний врача, при отказе от курения.Необходимо периодическое наблюдение у оперировавшего хирурга и контрольные ультразвуковые исследования. Для профилактики прогрессирования атеросклероза проводится комплекс мер по снижению холестерина и нормализации обмена веществ.
Альтернативы операции аорто-бифеморального шунтирования у ослабленных больных
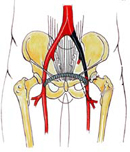 У
пациентов с критической ишемией и
высоким риском большой операции, при
синдроме Лериша, мы выполняем безопасные
вмешательства, которые называются
экстраанатомическими. Если закупорена
одна подвздошная артерия, то мы отводим
кровь с другой ноги. Если проходимая
(донорская) артерия сужена, то мы выполняем
ее раздувание баллоном и устанавливаем
стент, тем самым улучшая кровоток и в
относительно здоровой ноге.
У
пациентов с критической ишемией и
высоким риском большой операции, при
синдроме Лериша, мы выполняем безопасные
вмешательства, которые называются
экстраанатомическими. Если закупорена
одна подвздошная артерия, то мы отводим
кровь с другой ноги. Если проходимая
(донорская) артерия сужена, то мы выполняем
ее раздувание баллоном и устанавливаем
стент, тем самым улучшая кровоток и в
относительно здоровой ноге.
Если закрыты обе подвздошных артерии ног, тогда у ослабленных пациентов выполняется шунтирование из подмышечной артерии ниже ключицы в бедренную(ые) артерии (подмышечно-бедренное шунтирование). Преимущество экстраанатомических операций в то, что они выполняются легко и быстро с минимальным риском. Для обезболивания пригодна даже местная анестезия. Недостатком является меньшая проходимость шунтов. В течение 5 лет у 80%, В течение 10 лет у 70%. Однако в случае критической ишемии у пожилых и ослабленных другими болезнями пациентов эти операции помогают спасти ногу и избежать тяжелых осложнений. Альтернативой классическим операциям в последнее время стала рентгено-эндоваскулярная балонная дилатация и стентирование подвздошных артерий, которые выполняются через прокол в артерии и без открытого вмешательства, но результаты этих операций пока значительно уступают открытой хирургии и не всегда выполнимы из-за объема поражений. Однако сочетание этих операций с небольшими открытыми операциями позволяет сделать сосудистую хирургию эффективной и безопасной.и пожилых пациентов с высоким риском.
Послеоперационный период
Операции при синдроме Лериша переносятся хорошо, однако в послеоперационном периоде возможны осложнения. При сложной операции возможно кровотечение, которое требует переливания крови. Необходимо следить за артериальным давление и функцией почек. В раннем послеоперационном периоде возможно повышение температуры тела, иногда, у больных не спавших от боли несколько месяцев возможен острый психоз. Важно не допускать нагноения раны, так как инфекция может попасть на протез и вызвать его нагноение и кровотечение из анастомоза. После операции по поводу критической ишемии возможен выраженный отек ног, который держится до 3 месяцев. При сложных операциях на бедре возможна травма бедренного нерва, что иногда приводит к временному нарушению сгибания ноги в коленном суставе, как правило, эти явления проходят в течение месяца. Аорто-бедренные шунты работают долго, но требуют переодического внимания оперировавшего хирурга. Каждые 6 месяцев необходимо ультразвуковое сканирование артерий, чтобы выявить возможные патологические изменения. Сосудистая операция восстанавливает кровообращение в ноге, но не лечит атеросклероз, поэтому в послеоперационном периоде необходим прием препаратов, уменьшающих возможность тромбоза и прогрессирования атеросклероза.
Б) бедренно-подколенное шунтирование
Шунтирование артерий ног
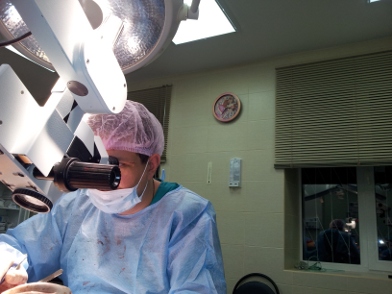 Поражение
артерий ниже паховой складки встречается
очень часто. При атеросклерозе эти
поражения развиваются медленно и
вызывают лишь перемежающуюся хромоту
(периодическая остановка из за болей в
икрах). Однако со временем может развиться
критическая ишемия и даже гангрена.
Операции при таких поражениях не любят
большинство сосудистых хирургов, так
как без использования микрохирургической
техники их исходы неудовлетворительны.
Наша клиника уже много лет занимается
этой проблемой и выполняет большинство
подобных операций в России, добиваясь
отличных результатов в сохранении ноги
при гангрене.
Поражение
артерий ниже паховой складки встречается
очень часто. При атеросклерозе эти
поражения развиваются медленно и
вызывают лишь перемежающуюся хромоту
(периодическая остановка из за болей в
икрах). Однако со временем может развиться
критическая ишемия и даже гангрена.
Операции при таких поражениях не любят
большинство сосудистых хирургов, так
как без использования микрохирургической
техники их исходы неудовлетворительны.
Наша клиника уже много лет занимается
этой проблемой и выполняет большинство
подобных операций в России, добиваясь
отличных результатов в сохранении ноги
при гангрене.
Показания к бедренно-дистальному шунтированию
Эту операцию необходимо выполнять только при критической ишемии или начинающейся гангрене. Выполнение операции при перемежающейся хромоте неоправдано, так как тромбоз реконструкции усугубляет ишемию. Принцип нашей клиники такой: если где-то предложили ампутацию, то мы возьмемся за микрошунтирование.
Пациент должен быть способен к самостоятельному передвижению. Нецелесообразно выполнять эту сложнейшую операцию у больных, прикованных к постели другим заболеванием. В данном случае при гангрене показана ампутация.
Тяжесть сопутствующих заболеваний играет небольшую роль, бедренно-тибиальный шунт переносится хорошо, значительно лучше, чем ампутация бедра при гангрене и шанс выжить у пациента после шунтирования больше.
Техническая возможность выполнения шунта. У пациента должна быть адекватная артерия притока (донорская), пригодная воспринимающая артерия и хороший материал для шунта. В этих случаях операция выполнима и дает хорошие результаты.
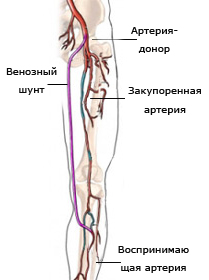 Техника
операции
Техника
операции
Доступ к целевой артерии. По результатом дооперационного обследования (УЗИ сосудов, МСКТ,ангиография) принимается решение о выборе артерии ниже места поражения, которая должна обеспечивать ногу кровью. Ревизия (осмотр) этой артерии является заключительным актом диагностики. Если этот сосуд оказывается пригодным, то операция выполнима, если нет, то нужно искать другой или отказываться от вмешатеьства. Благодаря использованию операционного микроскопа мы можем оценить артерию с большой степенью достоверности.
Выделение аутовенозного шунта. Поблизости от целевой артерии выделяется стволовая подкожная вена, выделяются ее притоки и проводится зондирование. Если вена проходима и достаточного диаметра (не менее 2 мм) шунтирование считается возможным. Если нет, изыскиваются другие возможные варианты шунтов (вена с другой ноги или руки, искусственный сосуд).
Доступ к донорской артерии. Как правило, используется бедренная артерия в области паха. При ревизии оценивается степень ее пригодности, в случае серьезных поражений - они исправляются удалением бляшек и ангиопластикой. Тут же забирается верхний участок вены, который вшивается в разрез бедренной артерии.
Разрушение венозных клапанов. При использовании большой подкожной вены in situ, внутрь вены вводится специальный зонд-нож, который при его выведении срезает створки венозных клапанов и обеспечивает поток крови по вене. Процедура повторяется несколько раз.
Перевязка сбросов крови по шунту. Так как большая подкожная вена имеет связи с глубокими венами, артериальная кровь из нее легче течет в венозную систему, а кровоток по шунту остается слабым. Поэтому необходимо выявить все сбросы крови и перевязать их. Венозные сбросы выявляются по УЗИ во время операции.
Выполнение анастомоза с целевой артерией. После появления хорошей пульсации шунта, вена сшивается с целевой артерией. Для выполнения этого этапа операции необходима микрохирургическая техника с увеличением в 16-25 раз. Операционный микроскоп позволяет выполнить анастомоз безупречно, даже с очень плохими артериями.
Контрольное УЗИ и ангиография. После запуска шунта необходимо оценить его функцию. Проводится изучение скорости кровотока по шунту, в анастомозе и в артериях ниже его. В случае сомнений выполняется контрастная ангиография. Если выявляются нарушения, угрожающие шунту, то принимаются меры по их исправлению.
Послеоперационный период после дистального шунтирования.
Кровоток обычно восстанавливается в течение нескольких часов после операции. Нога нагревается, заполняются вены на стопе. Влажные некрозы отграничиваются. Изменяется характер боли в ноге. Обычная для пациентов боль, заставляющая опускать ногу сменяется обратным ощущением - пациенту легче, когда нога вверху. Болевые ощущения принимают характер жжения и продолжаются еще 3-5 дней после операции. Послеоперационный отек - очень частое явление, он может продолжаться до 2-х месяцев после операции, но постепенно проходит.
Правильно выполненный бедренно - берцовый шунт приводит к купированию критической ишемии и способствует заживлению стопы после гангрены. Продолжительность работы таких шунтов в среднем 5 лет, однако нельзя забывать о профилактике тромбозов и проходить необходимое исследование. По опыту нашей клиники, с помощью бедренно-дистальных микрошунтов удается сохранить ногу 90% больным с критической ишемией и начинающейся гангреной.
В) симпатэктомия
По мере изучения роли нервной системы в патогенезе трофических расстройств конечностей стали производить операции на различных отделах нервной системы. На основании того, что сосудосуживающие симпатические волокна проходят в адвентиции сосудов, для расширения сосудов были предложены операции, направленные на пересечение вазоконстрикторов: ангиолиз [выделение участка артериального ствола из окружающей клетчатки —операция Жабуле (Jaboulay)], периартериальная симпатэктомия (циркулярное удаление адвентициалыного покрова артерии на протяжении нескольких сантиметров — операция Лериша), «химическая перерезка» симпатических путей (операция Разумовского), достигаемая путем смачивания артерии 80% алкоголем, и т. п. В. Н. Шамов в 1919 г. первым в Советском Союзе с успехом произвел десимпатизацию бедренной артерии при спонтанной гангрене, о чем сообщил на XV съезде российских хирургов. Ввиду того что облитерированная артерия, превращаясь в соединительнотканный тяж, не только прекращает свою функцию, но, становясь патологическим раздражителем, вызывает спастические реакции и тем самым снижает функцию коллатералей, Лериш предложил артериэктомию. Производимая при этой операции резекция измененного участка артерии является более действенной, чем десимпатизация артерии. В 1920 г. Лериш впервые произвел артериэктомию при тромбангиите и получил положительный результат. В дальнейшем он стал иссекать участки артерии длиной 20 см и более. Благоприятные результаты после артериэктомии отмечали В. Н. Шамда, резецировавший облитерированный участок при атеросклеротичеокой облитерации, Д. М. Думбадзе и др. Резекция измененного участка артерии производится и при последствиях лигатуры, при аневризмах, приводя в некоторых случаях к улучшению кровообращения (за счет снятия спастических явлений и расширения коллатералей) и трофики конечности. Артериэктомия применяется и в настоящее время (А. В. Бондарчук, А. Н. Филатов), особенно при обли-терирующем атеросклерозе, у пожилых больных, которым по общему состоянию нельзя произвести более эффективные операции. Из операций на симпатической нервной системе наибольшее распространение получила операция Диэца (Diez) — удаление симпатических ганглиев (поясничных при поражении сосудов нижних конечностей и грудных — при поражении верхних конечностей), которую производят не только при облитерирующих заболеваниях, но и при трофических расстройствах иного генеза. Ф. М. Плоткин получил успешный результат после поясничной симпатэктомии, которую сделал при остро развившейся ишемии после удаления аневризмы подколенной области. К этому времени уже была опубликована на русском языке работа Лериша и Фонтена, в которой приведен анализ 1256 операций на различных отделах симпатической нервной системы. По данным авторов, после артер'изктомии и поясничной ганглиэктомии получены лучшие результаты в тех случаях, когда трофические растройства были вызваны травмой артерий или болезнью Рено. При облитерирующем тромбангиозе различные операции - дали сходные результаты — около 60% улучшения, а при облитерирующем артериосклерозе улучшения добились в 76%. По мере накопления наблюдений по отдаленным результатам операций на симпатической нервной системе было установлено, что нередко они давали лишь временный эффект, а иногда приводили в последующем к тяжелым осложнениям: разрыву артерий после десимпатизации по Леришу или алкоголизации по Разумовскому, прогрессирующей ишемии конечности после поясничной симпатэктомии и т. я. Все это заставляло более сдержанно относиться к этим операциям. Однако в дальнейшем выяснилось, что осложнения, наблюдавшиеся после поясничной симпатэктомии, зависят от неправильного отбора больных, вмешательств в период обострения [Ф. М. Ламперт, Н. И. Махов, Такас (Takats)], недоучета артериовенозных анастомозов и т. д. В клинике, руководимой А. Т. Лидским, произведено 155 симпатэктомии у 126 больных с облитерацией артерий нижних конечностей в стадии значительной декомпенсации периферического кровообращения. Непосредственный положительный эффект отмечен в 63,9% случаев. Из 48 больных, у которых симпатэктомия не дала улучшения, у 33 пришлось ампутировать конечность в первый же месяц. Галлен (Hallen) отметил хорошие результаты после операции Диэца у 50—60% из 800 больных. Соответствующие данные приводят Буд и Ратлиф (Boud, Ratcllife)—60%, Ф. М. Ламперт — 81%, И. М. Тальман — 50—80%. А. Н. Шабанов из 1100 наблюдаемых им больных 242 произвел 284 симпатэктомии и получил в 81% случаев хорошие и удовлетворительные результаты. В. М. Ситенко, проследив 58 больных в течение 10—15 лет после поясничной ганглиэктомии, у 33 наблюдал значительное улучшение, в том числе у 14 — исчезновение перемежающейся хромоты, отсутствие дистрофий и пр.; 7 человек подверглись ампутации и у остальных больных состояние не изменилось или ухудшилось. А. В. Бондарчук также отмечает после симпатэктомии не только потепление конечности и исчезновение болей, но в последующем уменьшение, а у некоторых и исчезновение симптома перемежающейся хромоты: у 71% больных эффект оказался стабильным в сроки от 1 года до 10 лет. А. В. Бондарчук в то же время подчеркивает, что симпатэктомия противопоказана при юношеских, быстро текущих формах с генерализацией процесса, при прогрессирующем распаде тканей, интенсивных ишемических и невритичесиих болях и бурном гангренозном процессе, при наличии тромбоза вен. Данные литературы, в частности материалы XXVII Всесоюзного съезда хирургов, свидетельствуют, что поясничная симпатэктомия продолжает оставаться одной из наиболее распространенных операций при облитерации периферических сосудов, особенно при тромбангиите. Многие хирурги (А. Н. Филатов, Н. И. Махов, Гоффман и Генроти и др.) считают эту операцию рациональной и при облитерирующем атеросклерозе. А. Т. Лидокий утверждает, что в незапущенных случаях у лиц не старше 55 лет симшатэктомия нередко дает удовлетворительные результаты, предупреждая развитие гангрен. В последние годы часто производят симпатэктомию в сочетании с другими операциями (артериэктомией, тромбэктомией, пластикой сосудов, десимпатизацией артерий). Фонтен находит, что более выраженный терапевтический эффект достигается в тех случаях, когда наряду с симпатэктомией удаляют и надпочечник по Оппелю. Называя операции на симпатической нервной системе «сосудорасширяющими, гиперемирующими», Фонтен указывает, что за 25 лет им и его учителем Леришем было произведено 786 таких операций у 517 больных с хорошими результатами в 46% случаев. Стабилизация процесса при тромбангиозе отмечена у 13% больных, неудачные результаты — у 41 %.
Показания к лапароскопической симпатэктомии
Облитерирующий эндартериит и неспецифический артериит I—III степени
Облитерирующий атеросклероз сосудов нижних конечностей при ХАН IIA—III степени
Диабетическая ангиопатия
ПТФС глубоких вен нижних конечностей в III стадии (по B.C. Савельеву) — относительное показание.
Преимущества лапароскопической симпатэктомии
Малая травматичность снижает интенсивность послеоперационных болей, часто встречающихся при открытой операции. Редко наблюдают послеоперационный парез кишечника.
Короткий послеоперационный госпитальный период — больные через сутки способны самостоятельно вставать, начинают приём пищи. Через 2—3 дня пациента можно переводить на амбулаторное лечение.
Косметический эффект.
Снижение частоты развития послеоперационных гнойных осложнений.
Относительные противопоказания связаны с необходимостью создания напряжённого ретропневмоперитонеума
Тяжёлые сопутствующие заболевания.
ХОЗЛ.
Инфаркт миокарда.
Пороки сердца.
Сердечно-сосудистая недостаточность III степени.
Перенесённые операции на органах забрюшинного пространства.
Ожирение III—IV степени. Из-за сильно развитой жировой клетчатки выделение симпатического ствола проблематично.
Предоперационная подготовка к эндоскопической поясничной симпатэктомии такая же, как и к открытой забрюшинной симпатэктомии.
Обезболивание. Применяют интубационный наркоз или высокую спинномозговую анестезию.
Положение больного. Для выполнения поясничной симпатэктомии как справа, так и слева пациента укладывают на бок с подложенным под него валиком.
Оперативная техника лапароскопической симпатэктомии
Ретропневмоперитонеум. Забрюшинная поясничная симпатэктомия требует создания пространства между поясничными мышцами и забрюшинной клетчаткой для выделения поясничного симпатического ствола. Операция проходит на фоне напряжённого ретропневмоперитонеума, для создания которого используют углекислый газ или воздух.
В области схождения косых и прямой мышц живота на уровне пупка делают разрез кожи длиной 10 мм для введения видеотроакара (например, «Visiport»). Затем под контролем лапараскопа постепенно и осторожно расслаивают мягкие ткани до брюшины. После обнажения брюшины её тупо отслаивают для создания полости в забрюшинном пространстве.
Этот этап выполняют одним из двух вариантов.
Для создания необходимого пространства используют специальный раздувной баллон. Затем его удаляют и под контролем лапароскопа вводят второй 10-миллиметровый троакар для эндоретрактора. После частичной отслойки брюшины вводят 10-миллиметровый троакар, лапароскоп и нагнетают газ для создания полости. Под контролем лапароскопа на 2—3 см ниже первого троакара вводят второй 10-миллиметровый троакар для эндоретрактора. Этим инструментом продолжают отслаивать брюшину и забрюшинную клетчатку до поясничных мышц.
На следующем этапе вводят еще два 5-миллиметровых троакара для инструментов: один — отступя 2—3 см от гребня подвздошной кости, другой — отступя 2—3 см от рёберной дуги по подмышечной линии.
После того как от поясничных мышц отслоены брюшина и забрюшинная клетчатка им же выделяют симпатический ствол с ганглиями. Слева он будет находиться между аортой и поясничными мышцами, справа — между нижней полой веной и поясничными мышцами.
Ассистент удерживает ретрактором забрюшинную клетчатку, а оперирующий хирург вводит L-образный электрод и гибкий 5-миллиметровый диссектор. Подведя диссектор под симпатический ствол и поднимая его, хирург отсекает коллатеральные ветви ствола и выделяет симпатические ганглии. Как правило достаточно удалить 3—4 ганглия. После их выделения ретрактор меняют на зажим, диссектор — на ножницы. Симпатический ствол вместе с ганглиями иссекают ножницами без коагуляции для профилактики болей в послеоперационном периоде. После контроля гемостаза газ удаляют.
Возможно одномоментное выполнение двусторонней лапароскопической симпатэктомии.
Осложнения симпатэктомии
Повреждение брюшины во время создания ретропневмоперитонеума требует прекращения лапароскопической операции, так как введение газа создает пневмоперитонуем, сдавливающий забрюшинное пространство. Операцию заканчивают открытым методом. Частота этого осложнения варьирует от 2% до 8%.
Повреждение кровеносных сосудов. При левосторонней лапароскопической симпатэктомии возможно ранение поясничных артерий, отходящих от аорты, при правосторонней — поясничных вен, отходящих от нижней полой вены. Поясничные артерии обычно удаётся клипировать, повреждение вен может потребовать перехода к открытой операции.
Нагноение операционных ран происходит крайне редко. Продолжительность операции — от 30 до 60 минут. Лапароскопическая поясничная симпатэктомия — безопасная и достаточно эффективная операция в сравнении с открытым вмешательством.
Идея симпатэктомии при вегетативных сосудистых расстройствах принадлежит Жабулею (Gabouley), который предложил симпатэктомию сначала для лечения функциональных расстройств мочевого пузыря (1898), а затем для снятия сосудистых спазмов при облитерирующем эндартериите (1899).
Периартериальная симпатэктомия
Техника периартериальной симпатэктомии на бедренной артерии, детально разработанная Леришем, несложна.
Линейным разрезом параллельно продольной оси магистральной артерии обнажают и выделяют из ложа кровеносный сосуд. Затем глазным осторожно рассекают наружную оболочку артерии и снимают ее на намеченном участке.
В результате вмешательства сосуд расширяется, что отражается на кровообращении. Вскоре после операции кожа приобретает розовый цвет и становится более теплой. К сожалению, эта реакция длится недолго, всего 2—3 дня, после чего окраска конечности опять становится прежней.
У нас впервые эту операцию выполнил В. Н. Шамов (1919). В. И. Разумовский рекомендовал не удалять адвентициальную оболочку, а только смазывать ее спиртом. П. И. Страдынь с этой же целью вводил спирт в паравазальную клетчатку. Периартериальная симпатэктомия современными хирургами почти полностью оставлена ввиду малой эффективности.
Поясничная симпатэктомия
Значительно большее число сторонников приобрела люмбальная симпатэктомия, которую некоторые хирурги охотно применяют и сейчас. После люмбосакральной симпатэктомии местная температура может повыситься на 8 градусов.
Существуют три способа люмбальной симпатэктомии. Наиболее доступным и простым является подвздошный внебрюшной способ, разработанный Сталем-Вертхеймером и Боннио.
Операцию производят под ингаляционным потенцированным наркозом, спинномозговой анестезией. Больной лежит на спине или на боку. Кожный разрез проводят на 2 поперечных пальца ниже XI ребра по направлению к передней ости подвздошной кости, поворачивая его на 3 см выше последней, к середине под тупым, закругленным углом, чтобы он проходил на 3 см выше пупартовой связки в направлении прямой мышцы живота, заходя за боковой ее край на 1 см. На протяжении этого разреза расслаивают и частично пересекают наружную, внутреннюю косые, поперечную мышцы живота. Необходимо сохранить неповрежденными 11 и 12 межреберные нервы, для чего вверху раны манипулировать следует с большой осторожностью. После расслоения и пересечения мышц тупо расслаивают поперечную фасцию, а затем отодвигают кнутри париетальный листок брюшины с покрывающей его рыхлой предбрюшинной клетчаткой.
При отслаивании на протяжении разреза брюшинного листка, что удается сделать очень легко, в подвздошной области быстро обнажаются магистральные сосуды таза. Листок брюшины вместе с кишечником ассистент отодвигает кнутри и кверху, и хирург продолжает отслойку брюшины слева — от бокового края аорты, справа — от нижней полой вены. Постепенно обнажается переднебоковая поверхность III и II поясничных позвонков. Облегчает ориентацию в этом месте промежностнобедренный нерв, который обнаруживается на уровне III поясничного позвонка и проходит по m. psoas major; нерв должен быть отслоен от брюшины. М. psoas major отодвигают, при этом лимфатические узлы вместе с паравазальной клетчаткой отходят к сосудам. Таким образом доходят до тел позвонков, на которых, плотно прилегая к ним, располагается пограничный ствол симпатического нерва с ганглиями. Его следует искать по ганглиям.
Под освобожденный ганглий подводят лигатуру, после чего, натягивая ее, легко обнаружить межганглионарные веточки, которые отсепаровывают и отсекают на протяжении от II до IV поясничного позвонка. Для выделения ганглиев от V поясничного до III крестцового позвонка надо отслаивать брюшину книзу и к середине от передней поверхности крестца. Пограничные узлы симпатического нерва располагаются за сосудами, причем ганглий на уровне V поясничного позвонка оказывается толще других и нередко бывает двойным.
Операции на сакральном отделе симпатического нерва происходят на большой глубине и требуют для их выполнения специального освещения. Таз больного должен быть слегка приподнят. Четкому выполнению операции препятствуют мелкие кровеносные сосуды. При повреждении их часто приходится пользоваться тампонами, так как лигировать или коагулировать сосуды технически очень трудно.
Задняя внебрюшинная люмбальная симпатэктомия разработана Леришем и Вертхеймером. Операция технически сложна, при выполнении ее необходимо удалять поперечные отростки позвонков и часть подвздошной кости. Хирургу приходится манипулировать на большой глубине при недостаточно хорошей экспозиции. Не менее сложен и способ Ройля.
Способ Ройля заключается в следующем: больной лежит на противоположном боку с приподнятым тазом. Продольным разрезом от XII ребра к верхнему краю подвздошной кости рассекают послойно мягкие ткани, после чего разрез продолжают кпереди до передней ости подвздошной кости. Все мышцы до поперечной фасции пересекают. После рассечения поперечной фасции хирург погружает руку в пространство между четырехугольной поясничной и большой поясничной (m. psoas major) мышцами, при этом брюшную стенку нужно отодвигать кпереди тупыми крючками. Доступ к симпатическим ганглиям оказывается очень травматичным и кровавым. При нем приходится пересекать большие массивы мышц.
Большинство современных хирургов предпочитает внебрюшинный способ симпатэктомии, выполняя ее одновременно с обеих сторон через два отдельных разреза. Многие хирурги рекомендуют удалять второй и третий, реже, четвертый поясничный ганглий. Попытки еще больше расширить десимпатизацию в случаях, окончившихся неудачей после люмбальной симпатэктомии, оказались безуспешными.
Блокада симпатических ганглиев путем введения в паранефральную клетчатку 80—100 мл 0,25% новокаина является простым доступным методом, который позволяет через 2—3-недельный промежуток времени повторить лечение. Рекомендуется производить введение новокаина в сочетании со спиртом, но только в определенные участки симпатического ствола. Такая временная десимпатизация позволяет через некоторое время, как и при паранефральной блокаде, повторять ее; этот метод, однако, требует хорошей техники и точного выполнения.
Для хирургической десимпатизации большинство хирургов считает наиболее показанной операцию в первой и второй стадиях облитерирующего эндартериита.
В топографо-анатомическом и функциональном отношении различают преганглиозные, ганглиозные и постганглиозные вмешательства на симпатической нервной системе. Считается нужным удалять два поясничных ганглия, что приводит к перерыву максимального количества преганглионарных волокон при сохранении постганглионарных клеток и волокон. По его мнению, преганглионарная поясничная симпатэктомия прерывает дугу патологического рефлекса и устраняет спазм периферических сосудов, вследствие чего после операции происходит расширение коллатералей.
Постганглионарная симпатэктомия с удалением 2—4 поясничных симпатических ганглиев может ухудшить состояние больных. После того как в руководимой им клинике отказались от массивных симпатэктомий, результаты лечения стали лучше.
Следует помнить, что число симпатических ганглиев может не соответствовать количеству поясничных позвонков и не всегда ганглий может быть расположен точно на уровне одноименного позвонка. Описаны случаи слияний ганглиев в три, два и даже в один общий узел.
V. Венозная патология нижних конечностей
1. Функциональные пробы на проходимость глубоких вен, маршевая проба Дельбе-Пертеса и проба Пратта-1
2.Проба на несостоятельность клапанов : (Троянова-Тределенбурга, Гаккенбруха).
3.Проба на выявление коммуникантных вен: Пратта, трехжгутовая проба Шейниса.
ВРВ. Функциональные пробы состояния клапанов вен нижних конечностей.
О состоянии клапанного аппарата поверхностных вен позволяют судить проба Троянова —Тренделенбурга и проба Гаккенбруха.
Проба Троянова —Тренделенбурга.Больной,находясь в горизонтальном положении,поднимает ногу вверх под углом 45 °.Врач,поглаживая конечность от стопы к паху,опорожняет варикозно-расширенные поверхностные вены.После этого на верхнюю треть бедра накладывают мягкий резиновый жгут или сдавливают пальцами большую подкожную вену в овальной ямке у места ее впадения в бедренную.Больного просят встать.В норме наполнение вен голени не происходит в течение 15 с.Быстрое наполнение вен голени снизу вверх свидетельствует о поступлении крови из коммуникантных вен вследствие недостаточности их клапанов.Затем быстро снимают жгут (или прекращают сдавление вены).Быстрое наполнение вен бедра и голени сверху вниз свидетельствует о недостаточности остиального клапана и клапанов ствола большой подкожной вены,характерного для первичного варикозного расширения вен.
Проба Гаккенбруха.Врач нащупывает на бедре овальную ямку — место впадения большой подкожной вены в бедренную и просит больного покашлять.При недостаточности остиального клапана пальцы воспринимают толчок крови (положительный симптом кашлевого толчка).
Для оценки состоятельности клапанов коммуникантных вен используют пробу Пратта-2,трехжгутовую пробу Шейниса или пробу Тальмана.
Проба Пратта-2.В положении больного лежа после опорожнения подкожных вен на ногу,начиная со стопы,накладывают резиновый бинт,сдавливающий поверхностные вены.На бедре под паховой складкой накладывают жгут.После того как больной встанет на ноги,под самым жгутом начинают накладывать второй резиновый бинт.Затем первый (нижний)бинт снимают виток за витком,а верхним обвивают конечность книзу так,чтобы между бинтами оставался промежуток 5 —6 см.Быстрое наполнение варикозных узлов на свободном от бинтов участке указывает на наличие здесь коммуникантных вен с несостоятельными клапанами.
Трехжгутовая проба Шейниса по существу является модификацией предыдущей пробы.Больного укладывают на спину и просят приподнять ногу,как при пробе Троянова —Тренделенбурга.После того как подкожные вены спадутся,накладывают три жгута в верхней трети бедра (вблизи паховой складки),на середине бедра и тотчас ниже колена.Больному предлагают встать на ноги.Быстрое наполнение вен на каком-либо участке конечности, ограниченном жгутами,указывает на наличие в этом сегменте коммуникантных вен с несостоятельными клапанами.Быстрое наполнение варикозных узлов на голени свидетельствует о наличии таких вен ниже жгута.Перемещая жгут вниз по голени (при повторении пробы),можно более точно локализовать их расположение.
Проба Тальмана — модификация пробы Шейниса.Вместо трех жгутов используют один длинный (2 —3 м)жгут из мягкой резиновой трубки,который накладывают на ногу по спирали снизу вверх;расстояние между витками жгута — 5 —6 см.Наполнение вен на каком-либо участке между витками свидетельствует об имеющейся в этом пространстве коммуникантной вены с несостоятельными клапанами.
Представление о проходимости глубоких вен дают маршевая проба Дельбе —Пертеса и проба Пратта-1.
Маршевая проба Дельбе —Пертеса.Больному в положении стоя,когда максимально наполняются подкожные вены,ниже коленного сустава накладывают жгут,сдавливающий только поверхностные вены.Затем просят больного походить или промаршировать на месте в течение 5 —10 мин.Если при этом подкожные вены и варикозные узлы на голени спадаются,значит, глубокие вены проходимы.Если вены после ходьбы не запустевают,напряжение их на ощупь не уменьшается,то результат пробы надо оценивать осторожно,так как он не всегда указывает на непроходимость глубоких вен,а может зависеть от неправильного проведения пробы (сдавление глубоких вен чрезмерно туго наложенным жгутом),от наличия резкого склероза поверхностных вен,препятствующего спадению их стенок.Пробу следует повторить.
Проба Пратта-1.После измерения окружности голени (уровень следует отметить,чтобы повторное измерение провести на этом же уровне)больного укладывают на спину и поглаживанием по ходу вен опорожняют их от крови.На ногу (начиная снизу)туго накладывают эластичный бинт,чтобы надежно сдавить подкожные вены.Затем больному предлагают походить в течение 10 мин.Появление боли в икроножных мышцах указывает на непроходимость глубоких вен.Увеличение окружности голени после ходьбы при повторном измерении подтверждает это предположение.
Локализацию перфорантных вен с несостоятельными клапанами можно определить иногда путем пальпации дефектов в апоневрозе,через которые они перфорируют фасцию.Инструментальная оценка несостоятельности клапанов точнее перечисленных выше проб.
