- •Лекция 17. Явления переноса.
- •16. 1. Среднее число столкновений и длина свободного пробега молекул.
- •16. 1. Длина свободного пробега молекул.
- •16. 2. Среднее число столкновений молекул.
- •16. 2. Явления переноса в термодинамически неравновесных системах
- •16. 2. 1. Диффузия.
- •16. 2. 2. Теплопроводность.
- •16. 2. 3. Вязкость жидкостей и газов (Внутреннее трение).
- •16. 3. Заключение. Связь коэффициентов переноса.
Федун В. И. Конспект лекций по физике Молекулярная физика и термодинамика
Лекция 17. Явления переноса.
До сих пор мы почти всегда рассматривали системы, находящиеся в состоянии термодинамического, или статистического равновесия. Однако, несмотря на безусловно важную роль равновесных состояний, они все же представляют собой особый случай. Во многих задачах, представляющих огромный физический интерес, мы имеем дело с системами, не находящимисяв равновесных состояниях.
Наука, изучающая процессы, идущие при нарушении равновесия, называется физической кинетикой.Физическая кинетика рассматривает необратимые процессы в телах, протекающие с конечными скоростями.
Рассмотрение неравновесных процессов, приводящих систему в состояние равновесия, представляет собой весьма сложную задачу. Поэтому мы подойдем к рассмотрению проблемы с помощью простейших приближенных методов, выбрав в качестве объекта исследования разреженный газ.
16. 1. Среднее число столкновений и длина свободного пробега молекул.
16. 1. Длина свободного пробега молекул.
Длиной
свободного пробега
![]() называется
путь, проходимый молекулой между двумя
последовательными столкновениями.
называется
путь, проходимый молекулой между двумя
последовательными столкновениями.
Вследствие
хаотичности движения
![]() различны.
различны.
Средней
длиной свободного пробега
молекул
<![]() >называется
путь, который в среднем проходят молекулы
между двумя последовательными
столкновениями:
>называется
путь, который в среднем проходят молекулы
между двумя последовательными
столкновениями:
|
|
(16.1) |
где N - число молекул.
|
|
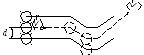
Эффективным диаметром d молекулы называется минимальное расстояние, на которое сближаются при столкновении центры двух молекул (см. рис. 16.1).
В
общем случае эффективный диаметр
зависит от скорости сталкивающихся
молекул, т.е. от температуры газа.
Эффективный диаметр молекулы
|
|
Рисунок 16. 1. |
Значения D при нормальных условиях для некоторых газов
|
Газ |
Воздух |
Водород |
Кислород |
Азот |
|
D, нм |
0,27 |
0,28 |
0,36 |
0,58 |
16. 2. Среднее число столкновений молекул.
Введём
понятие среднего
числа столкновений <![]() >молекулы
в единицу времени.
>молекулы
в единицу времени.
Тогда
число столкновений молекулы за время
![]() есть
есть
![]() и
оно равно отношению среднего пути
молекулы
и
оно равно отношению среднего пути
молекулы
![]() к
средней длине свободного пробега <
к
средней длине свободного пробега <![]() >:
>:
|
|
(16.2) |
|
|
|
|
Рисунок 16. 2. |
Введём
понятие эффективного
сечения
![]() столкновения
как
площади поперечного сечения («коридора»)
ломаного цилиндра, в которой должны
попасть центры соседних молекул, чтобы
столкнуться с данной. Из рисунка 16.2
видно, что:
столкновения
как
площади поперечного сечения («коридора»)
ломаного цилиндра, в которой должны
попасть центры соседних молекул, чтобы
столкнуться с данной. Из рисунка 16.2
видно, что:
|
|
(16.3) |
Рассчитаем
число столкновений молекулы за время
![]() .
.
Предположим,
что рассматриваемая молекула движется
со скоростью
![]() ,
а
остальные покоятся. Тогда рассматриваемая
молекула столкнётся со всеми молекулами,
находящимися в цилиндре
площадью
основания Sэфф
и
длиной
,
а
остальные покоятся. Тогда рассматриваемая
молекула столкнётся со всеми молекулами,
находящимися в цилиндре
площадью
основания Sэфф
и
длиной
![]() .
Число
молекул, а значит и число столкновений
определяется соотношением:
.
Число
молекул, а значит и число столкновений
определяется соотношением:
|
|
(16.4) |
где n- концентрация молекул.
Чтобы
учесть движение всех молекул можно,
например, перейти в систему координат,
связанную с движущейся молекулой, т.е.
перейти от скорости
![]() к
средней скорости
к
средней скорости
![]() движения молекул. Поскольку все движения
молекул равновероятны, то угол между
направлениями скоростей лежит в интервале
(
движения молекул. Поскольку все движения
молекул равновероятны, то угол между
направлениями скоростей лежит в интервале
(![]() )
и
средний угол равен
)
и
средний угол равен
![]() .
Модуль
относительной скорости тогда будет:
.
Модуль
относительной скорости тогда будет:
|
|
(16.5) |
С учётом сделанных поправок, формула () приобретает вид:
|
|
(16.6) |
Тогда
среднее число столкновений молекулы в
единицу времени
![]() будет
определяться выражением:
будет
определяться выражением:
|
|
(16.7) |
Приведённое соотношение носит название формулы Клаузиуса - Максвелла.
Чтобы
найти число столкновений в единицу
времени молекул газа концентрации
![]()
![]() и
в объёме
и
в объёме
![]() ,
т.е.
для
,
т.е.
для
![]() молекул газа надо величину
молекул газа надо величину![]() умножить
на
умножить
на
![]() ,
т.к.
в каждом столкновении принимают участие
2 молекулы:
,
т.к.
в каждом столкновении принимают участие
2 молекулы:
|
|
(16.8) |
Тогда среднее число столкновений молекул в единицу времени в единичном объёме есть:
|
|
(16.9) |
Теперь можно вернуться к средней длине свободного пробега молекулы.
За
время
![]() молекула
проходит путь:
молекула
проходит путь:
|
|
(16.10) |
и испытывает за это время число соударений, равное:
|
|
(16.) |
Значит
средняя длина свободного пробега
![]() будет
равна (с учётом ()):
будет
равна (с учётом ()):
|
|
(16.) |
Если
учесть, что
![]() ,
то
получаем:
,
то
получаем:
|
|
(16.11) |
Концентрация
молекул
![]() связана
с термодинамическими параметрами
связана
с термодинамическими параметрами
![]() и
и
![]() уравнением состояния.
уравнением состояния.
|
|
(16.12) |
Тогда окончательно получаем:
|
|
(16.13) |