
- •Изучение процесса кристаллизации
- •Теоретические сведения
- •Приборы, материалы, инструмент
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Определение твердости металлов и сплавов
- •Теоретические сведения
- •Приборы, материалы, инструмент
- •Определение твердости по Бринеллю
- •Определение твердости по Роквеллу
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Выявление микроструктуры металлов и сплавов
- •Теоретические сведения
- •Приборы, материалы, инструмент
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Анализ микроструктуры углеродистых сталей
- •Теоретические сведения
- •100 % Перлита - 0,8 % с
- •40 % Перлита - х % с
- •Приборы, материалы и инструменты
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Анализ микроструктуры чугунов
- •Теоретические сведения
- •Приборы, материалы и инструмент
- •Порядок выполнения работы
- •Содержание отчета
- •Контрольные вопросы
- •Параметры испытания при определении твердости методом Бринелля
- •Определение чисел твердости по Бринеллю
- •Выбор нагрузки и индентора для испытаний методом Роквелла
- •Соотношение чисел твердости по Бринеллю и Роквеллу
Лабораторная работа 1
Изучение процесса кристаллизации
Цель работы : 1. С помощью биологического микроскопа провести наблюдение за процессом кристаллизации из раствора соли.
2. Определить факторы, влияющие на формирование структуры кристаллического тела.
Теоретические сведения
Переход материала из жидкого состояния в твердое с образованием кристаллической структуры называется кристаллизацией.
Самопроизвольная кристаллизация обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением термодинамического потенциала G (энергии Гиббса). Энергетическое состояние веществ а при равновесии характеризуется минимальным значением G. С повышением температуры термодинамический потенциал вещества уменьшается как в твердом, так и в жидком состоянии (рис. 1).
Температура, при которой термодинамические потенциалы вещества в твердом и жидком состоянии равны (Ts ), называется равновесной температурой кристаллизации. Кристаллизация происходит в том случае, если термодинамический потенциал вещества в твердом состоянии будет меньше термодинамического потенциала вещества в жидком состоянии, т.е. при переохлаждении жидкого металла до температуры ниже равновесной.
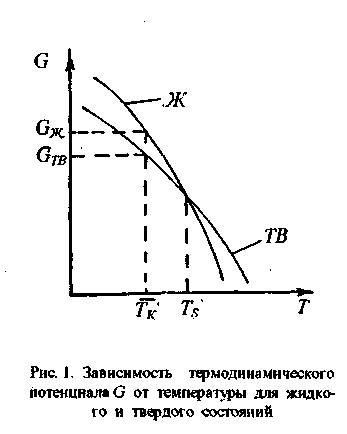

|
|
|
Процесс образования кристаллов путем зарождения центров кристаллизации и их роста можно изучить с помощью модели, представленной на рис. 3.
Эта модель позволяет объяснить два важных момента:
1. По мере развития процесса кристаллизации в нем участвует все большее число кристаллов. Процесс ускоряется до тех пор, пока в какой-то момент взаимное столкновение растущих кристаллов не начинает заметно препятствовать их росту.
2. Пока кристалл окружен жидкостью, он имеет правильную форму, но при столкновении кристаллов форма нарушается - она оказывается зависимой от условий соприкосновения кристаллов. Такое строение металла называется поликристаллическим (гр. poly - много). Кристаллы неправильной формы в полукристаллическом агрегате называются кристаллитами, или зернами.
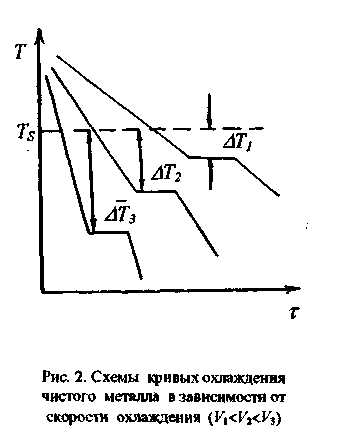
Скорость процесса кристаллизации количественно определяется двумя величинами: скоростью зарождения центров кристаллизации (ч.ц.) и скоростью роста кристаллов (с.к.). Установлено, что ч.ц. и с.к. зависят от степени переохлаждения. Эта зависимость выражается кривыми с максимумом (рис. 4). При теоретической температуре кристаллизации значения ч.ц. и с.к. возрастают (так как возрастает G, рис. 1), достигают максимума и затем понижаются (так как при пониженных температурах уменьшается подвижность атомов).
Размер образовавшихся кристаллов зависит от соотношения величин с.к. и ч.ц. при данной степени переохлаждения. При большом значении с.к. и малом значении ч.ц. (малые степени переохлаждения, рис. 4) образуются немногочисленные крупные кристаллы, при малых значениях с.к. и ч.ц. (большие степени переохлаждения) образуется большое количество мелких кристаллов. Реально протекающий процесс кристаллизации усложняется действием различных факторов, и роль степени переохлаждения может стать в количественном отношении второстепенной.

В направлении отвода тепла кристалл растет быстрее, в результате чего образуется вытянутый кристалл, так называемый дендрит (древовидный).
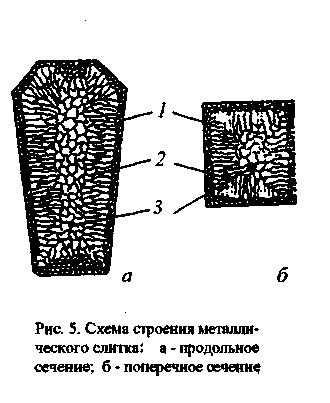
Сочетание перечисленных факторов (часто не поддающихся точному учету) с общими законами кристаллизации и определяет особенности строения металлического слитка (рис. 5). Структура литого металла состоит из трех основных зон. Сначала на поверхности слитка образуется зона 1 - мелкие кристаллы (результат влияния холодной металлической формы, которая обеспечивает в первые моменты затвердевания большую степень переохлаждения). Затем формируется зона 2. Из-за повышения температуры стенки формы степень переохлаждения уменьшается, в результате чего из небольшого числа центров в направлении отвода тепла начинают расти дендриты.
Зона 3 – зона равноосных кристаллов. В центре слитка уже нет определенной направленности отдачи теплоты, наблюдается наименьшая степень переохлаждения, и поэтому образуются равноосные зерна больших размеров. При определенных условиях (перегретый жидкий металл, малое содержание примесей) зона равноосных кристаллов может отсутствовать.
В процессе кристаллизации капли раствора соли, как и при затвердевании металлического слитка, наблюдаются три структурные зоны.
