
- •Методы исследования физиологических функций и констант организма (вопросы к экзаменам) Кровь
- •Анализ нарушений кислотно-щелочного состояния
- •Сердечно-сосудистая система
- •Метод Фика
- •Дыхание
- •Сенсорные системы
- •Адаптометрия
- •Нервная система и вмф
- •Обмен, пищеварение и питание
- •Выделение
- •Определение скорости клубочковой фильтрации (скф) для диагностики заболеваний почек
- •Прямое измерение
- •Косвенная оценка
Анализ нарушений кислотно-щелочного состояния
р Н а р т е р и а л ь н о й к р о в и
АЦИДОЗ (меньше 7.4) АЛКАЛОЗ (больше 7.4)
дыхательный недыхательный дыхательный недыхательный
рСО2>40 pCO3< 24 (BE <0) pCO2<40 HCO3> 24 (BE >0)
почечная легочная почечная легочная
компенсация компенсация компенсация компенсация
HCO3 > 24 (BE >0) pCO2 <40 pCO3 < 24 (BE <0) рСО2 >40

Нарушения кислотно-щелочного состояния (КЩС) являются в большинстве случаев следствием серьезного патологического нарушения и редко имеют самостоятельное значение. Исследование газового состава артериальной крови (ГАК) - незаменимый метод диагностики.
♦ Обычно pH измеряют прямым методом при помощи специального стеклянного электрода, который имеет мембрану, проницаемую для H+.
♦ Концентрация ионов бикарбоната - HCO3- измеряется бикарбонатным электродом или может быть получена расчетным путем.
♦ CO2 обычно измеряется прямым методом при помощи СО2-электрода.
Бикарбонатная система участвует в регуляции pH всех компартментов внутренней среды, обладая возможностью вмешиваться в кислотно-щелочное состояние на двух уровнях: концентрация HCO3- регулируется почками, a CO2 – легкими: H+ + HCO3- → H2CO3 → H2O + CO2
Точное значение pH среды может быть рассчитано при помощи уравнения Гендерсона-Хассельбаха:
pH = pK + log
[основание] / [кислота] = pK + log [HCO3-] / [H2CO3]
pK представляет собой специфичную для данного буфера константу (например, для бикарбонатной системы при 37°С pK составляет 6,1).
Поскольку концентрация HCO3- регулируется почками, а выведение CO2 - легкими, уравнение принимает следующий вид: pH = константа ПОЧКИ / ЛЕГКИЕ
Терминологические замечания: ацидоз / ацидемия и алкалоз / алкалемия. Суффикс "емия" ("aemia") означает "определяемый в крови".
|
Нормальные значения газового состава крови | |||
|
Показатель |
Границы нормы |
Единицы |
Примечания |
|
pH |
7,35 - 7,4 - 7,45 |
|
(относительная величина) |
|
PaCO2 |
4,8 - 5,3 - 5,9 36 - 40 - 44 |
кПа мм рт. ст. |
|
|
PaO2 |
11,9 - 13,2 90 - 100 |
кПа мм рт. ст. |
На уровне моря FiO2 = 21%, становится ниже с повышением высоты, повышается при кислородотерапии |
|
HCO3- (актуальный бикарбонат - AB) |
22 - 24 - 26 |
ммоль/л |
Нормальные значения могут варьировать при изменении PCO2 |
|
Стандартный бикарбонат (SB) |
22 - 24 - 26 |
ммоль/л |
[HCO3-] после его стандартизации (эквилибровка) по значению CO2 40 мм рт. ст. (5,3 кПа) |
|
Избыток оснований (BE) |
-2,0 - +2,0 |
ммоль/л |
При отрицательном значении BE говорят о дефиците оснований |
Бикарбонатная буферная система играет наиболее важную роль в поддержание постоянства кислотно-щелочного состояния и может быть оценена при анализе газового состава крови. Легкие способны регулировать выведение CO2, а почки экскрецию или задержку HCO3-. Это взаимодействие позволяет с высокой точностью поддерживать и регулировать соотношение кислот и оснований в организме.
|
Каково значение показателей кислотно-щелочного состояния (КЩС) и газового состава артериальной крови (ГАК)? | |
|
pH |
Общие кислотно-щелочные свойства среды. Указывает, имеется ли у пациента ацидемия или алкалемия. |
|
PCO2 |
Респираторный компонент |
|
PO2 |
Характеризует оксигенацию и не имеет отношения к кислотно-щелочному состоянию (КЩС). В общих чертах является маркером тяжести заболеваний легких, но не поддается интерпретации при неизвестном значении FiO2. PO2 может быть выше 650 мм рт. ст. (85 кПа) при нормальной функции легких на фоне FiO2 = 100%. Прогнозируемый уровень PaO2 при нормальной функции легких может быть рассчитан при помощи уравнения альвеолярного газа. В грубом приближении значение прогнозируемого PaO2 может быть рассчитано как FiO2 (%) х 6 мм рт. ст. (например, при вентиляции пациента с FiO2 = 40% PaO2 должно составить 6 х 40 = 240 мм рт. ст.). Если реальное значение ниже расчетного, имеет место внутрилегочное шунтирование крови (кровь не проходит через вентилируемые альвеолы и поступает в аорту неоксигенированной.). Чем тяжелее поражение легких, тем ниже будет значение PaO2 при данном уровне FiO2. |
|
HCO3- (актуальный бикарбонат) |
Ренальный компонент компенсации. |
|
Стандартный бикарбонат |
Дополнительный показатель, характеризующий ренальный (метаболический) компонент в нарушениях кислотно-щелочного состояния (КЩС). Имеет большую ценность, чем актуальный бикарбонат, поскольку корректирован по отношению к измененному значению PCO2. |
|
Избыток оснований |
Соответствует количеству сильной кислоты (или основания в случае дефицита оснований), необходимому для титрования 1 литра крови и возвращении значения pH к значению 7,4 при PCO2 = 5,3 кПа и температуре 37°С. Дополнительный показатель, характеризующий ренальный (метаболический) компонент нарушения. Информационная ценность близка к таковой стандартного бикарбоната (нормальное значение около 0 ммоль/л, для стандартного бикарбоната - 24 ммоль/л). |
Дыхательная система способна осуществлять быструю компенсацию нарушений кислотно-щелочного состояния (КЩС) (в течение нескольких минут). Метаболическая компенсация (почки, система бикарбоната) запускается в течение часов или нескольких дней. Взаимодействие этих компенсаторных систем позволяет точно регулировать кислотно-щелочного состояние (КЩС). Их цель состоит в поддержании внеклеточного значения pH на уровне 7,4, который является оптимальным для протекания большинства метаболических процессов, например, химических реакций, катализируемых ферментами, и переноса веществ через клеточные мембраны.
Патологические процессы, такие, как тканевая гипоксия, почечная недостаточность, гиповентиляция ведут к нарушению кислотно-щелочного баланса. При нарушении со стороны одной из регуляторных систем другая будет пытаться компенсировать изменения кислотно-щелочного состояния (КЩС) и привести pH к оптимальному значению. Нарушения кислотно-щелочного состояния (КЩС) и некоторые их причины представлены в таблице "Нарушения кислотно-щелочного состояния".
|
Нарушения кислотно-основного состояния | ||
|
Респираторный ацидоз |
PaCO2 повышено |
Развивается при неадекватной вентиляции, когда продукция CO2 превышает его элиминацию. Возможные причины: обструкция дыхательных путей, депрессия дыхания (вследствие действия препаратов, ЧМТ, заболеваний дыхательной системы и т.д.) |
|
Респираторный алкалоз |
PaCO2 снижено |
Возникает при гипервентиляции. Гипервентиляция может быть следствием ответа на гипоксемию и включения гипоксического респираторного драйва. Способность легких к выведению CO2 значительно выше, чем к абсорбции O2, в связи с чем при заболеваниях легких часто наблюдается гипоксемия на фоне нормального или пониженного уровня CO2. Причиной респираторного алкалоза может быть ИВЛ с высоким минутным объемом вентиляции. |
|
Метаболический ацидоз |
HCO3- снижен (дефицит оснований) |
Множество этиологических факторов: ♦ Потери бикарбоната через ЖКТ или хроническое поражение почек (нормальный анионный интервал) ♦ Поступление дополнительных количеств неорганических кислот, например, при диабетическом кетоацидозе, лактат-ацидозе, связанном с тканевой гипоксией, передозировка салицилатов, отравление этиленгликолем и прочими ядами, снижение экскреции кислот при почечной недостаточности (повышение анионного интервала). |
|
Метаболический алкалоз |
HCO3- повышен (избыток оснований) |
Возникает при потерях желудочного содержимого (например, пилоро-стеноз) и терапии диуретиками. Метаболический алкалоз часто сопровождается снижением хлоридов (Cl-) сыворотки. |
|
Смешанный ацидоз |
PaCO2 повышено, HCO3- снижено |
Крайне опасное нарушение. Может развиваться при таких тяжелых расстройствах, как септический шок, полиорганная недостаточность, остановка кровообращения. |
Компенсаторные механизмы пытаются вернуть pH к нормальному значению, несмотря на сохранение отклонений [HCO3-] и PCO2 до коррекции первичного нарушения. Компенсация нарушений кислотно-щелочного состояния (КЩС) не должна носить характер избыточной. Например, при метаболическом ацидозе наблюдается падение значения pH < 7,4. При адекватной респираторной компенсации pH будет стремиться к нормальному значению, но не превысит 7,4.
Вот несколько подсказок, которые помогут Вам дифференцировать первичное нарушение и компенсаторный эффект.
Первичное нарушение (метаболического или респираторного характера) по типу параллельно отклонению pH: при снижении pH имеет место ацидотическое нарушение, при повышении pH развивается алкалоз. Компенсаторный эффект (респираторный или метаболический) имеет противоположное направление. Механизмы компенсации будут отклонять pH в сторону нормального значения, при этом полная компенсация достигается редко (восстановление нормального исходного значения), а избыточная компенсация - никогда.
К примеру, если Вы обнаружили сочетание метаболического ацидоза и респираторного алкалоза, значение pH подскажет, какое из нарушений носит первичный, а какое - компенсаторный характер. Если значение pH снижено, первичным дефектом является метаболический ацидоз с респираторной компенсацией. При повышении pH в роли первичного нарушения выступает респираторный алкалоз с метаболической компенсацией.
|
Пошаговая интерпретация газового состава крови | ||
|
Шаг 1 |
Общая картина без отклонений, имеется ацидемия или алкалемия? |
pH < 7,35 = ацидемия [... перейдите к шагу 2] pH > 7,45 = алкалемия [... перейдите к шагу 5] |
|
Шаг 2 |
Если наблюдается ацидемия: Характер первичного нарушения: метаболический, респираторный или смешанный? |
CO2 повышен = респираторный ацидоз [... шаг 3] Бикарбонат снижен, значение BE отклонено в отрицательном направлении = метаболический ацидоз [... шаг 4] |
|
Шаг 3 |
Если имеет место респираторный ацидоз: Имеется метаболическая компенсация? |
CO2 повышено (респираторный ацидоз), но метаболический компонент изменяется в противоположном направлении (BE или стандартный бикарбонат (SB) повышены, как при метаболическом алкалозе), что говорит о метаболической компенсации первичных нарушений кислотно-щелочного состояния (КЩС). |
|
Шаг 4 |
Если имеет место метаболический ацидоз: Имеется ли респираторная компенсация? |
Значение BE принимает отрицательное значение (метаболический ацидоз); респираторный компонент изменяется в противоположном направлении (CO2 снижен - респираторный алкалоз), что говорит о респираторной компенсации. |
|
Шаг 5 |
Если наблюдается алкалемия: Характер первичного нарушения: метаболический или респираторный? |
Первичное нарушение имеет то же направление, что и изменения pH (в сторону алкалоза). Респираторный алкалоз сопровождается снижением CO2. При метаболическом алкалозе CO2 повышается и значение BE становится положительным. |
|
Шаг 6 |
При наличии респираторного или метаболического алкалоза: Есть ли элементы компенсации? |
Изменения равнозначны вышеуказанным. |
|
Шаг 7 |
Обратите внимание на оксигенацию |
Соответствует ли значение PaO2 установленному FiO2? Уровень оксиге-нации ниже прогнозированного может указывать на заболевание легких, шунтирование крови или ошибочный забор образца венозной крови (в последнем случае PaO2 обычно < 40 мм рт. ст., сатурация < 75%). Способность легких к элиминации CO2 превышает их резерв в отношении оксигенации. В связи с этим заболевания легких часто сопровождаются гипоксемией на фоне нормального или сниженного значения PCO2. Значительное повышение CO2 сопровождается параллельным снижением O2. |
|
Шаг 8 |
Суммируйте Ваши наблюдения |
Например: наблюдается метаболический ацидоз (поскольку pH снижен, BE имеет отрицательное значение) с респираторной компенсацией (поскольку параллельно снижено значение PCO2). |
|
Шаг 9 |
Попытайтесь установить причину нарушений |
|
Определение водородного показателя (рН) крови проводят электрометрическим способом с применением специального стеклянного электрода, чувствительного к ионам водорода.
Кислотно-основное состояние крови связано с содержанием в ней углекислого газа. Для установления уровня напряжения углекислого газа и кислорода в крови применяют эквилибрационную методику Аструпа или электрод Северингхауса. Значения, характеризующие изменения кислотно-основного состояния, рассчитывают посредством составления номограммы.
Сейчас массово выпускают приборы, определяющие рН, напряжение С02 и 02 в крови; расчеты производятся с помощью микрокомпьютера, входящего в состав прибора. В настоящее время для определения кислотно-щелочного состояния наиболее широко применяется так называемая методика Аструпа.
Для определения кислотно-основного состояния крови берется артериальная или капиллярная (из кончика пальца) кровь. Следует отметить, что наиболее высокое постоянство кислотно-щелочных показателей отмечается все же в артериальной крови.
У здорового человека рН артериальной крови составляет 7,35-7,45, т.е. кровь имеет слабощелочную реакцию.
Снижение величины рН свидетельствует о сдвиге реакции крови в кислую сторону, что называется «ацидоз» (рН < 7,35), а увеличение данного показателя свыше 7,45 - о сдвиге реакции крови в щелочную сторону (алкалозе).
Сдвиги рН более чем на 0,4 (рН менее 7,0 и более 7,8) расцениваются как несовместимые с жизнью.
Изменения рН, отличные от нормы, обозначаются как: 1) субкомпенсированный ацидоз (рН 7,25-7,35); 2) декомпенсированый ацидоз (рН < 7,25); 3) субкомпенсированный алкалоз (рН 7,45-7,55); 4) декомпенсированный алкалоз (рН > 7,55).
Немаловажно учитывать при оценке кислотно-основного состояния организма РаС02, т.е. напряжение углекислого газа в артериальной крови. В норме данный показатель составляет в среднем 40 мм рт. ст. (от 35 до 45), а более значительные отклонения от нормы являются признаком дыхательных нарушений.
Метаболический алкалоз или ацидоз определяется в том числе по избытку или недостаточности буферных оснований (Buffer Base, ВВ) в крови. У здорового человека В В = 0, а допустимые пределы колебаний составляют ±2,3 ммоль/л.
Такой показатель как «стандартные бикарбонаты» (SB) отражает концентрацию бикарбонатов в крови при стандартных условиях (рН = 7,40; РаС02 = 40 мм рт. ст.; t = 37 °С; S02 = 100%). «Истинные, или актуальные бикарбонаты» (АВ) отражают состояние бикарбонатного буфера в условиях конкретного организма, в норме совпадают со «стандартными» и составляют 24,0 ± 2,0 ммоль/л.
Показатели SB и АВ снижаются при нарушение обмена веществ со сдвигом реакции крови в кислую сторону и уменьшаются при сдвиге реакции крови в щелочную сторону.
Если лабораторные данные свидетельствуют о наличии метаболического ацидоза, это может быть признаком кетоацидоза, сахарного диабета, кислородного голодания (гипоксии) тканей, шокового состояния, а также ряда других патологических состояний.
Причиной метаболического алкалоза может стать неукротимая рвота (с большой потерей кислоты с желудочным соком) или чрезмерное употребление в пищу продуктов, вызывающих ощелачивание организма (растительных, молочных).
Дыхательный алкалоз может возникнуть у физически здорового человека в условиях высокогорья или при чрезмерной физической или психической нагрузке. Также он отмечается при одышке у пациентов с заболеваниями сердца и (или) легких, если углекислый газ не скапливается в легочных альвеолах.
Дыхательный ацидоз развивается при недостаточном поступлении воздуха в легкие, что может говорить об угнетении деятельности дыхательного центра в головном мозге, выраженной дыхательной недостаточности при тяжелой патологии легких.
Показатели осмотического и онкотического давления крови. Значение. Учебник
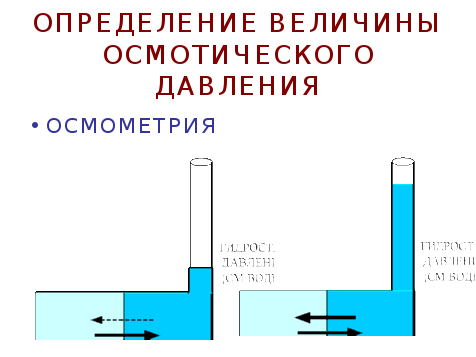





Определение осмотической резистентности эритроцитовРабота 3.5 – стр. 82
Определение осмотической резистентности эритроцитов (осмотической стойкости): используют набор гипотонических растворов NaCl (концентрация соли ниже 0.9%), помещают в них эритроциты исследуемой крови и отмечают концентрацию раствора, в котором (а) начинается гемолиз отдельных эритроцитов (в норме 0.48% NaCl и (б) происходит полный гемолиз всех эритроцитов (в норме 0.33% NaCl). Например, осмотическая стойкость эритроцитов уменьшается при сфероцитозе и увеличивается при талассемии.
Исследование буферных свойств сыворотки крови (опыт Фриденталя). Учебник
Показатель рН – 7.35 – 7.4 (отрицательный логарифм концентрации водородных ионов) – влияет на ход всех биохимических реакций в организме. Сдвиг рН в кислую сторону называется ацидозом, сдвиг в щелочную сторону – алкалозом. Регуляция рН: (1) В крови имеются буферные системы, которые могут связывать водородные и гидроксильные ионы и, таким образом, уменьшать колебания рН (доли секунды); (2) дыхательная система – удаление СО2 легкими (несколько минут); (3) выделительная функция почек – выведение кислых и щелочных продуктов обмена; самый медленный механизм (часы, дни), но самый мощный. Буферные системы крови: (1) бикарбонатный буфер (угольная кислота и бикарбонат натрия) – буферная система крови; (2) фосфатный буфер (гидрофосфат и дигидрофосфат натрия) – буферная система крови, почечных канальцев, а также внутриклеточная буферная система многих тканей; (3) гемоглобиновый буфер (восстановленный гемоглобин ННв и калиевая соль оксигенированного гемоглобина КНвО2) – буферная система эритроцитов, самая мощная (75% общей буферной емкости); (4) белковый буфер (амфолитные свойства белков) – буферная система крови, а также внутриклеточная буферная система.
Наблюдение буферных свойств плазмы крови (опыт Фриденталя).
Цель опыта: наглядная демонстрация буферных свойств плазмы крови.
Ход работы: Берут 2 чистых стаканчика и наливают в один 5 мл плазмы, а в другой 5 мл воды, прибавляют в оба стаканчика по капле метилового оранжевого и, считая капли, титруют 0,1 н раствором соляной кислоты до появления неисчезающего при взбалтывании красного окрашивания. Отмечают количество капель, пошедших на титрование воды и плазмы.
В чем суть опыта Фриденталя – в сравнении буферной емкости сыворотки крови и дистиллированной воды путем их титрования кислотой или щелочью в присутствии индикаторов.
Во сколько раз сыворотка крови более устойчива к закислению и защелачиванию, чем дистиллированная вода? - К закислению – в 300 – 400 раз, к защелачиванию – в 40 – 70 раз.
Значение минерального состава крови (Na, K, Ca) на примере работы сердца
Сердечная деятельность зависит от электролитного состава крови.
Важная роль в нормальной жизнедеятельности сердца принадлежит электролитам.
Изменения концентрации в крови солей калия и кальция оказывают весьма значительное влияние на автоматию и процессы возбуждения и сокращения сердца.
Избыток ионов калия угнетает все стороны сердечной деятельности, действуя отрицательно хронотропно (урежает ритм сердца), инотропно (уменьшает амплитуду сердечных сокращений), дромотропно (ухудшает проведение возбуждения в сердце), батмотропно (уменьшает возбудимость сердечной мышцы). При избытке ионов К+ сердце останавливается в диастоле. Резкие нарушения сердечной деятельности наступают и при уменьшении содержания ионов К+ в крови (при гипокалиемии).
Избыток ионов кальция действует в обратном направлении: положительно хронотропно, инотропно, дромотропно и батмотропно. При избытке ионов Са2+ сердце останавливается в систоле. При уменьшении содержания ионов Са2+ в крови сердечные сокращения ослабляются.
Таблица. Нейрогуморальная регуляция деятельности сердечно-сосудистой системы
|
Фактор |
Сердце |
Сосуды |
Уровень кровяного давления |
|
Ионы кальция |
учащают ритм и ослабляют сокращения |
суживают |
понижают |
|
Ионы калия |
замедляют ритм и ослабляют сокращения |
расширяют |
понижают |
Натрий - основной внеклеточный катион. Играет главную роль в поддержании осмотического давления - 90%. Участвует в возникновении и поддержании ПП и ПД, калий и натрий являются антагонистами на клеточном уровне, т.е. повышение содержания натрия приводит к уменьшению калия в клетке.

Гемолиз и его виды учебник
Гемолизом называется разрушение оболочки эритроцитов, сопровождающееся выходом гемоглобина в плазму крови, которая окрашивается при этом в красный цвет и становится прозрачной («лаковая кровь»).
Разрушение эритроцитов может быть вызвано уменьшением осмотического давления, что вначале приводит к набуханию, а затем к разрушению эритроцитов - это так называемый осмотический гемолиз (возникает в том случае, когда осмотическое давление окружающего эритроциты раствора уменьшается вдвое по сравнению с нормальным). Концентрация NaCl в окружающем клетку растворе, при которой начинается гемолиз, является мерой так называемой осмотической стойкости (резистентности) эритроцитов. У человека гемолиз начинается в 0,4% растворе NaCl, а в 0,34% растворе разрушаются все эритроциты. При различных патологических состояниях осмотическая стойкость эритроцитов может быть уменьшена и полный гемолиз может наступить и при больших концентрациях NaCl в растворе.
Химический гемолиз происходит под влиянием веществ, разрушающих белково-липидную мембрану эритроцитов— эфир, хлороформ, бензол, алкоголь, желчные кислоты, сапонин и некоторые другие вещества.
Механический гемолиз возникает под влиянием сильных механических воздействий, например в результате сотрясения ампулы с кровью.
Гемолиз также вызывают повторные замораживание и оттаивание крови – термический гемолиз.
Биологический гемолиз может возникать в организме под влиянием яда некоторых змей, микробов и паразитов крови (гемолитический стрептококк, палочка газовой гангрены, плазмодий малярии и др.), при переливании несовместимой крови и т.д.
Группы крови системы RhРабота 3.13 – стр. 95
Определение резус-принадлежности крови человека. Значение RhРабота 3.13 – стр. 95
Определения количества гемоглобина в крови по способу Сали, Работа 3.3 – стр.77
Определение количества гемоглобина. Принцип определения – колориметрический (сравнение цвета исследуемой крови со стандартными растворами). (а) Гемометрия: гемометр Сали – небольшой штатив с тремя пробирками, где в среднюю пробирку помещают исследуемую кровь, а две другие пробирки содержат стандартный раствор для сравнения. Исследуемую кровь смешивают с соляной кислотой (для гемолиза и образования солянокислого гематина коричневого цвета). Затем добавляют дистиллированную воду до тех пор, пока раствор исследуемой крови на будет такого же цвета, как стандартные растворы. Средняя пробирка имеет шкалу в единицах измерения количества гемоглобина. Нормальное содержание гемоглобина 130-160 г/л. (б) Фотоэлектроколориметрия (с использованием ФЭК).
Для измерения содержания гемоглобина существует много методов, в том числе:
1) определение количества связанного O2 (1 г НЬ может присоединить до 1,36 мл O2);
2) анализ уровня железа в крови (содержание железа в гемоглобине составляет 0,34%);
3) колориметрия (сравнение цвета крови с цветом стандартного раствора);
4) измерение экстинкции (спектрофотометрия). При проведении рутинных определений уровня гемоглобина отдают предпочтение последнему методу, так как при
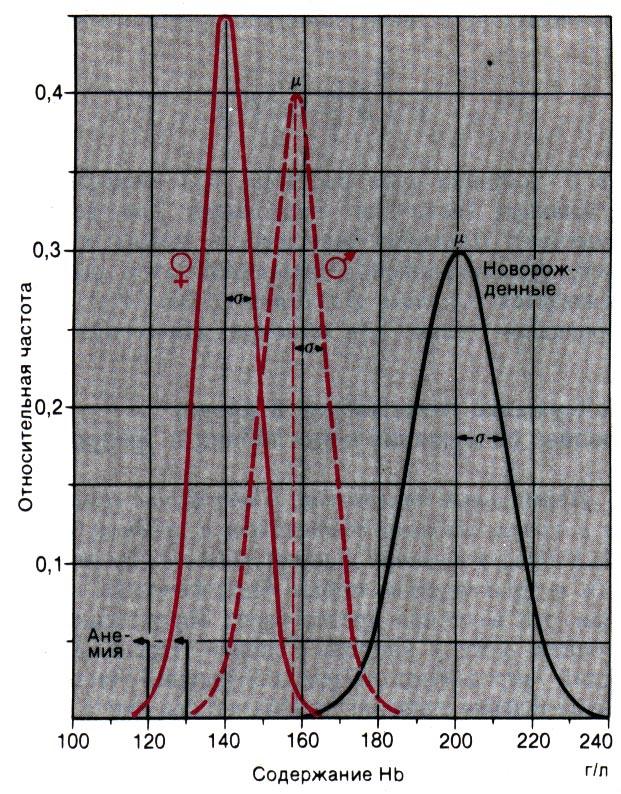
Рис. 22.5. Частотное распределение концентраций гемоглобина у взрослых мужчин (♂), взрослых женщин (♀) и новорожденных. По оси ординат–относительная частота встречаемости, по оси абсцисс–содержание гемоглобина; μ–среднее значение (медиана), ст–стандартное отклонение (величина, характеризующая разброс значений; соответствует расстоянию от медианы кривой нормального распределения до значения, соответствующего наиболее крутому участку этой кривой)
использовании первых двух способов необходима сложная аппаратура, а метод колориметрии неточен.
Спектрофотометрический анализ. Принцип метода состоит в определении содержания НЬ в крови по экстинкции монохроматического света. Поскольку растворенный гемоглобин нестабилен, а экстинкция зависит от степени оксигенации, его необходимо предварительно перевести в стабильную форму.
Спектрофотометрические измерения содержания гемоглобина производят следующим образом. Кровь набирают в капиллярную пипетку и затем смешивают с раствором, содержащим калий железосинеродистый (K3[Fe(CN)6]), цианистый калий (KCN) и бикарбонат натрия (NаНСО3). Под действием этих веществ эритроциты разрушаются, и гемоглобин превращается в циан–метгемоглобин HbCN (содержащий трехвалентное железо), способный сохраняться в течение нескольких недель. При спектрофотометрии раствор цианметгемоглобина освещают монохроматическим светом с длиной волны 546 нм и определяют экстинкцию Е. Зная коэффициент экстинкции e и толщину слоя раствора d, можно, исходя из закона Ламберта–Бэра [уравнение (2)], определить концентрацию раствора С непосредственно по величине экстинкции Е. Чаще предпочитают, однако, предварительно откалибровать шкалу экстинкции при помощи стандартного раствора. В настоящее время цианметгемоглобиновый метод считается наиболее точным из общепринятых способов измерения содержания гемоглобина [32].
Расчет цветового показателя крови.
Цветовой показатель крови (ЦП) показывает содержание гемоглобина в одном эритроците исследуемой крови по сравнению с нормой.
Нв (иссл.крови)________ Нв (станд)_______ Нв (иссл.крови) х эритроциты (станд)
эритроциты (иссл.крови) эритроциты (станд) эритроциты (иссл.крови) х Нв (станд)
Нв (иссл.крови) х 5.1012/л_______ (При делении 500 на 167 получается примерно 3)
эритроциты (иссл.крови) х 167 г/л
Упрощенная формула для вычисления ЦП: Нв (иссл.крови)_______ х 3
эритроциты (иссл.крови)
(первые три цифры)
Например, если Нв = 150 г/л, эритроцитов 4,5 х 1012/л, то ЦП = 1, т.к. (150 : 450) х 3 = 1
если Нв = 120 г/л, эритроцитов 4,8 х 1012/л, то ЦП = 0,75 т.к. (120 : 480) х 3 = 0,75
Примечание:если ЦП меньше 1 – это гипохромная анемия (например, железодефицитная).
Если ЦП больше 1 – это гиперхромная анемия (гемолитическая).
Определение скорости оседания эритроцитов (СОЭ) Работа 3.7 – стр.84
Определение СОЭ(скорость оседания эритроцитов): кровь и цитрат натрия (антикоагулянт) в соотношении 4:1 – в стеклянном капилляре оставляют на 1 час в строго вертикальном положении. Эритроциты оседают и в верхней части капилляра появляется столбик светлой плазмы крови. СОЭ в норме от 2 до 15 мм/час. СОЭ зависит от состава плазмы и свойств эритроцитов. Например, глобулины и фибриноген (крупномолекулярные белки) при хроническом воспалении, беременности способствуют образованию «монетных столбиков» и увеличивают СОЭ; альбумины (низкомолекулярные белки) препятствуют образованию «монетных столбиков» и уменьшают СОЭ.
Правила переливания цельной крови и отмытых эритроцитов. Учебник
Правила переливания крови: (1) определить группу крови в системе АВО, (2) определить резус-принадлежность, (3) провести пробу на биологическую совместимость крови донора и реципиента. Проба на биологическую совместимость необходима для выявления иммунных антител к другим, более редким антигенам эритроцитов (N,M,P,Левис,Даффи,Кидд и др.). Она проводится (а) in vitro – на фарфоровой тарелке: перекрестная проба при которой эритроциты донора смешивают с плазмой реципиента и эритроциты реципиента – с плазмой донора; и (б) in vivo – вводя реципиенту небольшой объем донорской крови (10-15 мл) внутривенно.
