
- •Предисловие.
- •1 Модуль, общая, неорганическая и физическая химия.
- •Тема 1. Способы выражения концентрации раствора.
- •Тема 2. Термодинамика.
- •Тема 3. Химическое равновесие.
- •Тема 4. Осмос.
- •Тема 5. Поверхностное натяжение, пав, пнв, пив и адсорбция.
- •Тема 6. Химическая кинетика.
- •Тема 7. Электролиты. РН.
- •Тема 8. Буферные растворы.
- •Тема 9. Комплексные и малорастворимые соединения…
- •Тема 10. Потенциал, эдс.
- •Тема 11. Ультрамикрогетерогенные системы. Мицеллы.
- •2 Модуль, Органика
- •Тема 1. Номенклатура.
- •Тема 2. Электронное строение.
- •Тема 3. Реакции sr, ae, se.
- •Тема 4. Реакции sn. Свойства соединений с σ – связью…
- •Тема 5. Реакции альдегидов, кетонов, карбоновых кислот и их производных.
Предисловие.
Будучи огорчен качеством преподавания химии в РНИИМУ, и тем более способом последующего контроля качества образования – тестами, я решил оказать посильную помощь студентам в сдаче оных. Пособие представляет собой краткую, насколько возможно, инструкцию, как, минимально загрузив голову, таки сдать этот окаянный тест. Я исследовал большое их количество, обобщил результаты. Вопросы были мной разделены на темы в таком порядке, в каком вы их изучали или якобы изучали, кому как повезло. На каждый вид вопросов я постарался дать ответ, в меру научный, чтобы все-таки не слишком уйти от своих химических корней, но и достаточно ясный, чтобы он мог быть воспринят среднестатистическим студентом РНИИМУ. Теперь я представляю свой труд на суд и пользование широкой общественности, надеюсь, моё творение сможет послужить к чьей-нибудь пользе.
Заранее благодарен за адекватные комментарии, дополнения и исправления к тексту. Текст создан исключительно из гуманных соображений и распространяется безвозмездно.
Удачи, ни пуха ни пера, дорогие любители химии.
Федоров Алексей, «Леша-химик»
15.01.2015
1 Модуль, общая, неорганическая и физическая химия.
Тема 1. Способы выражения концентрации раствора.
Введение. Весьма полезно будет иметь под рукой таблицу из голубой методички. Там есть, в случае чего и определений молярности-моляльности, и формулы этих ваших моляльностей.
Типичные вопросы:
Молярная концентрация.
Пример:
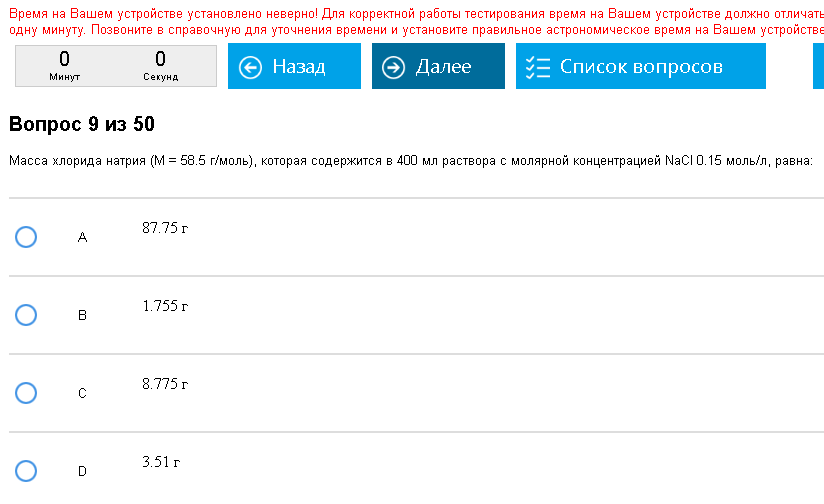
Внезапная задача.
Как с этим бороться:
Формула с=n/V, гдеc-молрная концентрация, моль/л,n-количество вещества, моль,V- объем, обязательно в л (!). Среднестатистический вопрос – необходимо вычислить массу растворенного вещества, если известно с иV, причем объем обычно в мл. Сначала из первой формулы вычисляем количество вещества, умножаем объем на молярность, (объем нужно перевести в литры, для этого мили литры делят на 1000). Затем по известной формулеn=m/Mнаходят массу, умножают молярную на количество вещества. Можно все сразу объединить в одну формулу,m=cVM, просто все перемножить, только объем в литры все равно надо перевести. Встречаются более редкие вариации этой задачи, например найти количество моль, это даже легче, решается в одно действие.
Масса, плотность и объем.
Пример:

Ответ D, догадались же?
Как с этим бороться:
Масса (m), плотность (ρ) и объем (V) раствора (внимание, НЕ растворенного вещества) связаны соотношениями:m=Vρ,V=m/ρ, ρ=m/V, с чем мы вас и поздравляем.
Растворимость.
Пример:
?
Не помню, еще перед новым годом находил один какой то вопрос.
Как с этим бороться:
Растворимость газов увеличивается с увеличением давления и уменьшением температуры, там вроде про это было.
Размерности физических величин.
Пример:

Массовая доля - %! Ура, товарищи!
Как с этим бороться:
Вы таки долго будете смеяться, но масса измеряется в граммах и килограмах, объем в милилитрах и литрах, плотность в г/мл. Остальные размерности концентраций, как например моляльность моль/кг растворителя, могут быть найдены в методичке.
Массовая доля.
Пример:

Примерчик.
Как с этим бороться:
Массовая доля ω, масса растворенного вещества m(X) и масса раствораm(р-р) связаны нехитрым соотношением ω=m(X)/m(р-р), из чего следует, чтоm(X)= ω·m(р-р), аm(p-p) =m(X)/ω. Чего же вам еще более? Из сложного, периодически встречались в 1 модуле хитровыкрученные задачи, где требовалось узнать массу воды, которую надо добавить к раствору с известной массой и массовой долей, чтобы разбавить его до тоже известной массовой доли. Ну, например от 15% до 10%. Решались проще всего подбором. Находим, сколько растворенного вещества в 15% растворе, затем прибавляем 1ое количество воды к нему (растворенное вещество остается той же массы, а вот масса раствора увеличивается за счет долитой воды) и смотрим, получилось 10% или нет. И так далее. Но в итоговом я таких не видел. Математика все таки великая вещь.
Неизвестный пока науке вид задач.
Пример:
?
Неизвестен.
Как с этим бороться:
Пока непонятно.
